CHƯƠNG 1. CẤU TẠO NGUYÊN TỬ A. PHẦN LÍ THUYẾT
BÀI 1. THÀNH PHẦN NGUYÊN TỬ
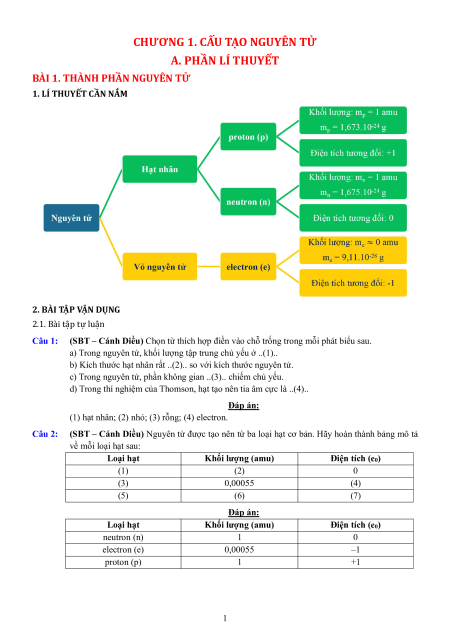
1. LÍ THUYẾT CẦN NẮM 2. BÀI TẬP VẬN DỤNG
2.1. Bài tập tự luận
Câu 1: (SBT – Cánh Diều) Chọn từ thích hợp điền vào chỗ trống trong mỗi phát biểu sau.
a) Trong nguyên tử, khối lượng tập trung chủ yếu ở . (1).
b) Kích thước hạt nhân rất . (2). so với kích thước nguyên tử.
c) Trong nguyên tử, phần không gian . (3). chiếm chủ yếu.
d) Trong thí nghiệm của Thomson, hạt tạo nên tia âm cực là . (4). Đáp án:
(1) hạt nhân; (2) nhỏ; (3) rỗng; (4) electron.
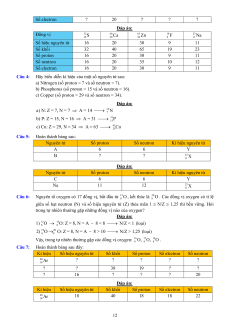
Câu 2: (SBT – Cánh Diều) Nguyên tử được tạo nên từ ba loại hạt cơ bản. Hãy hoàn thành bảng mô tả về mỗi loại hạt sau: Loại hạt Khối lượng (amu) Điện tích (e0) (1) (2) 0 (3) 0,00055 (4) (5) (6) (7) Đáp án: Loại hạt Khối lượng (amu) Điện tích (e0) neutron (n) 1 0 electron (e) 0,00055 –1 proton (p) 1 +1 1
Câu 3: (SBT – Cánh Diều) Một nguyên tử C có 6 proton và 6 neutron. Một nguyên tử O có 8 proton
và 8 neutron. Xét các phân tử CO và CO2 tạo nên từ các nguyên tử O và C ở trên. Hãy nối một
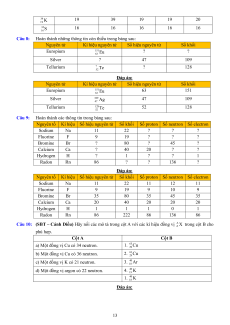
vế ở cột A tương ứng với một hoặc nhiều về ở cột B. Cột A Cột B a) Phân tử CO
1. có số proton và số neutron bằng nhau. b) Phân tử CO2
2. có khối lượng xấp xỉ 28 amu.
3. có khối lượng xấp xỉ 44 amu. 4. có 22 electron.
5. có số hạt mang điện nhiều gấp hai lần số hạt không mang điện. Đáp án: (a) – (1), (2) và (5) (b) – (1), (3), (4) và (5)
Câu 4: Tính tổng số electron, proton và neutron trong một phân tử nước (H2O). Biết trong phân tử này,
nguyên tử H chỉ tạo nên từ 1 proton và 1 electron; nguyên tử O có 8 neutron và 8 proton. Đáp án:
- H: P = E = 1, N = 0; O: P = E = 8; N = 8.
- Tổng số hạt electron trong H2O: 1.2 + 8 = 10.
- Tổng số hạt proton trong H2O: 1.2 + 8 = 10.
- Tổng số hạt neutron trong H2O: 8.
- Vậy tổng số hạt trong H2O là: 2.2 + 8.3 = 28 hạt.
Câu 5: Nguyên tử oxygen–16 có 8 proton, 8 neutron và 8 electron. Tính khối lượng nguyên tử oxygen theo đơn vị gam và amu? Đáp án: 24 24 28 23 + m
= 8.1,673.10 + 8.1,675.10 + 8.9,11.10 2,6784.10 gam O(gam) + m
= 8.1 + 8.1 + 8.0,00055 16,0044 amu O(amu)
Câu 6: Một loại nguyên tử nitrogen có 7 proton và 7 neutron trong hạt nhân. Tính khối lượng hạt nhân
và khối lượng nguyên tử nitrogen theo đợn vị amu và gam? Đáp án: 24 24 28 23 + m
= 7.1,673.10 + 7.1,675.10 + 7.9,11.10 2,344.10 gam N(gam) + m
= 7.1 + 7.1 + 7.0,00055 14,00385 amu N(amu)
Câu 7: Nguyên tử aluminium (Al) gồm 13 proton và 14 neutron. Tính khối lượng proton, neutron và
electron có trong 27 gam aluminium. Đáp án: - n = 1 mol
số nguyên tử Al: 1.6,023.1023 (nguyên tử). Al(27gam) 23 2 4
m = 13.6,023.10 .1,673.10 = 13,1 gam - 23 p P = E = 13.6,023.10 23 2 8 3
m = 13.6,023.10 .9,11.10 = 7,133.10 gam e - 23 23 2 4 N = 14.6,023.10
m = 14.6,023.10 .1,675.10 = 14,124 gam n
Câu 8: Trong một nguyên tử sulfur (S) có 16 electron và 16 neutron.
a) Tính khối lượng (gam) electron, proton và neutron trong 1 mol nguyên tử sulfur.
b) Tính khối lượng (gam) 1 mol nguyên tử sulfur. Từ kết quả đó coi khối lượng nguyên tử thực
tế bằng khối lượng hạt nhân được không? Đápán: - n = 1 mol
số nguyên tử S: 1.6,023.1023 (nguyên tử). S 2 23 24
m = 16.6,023.10 .1,673.10 = 16,12 gam p 23 P = E = 16.6,023.10 a) 23 28 3
m = 16.6,023.10 .9,11.10 = 8,78.10 gam e 23 N = 16.6,023.10 23 24
m = 16.6,023.10 .1,675.10 = 16,14 gam n
b) m = m + m + m = 32,27 gam . Vậy, khối lượng nguyên tử thực tế gần bằng khối lượng nt p n e hạt nhân.
2.2. Trắc nghiệm nhiều phương án lựa chọn
Câu 1: Các hạt cấu tạo nên hạt nhân của hầu hết các nguyên tử là A. electron và proton. B. proton và neutron.
C. neutron và electron.
D. electron, proton và neutron.
Câu 2: Các hạt cấu tạo nên hầu hết các nguyên tử là A. electron và proton. B. proton và neutron.
C. neutron và electron.
D. electron, proton và neutron.
Câu 3: Nguyên tử chứa những hạt mang điện là A. proton và α.
B. proton và neutron. C. proton và electron. D. electron và neutron.
Câu 4: Loại hạt được tìm thấy trong hạt nhân và không mang điện là A. electron. B. neutron. C. proton. D. photon.
Câu 5: Loại hạt được tìm thấy trong hạt nhân và mang điện tích dương là A. electron. B. neutron. C. proton. D. photon.
Câu 6: Loại hạt được tìm thấy trong vỏ nguyên tử và mang điện tích âm? A. electron. B. neutron. C. proton. D. photon.
Câu 7: Khi các nguyên tử tiến lại gần nhau để hình thành liên kết hóa học, sự tiếp xúc đầu tiên giữa hai
nguyên tử sẽ xảy ra giữa
A. lớp vỏ với lớp vỏ.
B. lớp vỏ với hạt nhân.
C. hạt nhân với hạt nhân.
D. hạt nhân với nguyên tử.
Câu 8: Nguyên tử gồm hạt nhân và vỏ nguyên tử. Vỏ nguyên tử chứa loại hạt nào sau đây? A. Proton. B. Electron.
C. Proton và neutron. D. Neutron.
Câu 9: Hạt nhân nguyên tử Na có 11 proton và 12 neutron. Số electron trong nguyên tử Na là A. 12. B. 11. C. 23. D. 22.
Câu 10: Hạt nhân của nguyên tử nguyên tố A có 24 hạt, trong đó số hạt không mang điện là 12. Số electron trong A là A. 12. B. 24. C. 13. D. 6.
Câu 11: Nguyên tử trung hòa về điện vì
A. được tạo nên bởi các hạt không mang điện.
B. có tổng số hạt proton bằng tổng số hạt electron.
C. có tổng số hạt electron bằng tổng số hạt neutron.
D. tổng số hạt neutron bằng tổng số hạt proton.
Câu 12: Nguyên tử oxygen (O) có 8 electron. Điện tích hạt nhân của nguyên tử oxygen là A. –8. B. +8. C. –16. D. 16.
Câu 13: Các đám mây gây hiện tượng sấm sét tạo nên bởi những hạt nước nhỏ li ti mang điện tích. Một
phép đo thực nghiệm cho thấy, một giọt nước có đường kính 50 μm, mang một lượng điện tích 3
âm là –3,33.10–17 C. Hãy cho biết điện tích âm của giọt nước trên tương đương với điện tích của bao nhiêu electron? A. 208. B. 2,08. C. 1. D. 108.
Câu 14: Nếu phóng đại một nguyên tử gold (Au) lên 1 tỉ (109) lần thì kích thước của nó tương đương
một quả bóng rổ (có đường kính 30cm) và kích thước của hạt nhân tương đương một hạt cát
(có đường kính 0,003cm). Cho biết kích thước nguyên tử Au lớn hơn so với hạt nhân bao nhiêu lần? A. 10000. B. 1000. C. 100. D. 10.
Câu 15: Thành phần nào không bị lệch hướng trong trường điện? A. Tia α. B. Proton.
C. Nguyên tử hydrogen. D. Tia âm cực.
Câu 16: Trong nguyên tử aluminium (Al), số hạt mang điện tích dương là 13, số hạt không mang điện là
14. Số hạt electron trong Al là A. 13. B. 15. C. 27. D. 14.
Câu 17: Đặc điểm của electron là
A. mang điện tích dương và có khối lượng.
B. mang điện tích âm và có khối lượng.
C. không mang điện và có khối lượng.
D. mang điện tích âm và không có khối lượng.
Câu 18: Trường hợp nào sau đây có sự tương ứng giữa hạt cơ bản với khối lượng và điện tích của chúng?
A. Proton, m ≈ 0,00055 amu, q = +1.
B. Neutron, m ≈ 1 amu, q = 0.
C. Electron, m ≈ 1 amu, q = –1.
D. Proton, m ≈ 1 amu, q = -–1.
Câu 19: Khối lượng của nguyên tử magnesium là 39,8271.10–27 kg. Khối lượng của magnesium theo amu là A. 23,985. B. 66,133.10–51. C. 24,000. D. 23,985.10–3.
Câu 20: Nguyên tử là phần tử nhỏ nhất của chất và A. không mang điện.
B. mang điện tích dương.
C. mang điện tích âm.
D. có thể mang điện hoặc không mang điện.
Câu 21: Số đơn vị điện tích hạt nhân của nguyên tử X là 53. Nguyên tử chứa
A. 53 electron và 53 proton.
B. 53 electron và 53 neutron.
C. 53 proton và 53 neutron. D. 53 neutron.
Câu 22: Oxygen (O) có khối lượng nguyên tử là 15,999 amu. Khối lượng 1 nguyên tử oxygen tính theo đơn vị gam là A. 26,566.10–24 gam.
B. 26,665.10–24 gam. C. 26,656.10–24 gam. D. 26,556.10–24 gam.
Câu 23: Beryllium (Be) có khối lượng nguyên tử là 9,012 amu. Khối lượng 1 nguyên tử beryllium tính theo đơn vị gam là A. 14,960.10–24 gam.
B. 14,694.10–24 gam. C. 14,649.10–24 gam. D. 14,464.10–24 gam.
Câu 24: Thông tin nào sau đây không đúng?
A. Proton mang điện tích dương, nằm trong hạt nhân, khối lượng gần bằng 1 amu.
B. Electron mang điện tích âm, nằm trong hạt nhân, khối lượng gần bằng 0 amu.
C. Neutron không mang điện, khối lượng gần bằng 1 amu.
D. Nguyên tử trung hòa điện, có kích thước lớn hơn nhiều so với hạt nhân, nhưng có khối
lượng gần bằng khối lượng hạt nhân.
Câu 25: Cho 1 mol kim loại X. Phát biểu nào dưới đây đúng?
A. 1 mol X chứa số lượng nguyên tử bằng số lượng nguyên tử trong 1 mol nguyên tử hydrogen. 4
Chuyên đề dạy thêm Hóa 10 (cấu trúc mới)
8.7 K
4.4 K lượt tải
200.000 ₫
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
- Tailieugiaovien.com.vn giới thiệu Chuyên đề dạy thêm Hóa lớp 10 dành cho cả 3 sách mới gồm: 7 chủ đề nhằm giúp Giáo viên có thêm tài liệu tham khảo tài liệu môn Hóa lớp 10.
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(8735 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)