Ngày soạn: .../.../... Ngày dạy: .../.../...
Trường: ……………………. Họ và tên giáo viên:
Tổ: ………………………….
………………………………..
BÀI 6. XU HƯỚNG BIẾN ĐỔI MỘT SỐ TÍNH CHẤT CỦA NGUYÊN TỬ CÁC
NGUYÊN TỐ TRONG MỘT CHU KÌ VÀ TRONG MỘT NHÓM (3 tiết) I. MỤC TIÊU:
1. Kiến thức: Học xong bài này, HS đạt các yêu cầu sau:
- Giải thích được xu hướng biến đổi bán kính nguyên tử trong một chu kì, trong một
nhóm (nhóm A) (dựa theo lực hút tĩnh điện của hạt nhân với electron ngoài cùng và dựa
theo số lớp electron tăng trong một nhóm theo chiều từ trên xuống dưới).
- Nhận xét và giải thích được xu hướng biến đổi độ âm điện và tính kim loại, phi kim
của nguyên tử nguyên tố trong một chu kì, trong một nhóm (nhóm A). 2. Năng lực - Năng lực chung:
+ Năng lực tự chủ và tự học trong tìm tòi khám phá.
+ Năng lực giao tiếp và hợp tác trong trình bày, thảo luận và làm việc nhóm.
+ Năng lực giải quyết vấn đề và sáng tạo trong thực hành, vận dụng. - Năng lực riêng:
+ Năng lực sử dụng ngôn ngữ hóa học: sử dụng các thuật ngữ hóa học, tên các nguyên tố hóa học trong bài học.
+ Nhận xét và giải thích được xu hướng biến đổi độ âm điện và tính kim loại, phi kim
của nguyên tử nguyên tố trong một chu kì, trong một nhóm (nhóm A). 3. Phẩm chất
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
- Có ý thức học tập, ý thức tìm tòi, khám phá và sáng tạo, có ý thức làm việc nhóm, tôn
trọng ý kiến các thành viên khi hợp tác.
- Chăm chỉ tích cực xây dựng bài, có trách nhiệm, chủ động chiếm lĩnh kiến thức theo sự hướng dẫn của GV.
Hình thành tư duy logic, lập luận chặt chẽ, và linh hoạt trong quá trình suy nghĩ.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
1. Đối với GV: SGK, Tài liệu giảng dạy, giáo án điện tử, bảng tuần hoàn các nguyên tố
hóa học cỡ lớn, bảng độ âm điện của một số nguyên tố hóa học cỡ lớn, đồ thị biến đổi
bán kính nguyên tử và độ âm điện cỡ lớn. Có thể chuẩn bị thí nghiệm biểu diễn (hoặc
tranh ảnh video mô tả thí nghiệm).
2. Đối với HS: SGK, SBT, vở ghi, giấy nháp, đồ dùng học tập (bút, thước...), bảng
nhóm, bút viết bảng nhóm.
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG (MỞ ĐẦU)
a) Mục tiêu: Yêu cầu học sinh dự đoán trước một phần nội dung sẽ được học trong bài mới.
Gợi tâm thế, tạo hứng thú học tập.
b) Nội dung: Giáo viên nêu yêu cầu, các HS suy nghĩ đưa ra dự đoán.
c) Sản phẩm: Học sinh dự đoán được xu hướng thay đổi kích thước nguyên tử của các
nguyên tố theo chiều tăng điện tích hạt nhân trong bảng tuần hoàn.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ:
-GV yêu cầu HS dự đoán xu hướng thay đổi kích thước nguyên tử của các nguyên tố
theo chiều tăng điện tích hạt nhân trong bảng tuần hoàn các nguyên tố hóa học:
+ Trong một chu kì, bán kính nguyên tử của các nguyên tố tăng hay giảm dần?
+ Trong một nhóm, bán kính của nguyên tử của các nguyên tố tăng hay giảm dần?
Bước 2: Thực hiện nhiệm vụ
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
- HS suy nghĩ, hoàn thành yêu cầu của GV đưa ra.
Bước 3: Báo cáo, thảo luận:
- GV gọi HS trả lời, HS khác nhận xét, bổ sung.
Bước 4: Kết luận, nhận định:
- Sau khi HS đưa ra dự đoán, GV dẫn vào bài mới: Để kiểm tra dự đoán của các em có
chính xác hay không, chúng ta cùng nhau đi tìm hiều bài mới: Bài 6. Xu hướng biến đổi
một số tính chất của nguyên tử các nguyên tố trong một chu kì và trong một nhóm.
B. HÌNH THÀNH KIẾN THỨC MỚI
Hoạt động 1: Cấu hình electron nguyên tử của các nguyên tố nhóm A. Bán kính
nguyên tử - độ âm điện.
a) Mục tiêu: Giải thích xu hướng biến đổi bán kính nguyên tử, độ âm điện của nguyên
tử các nguyên tố trong một chu kì, trong một nhóm (nhóm A).
b) Nội dung: HS đọc SGK, trả lời câu hỏi để tìm hiểu nội dung kiến thức theo yêu cầu của GV.
c) Sản phẩm: HS trình bày được xu hướng biến đổi và tương đồng về tính chất của các
nguyên tố trong một chu kì và trong một nhóm, giải được câu hỏi ?1,2 sgk.
d) Tổ chức thực hiện:
HOẠT ĐỘNG CỦA GV VÀ HS
SẢN PHẨM DỰ KIẾN
Bước 1: Chuyển giao nhiệm vụ:
I. Cấu hình electron nguyên tử của
-GV yêu cầu HS dựa vào kiến thức bài 5 nguyên tố nhóm A.
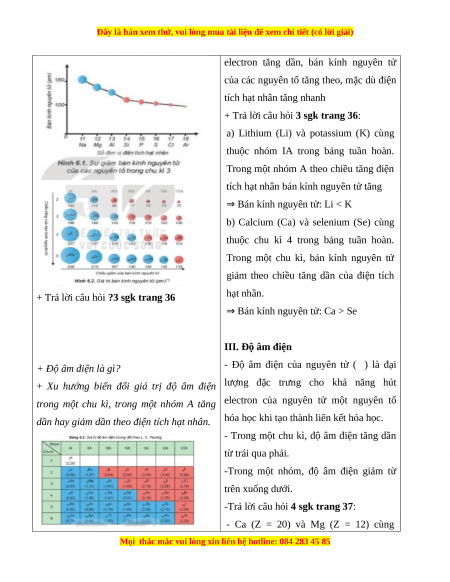
và nghiên cứu bảng 6.1 sgk trang 34 nhận - Nhóm A gồm các nguyên tố nhóm s và
xét nguyên nhân biến đổi tuần hoàn của p.
các nguyên tố, trả lời câu hỏi 1,2 sgk trang - Sự giống nhau của số electron hóa trị 35:
dẫn đến sự tương tự nhau về tính chất
+ Nhóm A gồm các nguyên tố nào trong 4 hóa học của các nguyên tố trong cùng
loại nguyên tố s, p, d, f? nhóm A.
+ Vì sao các nguyên tố trong cùng một ⇒ Sự biến đổi tuần hoàn của cấu hình
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
nhóm thì có tính chất hóa học tương tự electron lớp ngoài cùng là nguyên nhân nhau?
sự biến đổi tuần hoàn về tính chất các
+ Sau mỗi chu kì, cấu hình electron lớp nguyên tố.
ngoài cùng có lặp lại không? Điều này dẫn
đến sự biến đổi như thế nào về tính chất -Trả lời câu hỏi ?1 sgk trang 35:
của các nguyên tố?
+ Trả lời câu hỏi ?1,2 sgk trang 35.
-Trả lời câu hỏi ?2 sgk trang 35:
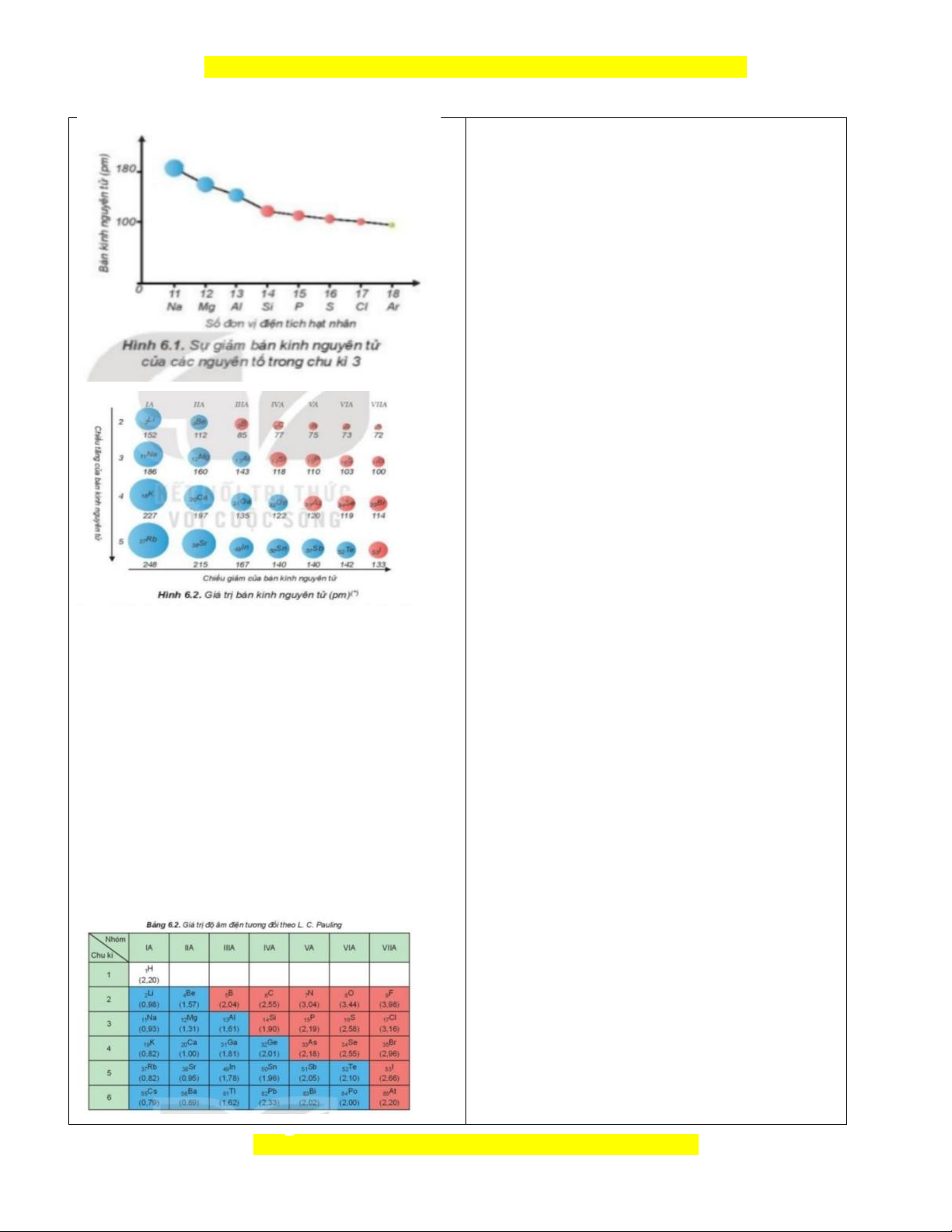
II. Bán kính nguyên tử
-GV yêu cầu HS quan sát hình ảnh, bảng - Một cách gần đúng, bán kính nguyên tử
và đề nghị nêu nhận xét, giải thích xu được xác định bằng một nửa khoảng cách
hướng biến đổi bán kính nguyên tử, độ âm trung bình giữa hai hạt nhân trong chất
điện trong một chu kì, trong một nhóm:
rắn đơn chất hoặc trong phân tử hai
+ Electron chuyển động hỗn loạn xung nguyên tử giống nhau.
quanh hạt nhân, vậy làm thế nào để xác - Trong một chu kì, bán kính nguyên tử
định được bán kính của một nguyên tử?
giảm dần theo chiều tăng dần của điện
+ Nhận xét xu hướng biến đổi bán kính tích hạt nhân. Do trong một chu kì điện
tăng dần hay giảm dần trong một chu kì, tích hạt nhân tăng, số lớp electron không trong một nhóm A.
đổi nên lực hút giữa hạt nhân với các
+ Giải thích nguyên nhân xu hướng biến electron lớp ngoài cùng cũng tăng theo.
đổi bán kính dựa vào lực hút tĩnh điện giữa - Trong một nhóm A, bán kính nguyên tử
hạt nhân, các electron và số lớp electron.
tăng dần theo chiều tăng dần của điện
tích hạt nhân. Do trong một nhóm A,
theo chiều từ trên xuống dưới số lớp
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
Giáo án Bài 6: Xu hướng biến đổi tính chất của nguyên tử các nguyên tố trong một chu kì và trong một nhóm Hóa học 10 Kết nối tri thức
1.1 K
554 lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Bộ giáo án Hóa học 10 Kết nối tri thức được cập nhật liên tục trong gói này từ nay đến hết tháng 6/2023.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Bộ giáo án Hóa học 10 Kết nối tri thức năm 2023 mới, chuẩn nhất được thiết kế theo phong cách hiện đại, đẹp mắt, trình bày chi tiết cho từng bài học và bám sát chương trình Sách giáo khoa Hóa học 10 Kết nối tri thức.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(1108 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN Hóa Học
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Lớp 10
Xem thêmTài liệu bộ mới nhất

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Ngày soạn: .../.../...
Ngày dạy: .../.../...
Trường: …………………….
Tổ: ………………………….
Họ và tên giáo viên:
………………………………..
BÀI 6. XU HƯỚNG BIẾN ĐỔI MỘT SỐ TÍNH CHẤT CỦA NGUYÊN TỬ CÁC
NGUYÊN TỐ TRONG MỘT CHU KÌ VÀ TRONG MỘT NHÓM
(3 tiết)
I. MỤC TIÊU:
1. Kiến thức: Học xong bài này, HS đạt các yêu cầu sau:
- Giải thích được xu hướng biến đổi bán kính nguyên tử trong một chu kì, trong một
nhóm (nhóm A) (dựa theo lực hút tĩnh điện của hạt nhân với electron ngoài cùng và dựa
theo số lớp electron tăng trong một nhóm theo chiều từ trên xuống dưới).
- Nhận xét và giải thích được xu hướng biến đổi độ âm điện và tính kim loại, phi kim
của nguyên tử nguyên tố trong một chu kì, trong một nhóm (nhóm A).
2. Năng lực
- Năng lực chung:
+ Năng lực tự chủ và tự học trong tìm tòi khám phá.
+ Năng lực giao tiếp và hợp tác trong trình bày, thảo luận và làm việc nhóm.
+ Năng lực giải quyết vấn đề và sáng tạo trong thực hành, vận dụng.
- Năng lực riêng:
+ Năng lực sử dụng ngôn ngữ hóa học: sử dụng các thuật ngữ hóa học, tên các nguyên tố
hóa học trong bài học.
+ Nhận xét và giải thích được xu hướng biến đổi độ âm điện và tính kim loại, phi kim
của nguyên tử nguyên tố trong một chu kì, trong một nhóm (nhóm A).
3. Phẩm chất
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
- Có ý thức học tập, ý thức tìm tòi, khám phá và sáng tạo, có ý thức làm việc nhóm, tôn
trọng ý kiến các thành viên khi hợp tác.
- Chăm chỉ tích cực xây dựng bài, có trách nhiệm, chủ động chiếm lĩnh kiến thức theo sự
hướng dẫn của GV.
Hình thành tư duy logic, lập luận chặt chẽ, và linh hoạt trong quá trình suy nghĩ.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
1. Đối với GV: SGK, Tài liệu giảng dạy, giáo án điện tử, bảng tuần hoàn các nguyên tố
hóa học cỡ lớn, bảng độ âm điện của một số nguyên tố hóa học cỡ lớn, đồ thị biến đổi
bán kính nguyên tử và độ âm điện cỡ lớn. Có thể chuẩn bị thí nghiệm biểu diễn (hoặc
tranh ảnh video mô tả thí nghiệm).
2. Đối với HS: SGK, SBT, vở ghi, giấy nháp, đồ dùng học tập (bút, thước...), bảng
nhóm, bút viết bảng nhóm.
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG (MỞ ĐẦU)
a) Mục tiêu: Yêu cầu học sinh dự đoán trước một phần nội dung sẽ được học trong bài
mới.
Gợi tâm thế, tạo hứng thú học tập.
b) Nội dung: Giáo viên nêu yêu cầu, các HS suy nghĩ đưa ra dự đoán.
c) Sản phẩm: Học sinh dự đoán được xu hướng thay đổi kích thước nguyên tử của các
nguyên tố theo chiều tăng điện tích hạt nhân trong bảng tuần hoàn.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ:
-GV yêu cầu HS dự đoán xu hướng thay đổi kích thước nguyên tử của các nguyên tố
theo chiều tăng điện tích hạt nhân trong bảng tuần hoàn các nguyên tố hóa học:
+ Trong một chu kì, bán kính nguyên tử của các nguyên tố tăng hay giảm dần?
+ Trong một nhóm, bán kính của nguyên tử của các nguyên tố tăng hay giảm dần?
Bước 2: Thực hiện nhiệm vụ
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
- HS suy nghĩ, hoàn thành yêu cầu của GV đưa ra.
Bước 3: Báo cáo, thảo luận:
- GV gọi HS trả lời, HS khác nhận xét, bổ sung.
Bước 4: Kết luận, nhận định:
- Sau khi HS đưa ra dự đoán, GV dẫn vào bài mới: Để kiểm tra dự đoán của các em có
chính xác hay không, chúng ta cùng nhau đi tìm hiều bài mới: Bài 6. Xu hướng biến đổi
một số tính chất của nguyên tử các nguyên tố trong một chu kì và trong một nhóm.
B. HÌNH THÀNH KIẾN THỨC MỚI
Hoạt động 1: Cấu hình electron nguyên tử của các nguyên tố nhóm A. Bán kính
nguyên tử - độ âm điện.
a) Mục tiêu: Giải thích xu hướng biến đổi bán kính nguyên tử, độ âm điện của nguyên
tử các nguyên tố trong một chu kì, trong một nhóm (nhóm A).
b) Nội dung: HS đọc SGK, trả lời câu hỏi để tìm hiểu nội dung kiến thức theo yêu cầu
của GV.
c) Sản phẩm: HS trình bày được xu hướng biến đổi và tương đồng về tính chất của các
nguyên tố trong một chu kì và trong một nhóm, giải được câu hỏi ?1,2 sgk.
d) Tổ chức thực hiện:
HOẠT ĐỘNG CỦA GV VÀ HS SẢN PHẨM DỰ KIẾN
Bước 1: Chuyển giao nhiệm vụ:
-GV yêu cầu HS dựa vào kiến thức bài 5
và nghiên cứu bảng 6.1 sgk trang 34 nhận
xét nguyên nhân biến đổi tuần hoàn của
các nguyên tố, trả lời câu hỏi 1,2 sgk trang
35:
+ Nhóm A gồm các nguyên tố nào trong 4
loại nguyên tố s, p, d, f?
+ Vì sao các nguyên tố trong cùng một
I. Cấu hình electron nguyên tử của
nguyên tố nhóm A.
- Nhóm A gồm các nguyên tố nhóm s và
p.
- Sự giống nhau của số electron hóa trị
dẫn đến sự tương tự nhau về tính chất
hóa học của các nguyên tố trong cùng
nhóm A.
⇒ Sự biến đổi tuần hoàn của cấu hình
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
nhóm thì có tính chất hóa học tương tự
nhau?
+ Sau mỗi chu kì, cấu hình electron lớp
ngoài cùng có lặp lại không? Điều này dẫn
đến sự biến đổi như thế nào về tính chất
của các nguyên tố?
+ Trả lời câu hỏi ?1,2 sgk trang 35.
-GV yêu cầu HS quan sát hình ảnh, bảng
và đề nghị nêu nhận xét, giải thích xu
hướng biến đổi bán kính nguyên tử, độ âm
điện trong một chu kì, trong một nhóm:
+ Electron chuyển động hỗn loạn xung
quanh hạt nhân, vậy làm thế nào để xác
định được bán kính của một nguyên tử?
+ Nhận xét xu hướng biến đổi bán kính
tăng dần hay giảm dần trong một chu kì,
trong một nhóm A.
+ Giải thích nguyên nhân xu hướng biến
đổi bán kính dựa vào lực hút tĩnh điện giữa
hạt nhân, các electron và số lớp electron.
electron lớp ngoài cùng là nguyên nhân
sự biến đổi tuần hoàn về tính chất các
nguyên tố.
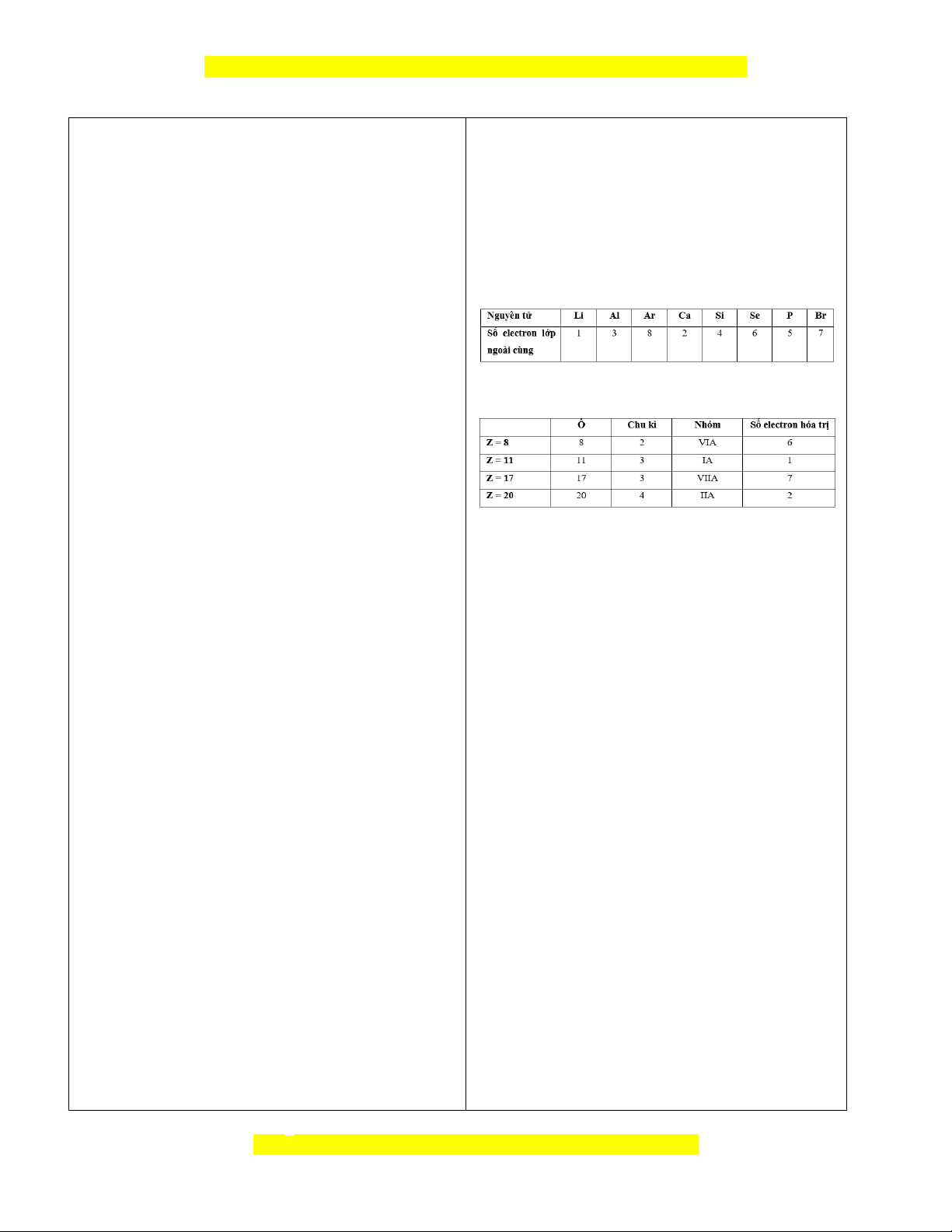
-Trả lời câu hỏi ?1 sgk trang 35:
-Trả lời câu hỏi ?2 sgk trang 35:
II. Bán kính nguyên tử
- Một cách gần đúng, bán kính nguyên tử
được xác định bằng một nửa khoảng cách
trung bình giữa hai hạt nhân trong chất
rắn đơn chất hoặc trong phân tử hai
nguyên tử giống nhau.
- Trong một chu kì, bán kính nguyên tử
giảm dần theo chiều tăng dần của điện
tích hạt nhân. Do trong một chu kì điện
tích hạt nhân tăng, số lớp electron không
đổi nên lực hút giữa hạt nhân với các
electron lớp ngoài cùng cũng tăng theo.
- Trong một nhóm A, bán kính nguyên tử
tăng dần theo chiều tăng dần của điện
tích hạt nhân. Do trong một nhóm A,
theo chiều từ trên xuống dưới số lớp
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
+ Trả lời câu hỏi ?3 sgk trang 36
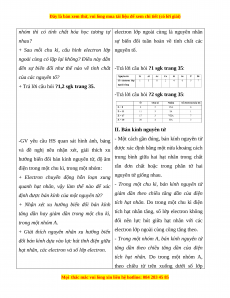
+ Độ âm điện là gì?
+ Xu hướng biến đổi giá trị độ âm điện
trong một chu kì, trong một nhóm A tăng
dần hay giảm dần theo điện tích hạt nhân.
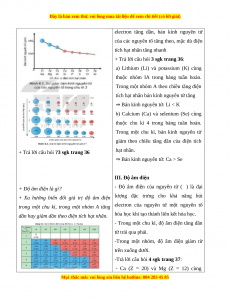
electron tăng dần, bán kính nguyên tử
của các nguyên tố tăng theo, mặc dù điện
tích hạt nhân tăng nhanh
+ Trả lời câu hỏi 3 sgk trang 36:
a) Lithium (Li) và potassium (K) cùng
thuộc nhóm IA trong bảng tuần hoàn.
Trong một nhóm A theo chiều tăng điện
tích hạt nhân bán kính nguyên tử tăng
⇒ Bán kính nguyên tử: Li < K
b) Calcium (Ca) và selenium (Se) cùng
thuộc chu kì 4 trong bảng tuần hoàn.
Trong một chu kì, bán kính nguyên tử
giảm theo chiều tăng dần của điện tích
hạt nhân.
⇒ Bán kính nguyên tử: Ca > Se
III. Độ âm điện
- Độ âm điện của nguyên tử (ꭓ) là đại
lượng đặc trưng cho khả năng hút
electron của nguyên tử một nguyên tố
hóa học khi tạo thành liên kết hóa học.
- Trong một chu kì, độ âm điện tăng dần
từ trái qua phải.
-Trong một nhóm, độ âm điện giảm từ
trên xuống dưới.
-Trả lời câu hỏi 4 sgk trang 37:
- Ca (Z = 20) và Mg (Z = 12) cùng
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85