Bài 11. LIÊN KẾT ION Mục tiêu
- Trình bày được khái niệm và sự hình thành liên kết
ion (nêu một số ví dụ điển hình tuân theo quy tắc octet).
- Nêu được cấu tạo tinh thể NaCl. Giải thích được vì
sao các hợp chất ion thường ở trạng thái rắn trong
điều kiện thường (dạng tinh thể ion).
- Lắp được mô hình tinh thể NaCl (theo mô hình có sẵn). Cấu trúc I. Sự tạo thành ion
II. Sự tạo thành liên kết ion III. Tinh thể ion
? Hợp chất NaCl nóng chảy ở nhiệt độ cao và
có khả năng dẫn điện khi nóng chảy hoặc khi
hoà tan trong dung dịch. Yếu tố nào trong
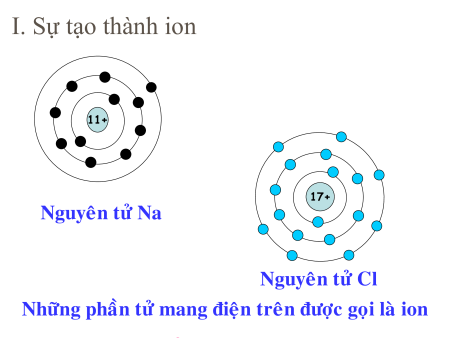
phân tử NaCl gây ra các tính chất trên? I. Sự tạo thành ion
PHIEÁU HOÏC TAÄP SOÁ 1:
• Cho: Na (Z = 11); Cl ( Z = 17)
* Cho bieát soá haït p, e.
• * Caùc nguyeân töû coù trung hoøa ñieän khoâng?
• * Vieát caáu hình electron cuûa nguyeân töû.
• * Neáu nguyeân töû Na nhöôøng 1e ôû lôùp ngoøai
cuøng. Haõy tính ñieän tích phaàn coøn laïi.
• * Neáu nguyeân töû Cl thu theâm 1e vaøo lôùp
ngoaøi cuøng. Haõy tính ñieän tích phaàn coøn laïi. I. Sự tạo thành ion * Na (Z = 11) * Cl (Z = 17) -Nguyên tử Na có 11p, -Nguyên tử Na có 17p, 11e → trung hoà về 17e → trung hoà về điện. điện. - Cấu hình electron - Cấu hình electron 1s22s22p63s1 1s22s22p63s23p5 - Nguyên tử Na - Nguyên tử Cl nhường nhường 1 electron 1 electron Na –nhường e→ Na+ Cl –nhận e→ Cl-
Giáo án Powerpoint Bài 11 Hóa học 10 Kết nối tri thức: Liên kết ion
115
58 lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Bộ bài giảng điện tử Hóa học 10 Kết nối tri thức được cập nhật đủ cả năm.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Bộ bài giảng powerpoint Hóa học 10 Kết nối tri thức bao gồm đầy đủ các bài giảng trong cả năm học. Bộ bài giảng được thiết kế theo phong cách hiện đại, đẹp mắt, trình bày chi tiết cho từng phần học và bám sát chương trình Sách giáo khoa Hóa học 10 bộ Kết nối tri thức.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(115 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)