Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t (c ế ó l i ờ gi i ả ) Bài 12: Liên k t
ế hydrogen và tư ng t ơ ác van der waals I. Liên k t ế hydrogen 1. Khái ni m ệ - Liên k t ế hydrogen là m t ộ lo i ạ liên k t ế y u ế đư c ợ hình thành gi a ữ nguyên tử H (đã liên k t ế v i ớ m t
ộ nguyên tử có độ âm đi n ệ l n) ớ v i ớ m t
ộ nguyên tử khác (có độ âm điện l n ớ ) còn c p
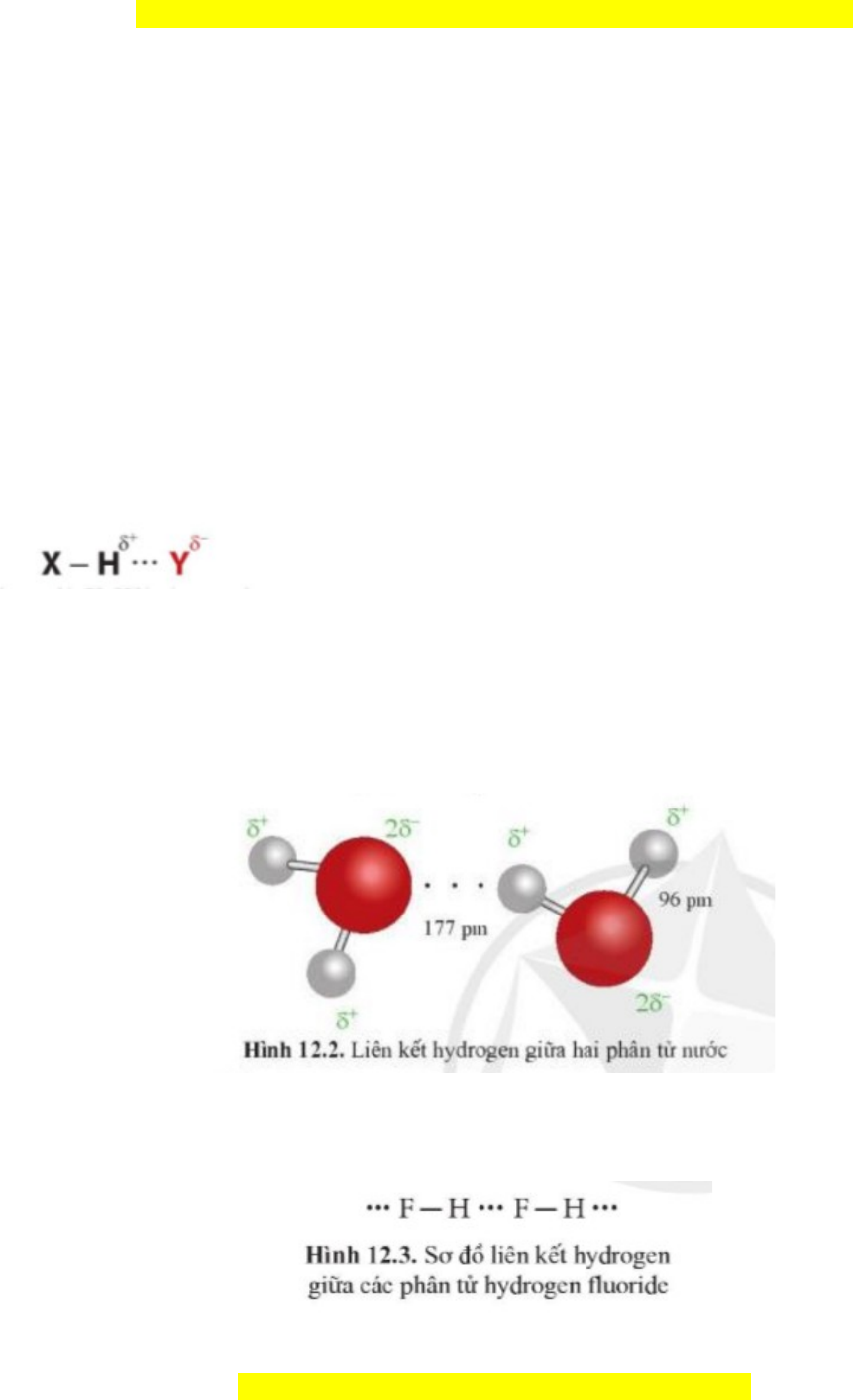
ặ electron riêng. Các nguyên tử có độ âm đi n ệ l n ớ thư ng ờ g p ặ trong liên k t ế hydrogen là N, O, F. - Liên k t ế hydrogen thư ng ờ đư c kí ợ hi u l ệ à d u ba ch ấ m ấ (…), r i ả đ u t ề nguyên t ừ H ử đ n nguyên ế t t ử o l ạ iên k t ế hydrogen v i ớ nó.
(Trong đó, X, Y là các nguyên t N ử , O, F) - Liên k t ế hydrogen có b n ả ch t ấ tĩnh đi n. ệ Tư ng ơ tác hút tĩnh đi n ệ gi a ữ H+ và Y- thể hiện b n ả ch t ấ c a ủ liên k t ế hydrogen. Ví d 1 ụ : Liên k t ế hydrogen đư c t ợ o ạ ra gi a ữ hai phân t n ử ư c. ớ Ví dụ 2: Ở nhi t ệ độ th p, ấ hydrogen fluoride (HF) t n ồ t i ạ ở thể r n ắ dư i ớ d ng ạ polimer (HF)n nhờ liên k t ế hydrogen. 2. Ảnh hư ng c ở a l ủ iên k t ế hydrogen t i ớ tính ch t ấ v t ậ lí c a n ủ ư c ớ M i ọ thắc m c
ắ vui lòng xin vui lòng: 084 283 45 85
Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t (c ế ó l i ờ gi i ả ) a) Đặc đi m ể t p h ậ p ợ Nhờ liên k t ế hydrogen, các phân t ử nư c ớ có th ể t p ậ h p ợ v i ớ nhau, ngay c ả ở th ể h i ơ , thành m t ộ c m ụ phân t . ử Kích thư c ớ các c m ụ phân t ử này thay đ i ổ tùy theo đi u ề ki n ệ nhiệt đ , áp s ộ uất. b) Nhi t ệ đ nóng ch ộ y và nh ả i t ệ đ s ộ ôi T i ạ áp su t ấ 1 bar, nư c ớ có nhi t ệ độ nóng ch y ả và nhi t ệ độ sôi tư ng ơ ng ứ là 0oC và (xấp x ) ỉ 100oC, cao h n ơ so v i ớ nhi u ề ch t ấ có kh i ố lư ng ợ phân t ử l n ớ h n ơ nư c. ớ Tính
chất này là do các phân tử nư c ớ liên k t ế khá ch t ặ chẽ v i ớ nhau b i ở các liên k t ế hydrogen. II. Tư ng t ơ ác van der Waals 1. Khái ni m ệ M i ọ thắc m c
ắ vui lòng xin vui lòng: 084 283 45 85
Lý thuyết Liên kết hydrogen và tương tác Van Der Waals Hóa 10 Cánh diều
680
340 lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Tài liệu được cập nhật liên tục trong gói này từ nay đến hết tháng 6/2023. Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Tailieugiaovien.com.vn giới thiệu Bộ câu hỏi lý thuyết Hóa học lớp 10 mới nhất nhằm giúp Giáo viên có thêm tài liệu tham khảo Lý thuyết môn Hóa học lớp 10.
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(680 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN Hóa Học
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Lớp 10
Xem thêmTài liệu bộ mới nhất
Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có l i gi i)ả ử ệ ể ế ờ ả
Bài 12: Liên k t hydrogen và t ng tác van der waalsế ươ
I. Liên k t hydrogenế
1. Khái ni mệ
- Liên k t hydrogen là m t lo i liên k t y u đ c hình thành gi a nguyên t H (đãế ộ ạ ế ế ượ ữ ử
liên k t v i m t nguyên t có đ âm đi n l n) v i m t nguyên t khác (có đ âmế ớ ộ ử ộ ệ ớ ớ ộ ử ộ
đi n l n) còn c p electron riêng. Các nguyên t có đ âm đi n l n th ng g p trongệ ớ ặ ử ộ ệ ớ ườ ặ
liên k t hydrogen là N, O, F.ế
- Liên k t hydrogen th ng đ c kí hi u là d u ba ch m (…), r i đ u t nguyên t Hế ườ ượ ệ ấ ấ ả ề ừ ử
đ n nguyên t t o liên k t hydrogen v i nó.ế ử ạ ế ớ
(Trong đó, X, Y là các nguyên t N, O, F)ử
- Liên k t hydrogen có b n ch t tĩnh đi n. T ng tác hút tĩnh đi n gi a Hế ả ấ ệ ươ ệ ữ
+
và Y
-
thể
hi n b n ch t c a liên k t hydrogen.ệ ả ấ ủ ế
Ví d 1:ụ Liên k t hydrogen đ c t o ra gi a hai phân t n c.ế ượ ạ ữ ử ướ
Ví d 2:ụ nhi t đ th p, hydrogen fluoride (HF) t n t i th r n d i d ngỞ ệ ộ ấ ồ ạ ở ể ắ ướ ạ
polimer (HF)
n
nh liên k t hydrogen.ờ ế
2. nh h ng c a liên k t hydrogen t i tính ch t v t lí c a n cẢ ưở ủ ế ớ ấ ậ ủ ướ
M i th c m c vui lòng xin vui lòng: 084 283 45 85ọ ắ ắ
Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có l i gi i)ả ử ệ ể ế ờ ả
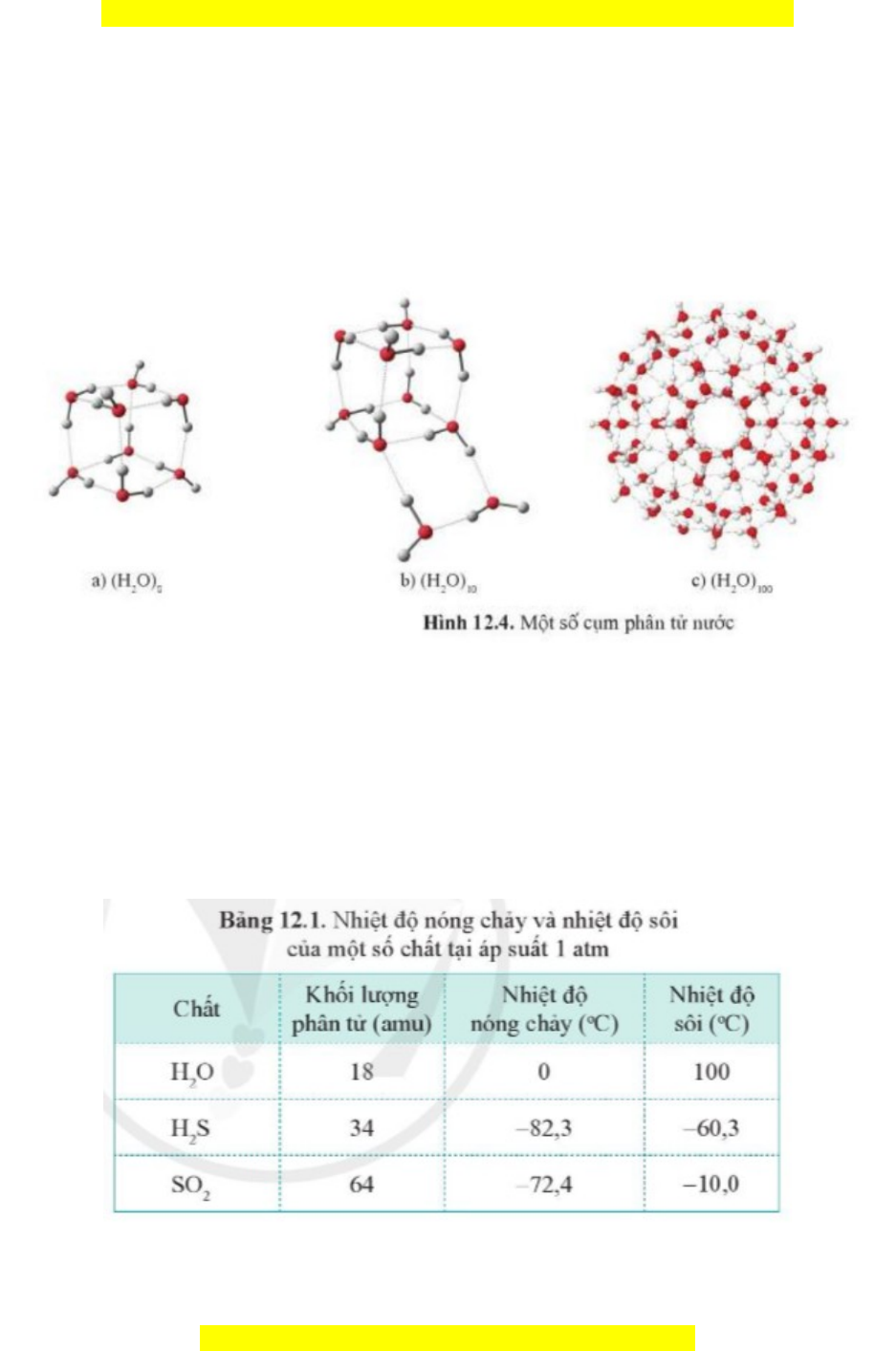
a) Đ c đi m t p h pặ ể ậ ợ
Nh liên k t hydrogen, các phân t n c có th t p h p v i nhau, ngay c th h i,ờ ế ử ướ ể ậ ợ ớ ả ở ể ơ
thành m t c m phân t . Kích th c các c m phân t này thay đ i tùy theo đi u ki nộ ụ ử ướ ụ ử ổ ề ệ
nhi t đ , áp su t.ệ ộ ấ
b) Nhi t đ nóng ch y và nhi t đ sôiệ ộ ả ệ ộ
T i áp su t 1 bar, n c có nhi t đ nóng ch y và nhi t đ sôi t ng ng là 0ạ ấ ướ ệ ộ ả ệ ộ ươ ứ
o
C và
(x p x ) 100ấ ỉ
o
C, cao h n so v i nhi u ch t có kh i l ng phân t l n h n n c. Tínhơ ớ ề ấ ố ượ ử ớ ơ ướ
ch t này là do các phân t n c liên k t khá ch t ch v i nhau b i các liên k tấ ử ướ ế ặ ẽ ớ ở ế
hydrogen.
II. T ng tác van der Waalsươ
1. Khái ni mệ
M i th c m c vui lòng xin vui lòng: 084 283 45 85ọ ắ ắ















