CHƯƠNG 3. HỢP CHẤT CHỨA NITROGEN
Phần A. BÀI TẬP THEO CHỦ ĐỀ CHỦ ĐỀ 1. AMINE * HỆ THỐNG LÝ THUYẾT
I. Khái niệm, phân loại, đồng phân, danh pháp 1. Khái niệm
- Amine là dẫn xuất của ammonia, trong đó nguyên tử hydrogen trong phân tử ammonia được thay
thế bằng gốc hydrocarbon.
VD: CH3NH2, C6H5NH2, CH3 – NH – CH3, (CH3)3N, … 2. Phân loại Theo bậc amine
Theo bản chất gốc hydrocarbon
- Bậc amine = số gốc hydrocarbon - Được phân thành nhiều loại trong đó có hai loại điển
(R) liên kết trực tiếp với nguyên tử hình: nitrogen.
♦ Alkylamine: Nhóm amine liên kết với gốc alkyl.
♦ Amine bậc một: R – NH2
Công thức: CnH2n+3N (n ≥ 1).
♦ Amine bậc hai: R – NH – R’
VD: C2H5NH2, CH3 – NH – CH3, … R N R'
♦ Arylamine (amine thơm): Nhóm amine liên kết trực ♦ Amine bậc ba: |
tiếp với nguyên tử carbon của vòng benzene. R'
VD: C6H5-NH2 (C6H5-: phenyl), … 3. Đồng phân
- Amine từ 2C trở lên có thể có các đồng phân: bậc amine, mạch carbon, vị trí nhóm amine.
- Khi viết đồng phân amine thì viết theo từng bậc, số đồng phân alkylamine: 2n-1 (n < 5). 4. Danh pháp
♦ Tên gốc chức = tên gốc hydrocabon + amine (viết liền). ♦ Tên thay thế
+ Tên amine bậc một = tên hydrocarbon (bỏ e) + vị trí nhóm amine + amine
+ Tên amine bậc hai = N – tên gốc hydrocarbon + tên gốc hydrocarbon mạch chính + vị trí nhóm amine + amine
+ Tên amine bậc ba = N – tên gốc HC thứ nhất – N – tên gốc HC thứ hai + tên gốc hydrocarbon
mạch chính + vị trí nhóm amine + amine (nếu gốc giống nhau thì dùng tiền tố di (2), tri (3), …)
♦ Tên thông thường: VD: C6H5NH2: aniline. Amine Tên gốc – chức Tên thay thế CH3NH2 methylamine methanamine CH3CH2NH2 ethylamine Ethanamine CH3CH2CH2NH2 propylamine Propan – 1 – amine CH3 – CH(NH2) – CH3 isopropylamine Propan – 2 – amine CH3 – NH – CH3 dimethylamine N – methylmethanamine (CH3)3N trimethylamine N, N – dimethylmethanamine
II. Đặc điểm cấu tạo Methylamine(CH3NH2) Aniline (C6H5NH2) Cấu trúc phân tử Mô hình phân tử
- Trong phân tử amine, nguyên tử nitrogen còn cặp electron chưa liên kết tương tự ammonia
Amine có một số tính chất hóa học tương tự ammonia, riêng aniline còn dễ tham gia phản ứng thế
nguyên tử hydrogen trong nhân thơm do ảnh hưởng của nhóm -NH2.
III. Tính chất vật lí
- Ở điều kiện thường, CH3NH2, C2H5NH2, CH3 – NH – CH3, (CH3)3N là những chất khí có mùi tanh
của cá hoặc mùi khai; các amin có phân tử khối lớn hơn là chất lỏng hoặc rắn.
- Các amine có số carbon nhỏ thường tan tốt trong nước do tạo được liên kết hydrogen với nước, độ
tan giảm khi số nguyên tử carbon trong gốc hydrocarbon tăng.
- Amine có nhiệt độ sôi cao hơn so với hydrocarbon có cùng số nguyên tử carbon.
Thứ tự giảm nhiệt độ sôi: Hợp chất ion > carboxylic acid > alcohol > amine > ester > hydrocarbon
- Ở điều kiện thường, aniline là chất lỏng, ít tan trong nước.
IV. Tính chất hóa học
1. Tính base và phản ứng tạo phức (a) Tính base
- Tương tự ammonia, các amine thể hiện tính base yếu: RNH2 + H2O RNH3+ + OH-
- Tính base: aniline < NH3 < alkylamine.
- Thí nghiệm thể hiện tính base của amine: Đĩa thủy tinh Ống nghiệm (1) Ống nghiệm (2) Lấy 2 mL dung dịch
Bước 1 Đặt vào mẩu giấy quỳ tím. CH Lấy khoảng 1 mL dung 3NH2 và nhỏ thêm vài giọt phenolphthalein. dịch FeCl3. Nhỏ vài giọt dung dịch Nhỏ từ từ khoảng 3 mL Bước 2 CH Nhỏ từ từ 2 mL dung 3NH2 vào mẩu giấy quỳ dung dịch CH3NH2 vào, tím. dịch HCl vào, lắc đều. lắc đều. Hiện tượng Quỳ tím chuyển màu xanh. Dung dịch từ màu hồng chuyển thành mất màu.
Xuất hiện kết tủa nâu đỏ.
♦ Đổi màu chất chỉ thị: Alkylamine đổi màu quỳ tím → xanh, phenolphthalein → hồng, aniline
không làm đổi màu quỳ tím và phenolphthalein vì là base yếu hơn.
♦ Tác dụng với acid → muối ammonium TQ: RNH2 + HCl → RNH3Cl CH3NH2 + HCl → CH3NH3Cl C6H5NH2 + HCl → C6H5NH3Cl
♦ Tác dụng với dung dịch muối → Muối ammonium + base mới (kết tủa)
TQ: 3RNH2 + 3H2O + FeCl3 → 3RNH3Cl + Fe(OH)3↓nâu đỏ
3CH3NH2 + 3H2O + FeCl3 → CH3NH3Cl + Fe(OH)3↓nâu đỏ
(b) Khả năng tạo phức
♦ Thí nghiệm tạo phức của methylamine:
- Bước 1: Cho khoảng 2 mL dung dịch CuSO4 0,1 M vào ống nghiệm.
- Bước 2: Thêm từ từ dung dịch methylamine 0,1 M vào ống nghiệm, lắc đều.
- Hiện tượng: Xuất hiện kết tủa xanh lam sau đó kết tủa tan hết.
- Các amine như methylamine, ethylamine có khả năng hòa tan Cu(OH)2 tạo dung dịch phức chất có
màu xanh lam. PTHH: 4CH3NH2 + Cu(OH)2 → [Cu(CH3NH2)4](OH)2 2
2. Phản ứng với nitrous acid (tính khử)
- Alkylamine bậc một tác dụng với nitrous acid ở nhiệt độ thường tạo alcohol và giải phóng N2.
TQ: RNH2 + HNO2 → ROH + N2↑ + H2O PƯ dùng để nhận biết amine bậc một. (HONO)
- Aniline tác dụng với nitrous acid ở nhiệt độ thấp (0 – 5 oC) tạo thành muối diazonium (thường
dùng để tổng hợp phẩm nhuộm azo và dược phẩm). PTHH: C 6H5NH2 + HNO2 + HCl o 0 5 C [C6H5N2]+Cl-
3. Phản ứng của aniline với nước bromine
♦ Thí nghiệm phản ứng của aniline với nước bromine.
- Bước 1: Cho khoảng 1mL nước bromine vào ống nghiệm
- Bước 2: Thêm từ từ vài giọt dung dịch aniline loãng vào ống nghiệm.
- Hiện tượng: Dung dịch bromine bị mất màu đồng thời xuất hiện kết tủa trắng.
- Tương tự phenol, aniline giam gia phản ứng thế nguyên tử H trong vòng benzene dễ hơn benzene
do có nhóm -NH2 đẩy e vào vòng benzene. Phản ứng thế ưu tiên ở các vị trí ortho và para.
V. Ứng dụng và điều chế 1. Ứng dụng
- Aniline là nguyên liệu quan trọng để tổng hợp phẩm nhuộm (phẩm màu azo), dược phẩm (paracetamol) hay polymer.
- Một số diamine dùng làm nguyên liệu tổng hợp polymer. VD: hexamethylenediamine (H2N –
(CH2)6 – NH2) được sử dụng để tổng hợp nylon-6,6. 2. Điều chế ♦ Alkyl hóa ammonia
- Alkylamine được điều chế từ ammonia và dẫn xuất halogen, tùy tỉ lệ mol các chất tham gia phản
ứng có thể tạo được amine bậc một, bậc hai hoặc bậc ba. CH3Br CH3Br CH3Br
NH CH NH CH - NH -CH (CH ) N 3 HBr 3 2 HBr 3 3 HBr 3 3
♦ Khử hợp chất nitro
- Aniline và các arylamine thường được điều chế bằng cách khử hợp chất nitro (-NO2) tương ứng bởi
một số kim loại (Zn, Fe, …) trong dung dịch HCl. C FeHCl 6H5NO2 + 6[H] C o t 6H5NH2 + 2H2O ❖ BÀI TẬP TỰ LUẬN
Câu 1. [CD -SGK] Cho các chất có công thức cấu tạo sau: H C 3 NH CH 2 O 2 NH2 H C 3 CH2 NH2 H C 3 NH2 (1) (2) (3) (4)
Trong các chất trên, hãy cho biết: (a) Chất nào là amine.
(b) Chất nào thuộc loại arylamine. 3 Hướng dẫn giải
(a) Chất là amine: (1), (2), (4).
(b) Chất nào thuộc loại arylamine: (2)
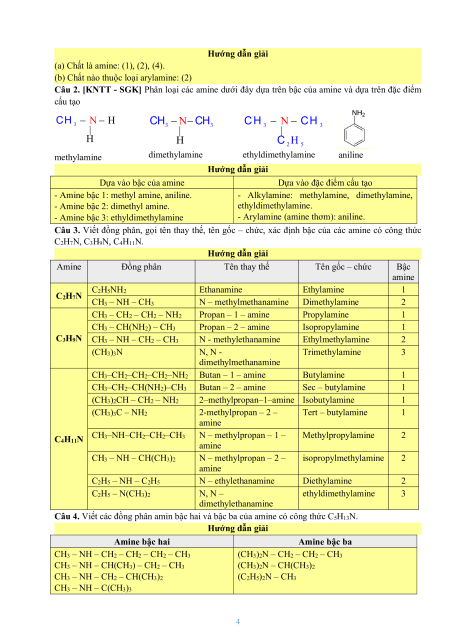
Câu 2. [KNTT - SGK] Phân loại các amine dưới đây dựa trên bậc của amine và dựa trên đặc điểm cấu tạo CH N H H C N CH N 3 CH CH | 3 3 | 3 3 | H H C H 2 5 methylamine dimethylamine ethyldimethylamine aniline Hướng dẫn giải Dựa vào bậc của amine
Dựa vào đặc điểm cấu tạo
- Amine bậc 1: methyl amine, aniline.
- Alkylamine: methylamine, dimethylamine,
- Amine bậc 2: dimethyl amine. ethyldimethylamine.
- Amine bậc 3: ethyldimethylamine
- Arylamine (amine thơm): aniline.
Câu 3. Viết đồng phân, gọi tên thay thế, tên gốc – chức, xác định bậc của các amine có công thức C2H7N, C3H9N, C4H11N. Hướng dẫn giải Amine Đồng phân Tên thay thế Tên gốc – chức Bậc amine C2H7N C2H5NH2 Ethanamine Ethylamine 1 CH3 – NH – CH3 N – methylmethanamine Dimethylamine 2 CH3 – CH2 – CH2 – NH2 Propan – 1 – amine Propylamine 1 CH3 – CH(NH2) – CH3 Propan – 2 – amine Isopropylamine 1
C3H9N CH3 – NH – CH2 – CH3 N - methylethanamine Ethylmethylamine 2 (CH3)3N N, N - Trimethylamine 3 dimethylmethanamine
CH3–CH2–CH2–CH2–NH2 Butan – 1 – amine Butylamine 1 CH3–CH2–CH(NH2)–CH3 Butan – 2 – amine Sec – butylamine 1 (CH3)2CH – CH2 – NH2
2–methylpropan–1–amine Isobutylamine 1 (CH3)3C – NH2 2-methylpropan – 2 – Tert – butylamine 1 amine C CH3–NH–CH2–CH2–CH3 N – methylpropan – 1 – Methylpropylamine 2 4H11N amine CH3 – NH – CH(CH3)2 N – methylpropan – 2 – isopropylmethylamine 2 amine C2H5 – NH – C2H5 N – ethylethanamine Diethylamine 2 C2H5 – N(CH3)2 N, N – ethyldimethylamine 3 dimethylethanamine
Câu 4. Viết các đồng phân amin bậc hai và bậc ba của amine có công thức C5H13N. Hướng dẫn giải Amine bậc hai Amine bậc ba
CH3 – NH – CH2 – CH2 – CH2 – CH3
(CH3)2N – CH2 – CH2 – CH3
CH3 – NH – CH(CH3) – CH2 – CH3 (CH3)2N – CH(CH3)2
CH3 – NH – CH2 – CH(CH3)2 (C2H5)2N – CH3 CH3 – NH – C(CH3)3 4
Chuyên đề dạy thêm Chương 3: Hợp chất chứa Nitrogen Hóa học 12 (sách mới)
1.6 K
814 lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Tailieugiaovien.com.vn giới thiệu Chuyên đề dạy thêm Hóa học lớp 12 dành cho cả 3 sách mới nhằm giúp Giáo viên có thêm tài liệu tham khảo tài liệu môn Hóa học 12.
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(1628 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)