Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t (c ế ó đáp án) S G Ở IÁO D C Ụ VÀ ĐÀO TẠO HẢI KỲ THI TH C Ử H N Ọ H C Ọ SINH GI I Ỏ D N ƯƠ G LỚP 10 THPT, NĂM H C Ọ 2022 - 2023
CỤM CÁC TRƯỜNG THPT Môn thi: Hóa h c ọ Th i
ờ gian làm bài: 180 phút, không k t ể h i ờ gian giao Đ C Ề HÍNH TH C Ứ đề
(Đề thi có 05 câu, 02 trang)
- Cho biết kh i ố lư n
ợ g nguyên t (t ử heo amu) c a
ủ các nguyên t : ố
H = 1; Mg = 24; C = 12; O = 16; N = 14; Na = 23; Si = 28; P = 31; S = 32; Cl = 35,5; K = 39; Ca = 40;
Al = 27 ; Cr = 52; Mn = 55; Fe = 56; Cu = 64; Zn = 65; Br = 80; Ag = 108; I = 127; Ba = 137; Hg = 201. - Cho biết s h ố i u ệ nguyên t c ử a ủ m t ộ s n ố guyên t :
ố 1H; 6C; 7N; 8O; 9F; 10Ne; 11Na;
12Mg; 13Al; 14Si; 15P; 16S; 17Cl; 18Ar; 19K; 20Ca. Câu I: (2 đi m) ể 1. H p c ợ hất X có công th c ứ phân t ử AxByDz trong đó: - B và D là 2 nguyên t ố thu c ộ 2 nhóm A k ế ti p ế và 2 chu kì k ế ti p ế trong b n ả g tu n ầ hoàn, ZD < ZB - T ng ổ s nguyê ố n tử là 6. - Nguyên tử D có s h ố ạt proton bằng s h ố ạt neutron. - T ng ổ s h ố ạt c b ơ ản trong phân t X ử là 150, trong đó h t ạ mang đi n ệ nhi u h ề n h ơ t ạ không mang đi n l ệ à 50. - % khối lư ng
ợ nguyên tố D trong X là 64%. a) Xác đ nh c ị ác nguyên t
ố A, B, D và công thức c a ủ X. b) So sánh tính chất c a ủ nguyên t D ố v i ớ nguyên t pho ố sphorus, nguyên t s ố ulfur.
2. Xerium – 137 là m t ộ đ ng ồ v t ị hư ng c ờ ó trong lò ph n ả ng h ứ t
ạ nhân. Chu kì bán rã c a ủ
137Ce là 30,2 năm, 137Ce là m t ộ trong các đ ng v ồ b ị ị phát tán m nh nhi ạ u vùng t ề i ạ Châu Âu sau tai
nạn hạt nhân trecnobun. Sau bao lâu, chất đ c ộ này còn l i ạ 1,0% k t ể l ừ úc x y ra ả tai n n? ạ Câu II: (2 đi m) ể
1. Viết công thức Lewis, xác đ nh t ị
rạng thái lai hóa của nguyên tử trung tâm và d ng hì ạ nh h c ọ c a ủ các phân t và ử
ion sau: HCHO, HCO -3, H2S, NF3. 2. Giải thích hi n t ệ ư ng s ợ au:
a) Khi hòa tan phân bón ure vào trong c c ố nư c ớ , thì th y c ấ c ố nư c ớ l nh d ạ n. ầ b) Khi thực hi n nung đá ệ
vôi trong các lò vôi, ngư i ờ ta thư ng s ờ p x ắ p xe ế n k đá ẽ vôi (CaCO3) v i ớ than hoặc củi? c) Phân t N
ử H3 có thể liên kết v i ớ nhau tạo thành c m ụ phân t (N ử H3)n. d) C2H5OH có nhiệt đ s ộ ôi cao h n C ơ 2H6? Câu III: (2 đi m) ể
1. Cân bằng các phư ng t ơ rình phản ng s ứ au theo phư ng ơ pháp thăng b ng e ằ lectron.
a) NaI + H2SO4 (đặc, nóng) H2S + I2 + Na2SO4 + H2O
b) FeSO4 + NaNO3 + NaHSO4
Fe2(SO4)3 + NO + Na2SO4 + H2O 0 t c) HCHO + AgNO 3 + NH3 + H2O (NH4)2CO3 + Ag + NH4NO3 d) KClO4 + HCl Cl2 + KCl + H2O M i
ọ thắc mắc vui lòng xin liên h h
ệ otline: 084 283 45 85
Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t (c ế ó đáp án) 2. Cho hình v m
ẽ ô tả quá trình đi u c ề h dung d ế c
ị h X trong phòng thí nghiệm:
a) Hãy cho biết dung dịch X thu đư c ợ trong ng ố nghi m ệ 2 là dung d c ị h gì? b) Trong điều ki n ệ thích h p, dung d ợ c ị h X trong ng nghi ố m ệ 2 có th ph ể n ả ng đ ứ ư c ợ v i ớ nh ng ữ chất nào trong s c
ố ác chất sau: K2MnO4, Fe3O4, NaHCO3, Cu, MgO, dung d c ị h AgNO3, dung d c
ị h Ba(NO3)2? Viết phư ng t ơ rình ph n ả ng x ứ ảy ra (n u c ế ó). khí HCl (1) Boâ ng H2SO4 ñaëc (2) NaCl X H2O Câu IV: (2 đi m) ể
1. Cho trình phản ng hóa ứ h c
ọ : 2NaHCO3 (s) → Na2CO3 (s) + CO2(g) + H2O (g) Chất NaHCO3 (s) Na2CO3 (s) CO2 (g) H2O (g) 0 S298 (J/mol·K) 101,7 135,0 213,8 188,7 0 H f 298 (kJ/mol) -950,8 -1130,7 -393,5 -241,8 0 0 0 a) Hãy tính H S G 298 ; 298 , 298 c a ủ phản ng? ứ 25 Ở 0C Phản ng c ứ ó tự xảy ra không? b) Tính lư ng ợ C2H5OH cần đ c ể ung cấp lư ng nhi ợ t ệ cho phản ng đi ứ u c ề h 2,479 l ế ít khí CO2 (đkc) t ở rên. Bi t ế : Chất C2H5OH (l) CO2 (g) O2 (g) H2O (g) 0 H f 298 (kJ/mol) -277,6 -393,5 0 -241,6 2. Để hòa tan h t ế m t ộ mẫu k m ẽ trong dung d c ị h HCl 20 ở
0C cần 6 phút. Cũng mẫu k m ẽ đó tan trong dung d c ị h axit nói trên 30 ở 0C trong 3 phút. H i ỏ đ hòa ể tan h t ế mẫu k m ẽ đó trong dung d c ị h axit nói trên 80 ở 0C cần th i ờ gian bao lâu? Câu V: (2 đi m) ể 1. Tr n ộ đ u 30,96 ga ề m h n h ỗ p ợ b t ộ X g m
ồ MgCO3 và kim loại R có hóa trị không đ i ổ rồi
chia làm 2 phần bằng nhau. - Đ t
ố nóng phần 1 trong không khí, sau khi các ph n ả ng ứ x y ra ả hoàn toàn thu đư c ợ 15 gam h n ỗ h p c ợ ác oxide kim loại. - Hòa tan h t ế phần 2 bằng dung d c ị h HNO3 loãng, d , ư sau phản ng t ứ hu đư c ợ được dung d c ị h A và 7,9328 lít h n h ỗ p khí ợ B g m
ồ 2 khí, trong đó có khí NO (đkc). a) Xác đ nh ki ị m loại R và t kh ỉ ối c a ủ B so v i ớ H2.
b) Nếu hòa tan hoàn toàn lư ng X ợ trên vào dung d c ị h HCl d , ư cô c n dung d ạ c ị h sau ph n ả ng ứ thu đư c
ợ bao nhiêu gam chất rắn khan. 2. Đun nóng h n h ỗ p X ợ g m ồ b t ộ Fe và S trong đi u ki ề n kh ệ
ông có không khí, thu được h n ỗ M i
ọ thắc mắc vui lòng xin liên h h
ệ otline: 084 283 45 85
Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t (c ế ó đáp án) h p ợ rắn A. Cho A tác d ng ụ v i ớ một lư ng d ợ dung d ư c ị h HCl thu được s n ph ả ẩm khí Y có t kh ỉ i ố so v i
ớ H2 là 13. Lấy 2,479 lít (đo ở đi u ki ề n ệ chuẩn) khí Y đem đ t ố cháy r i ồ cho toàn b s ộ ản phẩm
cháy đó đi qua 100 ml dung d c
ị h H2O2 5,1% (có khối lư ng
ợ riêng bằng 1gam/mL), sau phản ng ứ thu được dung d c ị h B. Các phản ng x ứ ảy ra hoàn toàn. a) Tính thành phần % kh i ố lư ng c ợ ác chất trong h n ỗ h p ợ X. b) Xác đ nh ị n ng đ ồ
ộ % các chất trong dung d c ị h B. -------------H T Ế ------------- CÂU ĐÁP ÁN ĐI M Ể G i ọ số hạt mang đi n ệ trong h p ợ ch t ấ X là 2Z, h t ạ không mang đi n ệ là N - Tổng số hạt c ơ bản trong phân t ử X là : 2Z + N = 150 (1) - Hạt mang đi n ệ nhi u ề h n ơ h t ạ không mang đi n ệ là 50 2Z – N = 50 (2)
Từ (1) và (2): có Z = 50; ⇒ ZA.x + ZB.y + ZD. z = 50 (3) N = 50 = NAx + NBy + NDz
Có: MX = Z + N = 100 = MA.x + MB.y + MD.z 0,25 - Trong phân t ử X, nguyên t ố D chi m ế 64%
MD .z = 64 ⇒ MD = 64 : z (64 ⋮ z) I. 1 Do trong X có 6 nguyên t ử nên ta có: x + y + z = 6 1,5 ⇒ 1 ≤ x, y, z ≤ 4;
điểm Mặt khác trong D có s ố h t ạ p = s ố h t ạ N Z 1 2 4 MD 64 32 16 Z 0,25 D 32 16 8 TH1: Nguyên t
ử D có: z = 1; Z = 32 ⇒ D là nguyên t ố selenum Từ (*) có ZA.x + ZB.y = 18 x + y = 5 ZB < 3, 6
Mặt khác B và D là 2 nguyên t ố thu c ộ 2 chu kì, 2 nhóm k ế ti p ế có Z 0,25 B > ZD loại TH2: Nguyên t
ử D có: z = 2; Z = 16 ⇒ D là nguyên t ố sulfur Từ (*) có ZA.x + ZB.y = 18 x + y = 4 0,25 ZB ≤ 6
Mặt khác B và D là 2 nguyên t ố thu c ộ 2 chu kì, 2 nhóm k ế ti p ế có ZB > ZD = 8 loại TH3: Nguyên t
ử D có: z = 4; Z = 8 ⇒ D là nguyên t ố oxygen Từ (*) có ZA.x + ZB.y = 18 x + y = 2 ⇒ x = y = 1 M i
ọ thắc mắc vui lòng xin liên h h
ệ otline: 084 283 45 85
Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t (c ế ó đáp án)
ZA + ZB = 18 (4) ZA < ZB ≤ 17 0,25
Mặt khác B và D là 2 nguyên t ố thu c ộ 2 chu kì, 2 nhóm k ế ti p ế
* ZB - ZD = 7 ZB = 9 + 7 = 15
Từ (4) ⇒ ZA = 3 ⇒ không th a ỏ mãn * Z 0,25 B - ZD = 9 ZB = 8 + 9 = 17 ⇒ ZA = 1 ⇒ Th a ỏ mãn Vậy CT X c n ầ tìm là HClO4 b) So sánh tính ch t: ấ ZD = 8: 1s22s22p4 ZS = 16: 1s22s22p63s23p4 ZP = 15: 1s22s22p63s23p3 - Phosphorus, sulfur thu c ộ cùng chu kì theo chi u ề tăng d n ầ đi n ệ tích h t ạ
nhân, tính phi kim tăng nên tính phi kim c a ủ P < S - D, S thu c ộ cùng nhóm theo chi u ề tăng d n ầ đi n ệ tích h t ạ nhân, tính phi kim giảm nên tính phi kim c a ủ S < O P < S < O I. 2 G i ọ khối lư ng ợ ban đ u ầ c a ủ Ce – 137 là m 0,5 - Sau th i ờ gian t thì kh i ố lư ng ợ 137Ce còn l i ạ 0,1% so v i ớ ban đ u: ầ m0 = 0,25 điểm 1,0%m t - Áp d ng ụ CT: m T o = m. 2 t 0,01m = m. 30,2 2 0,25 t = 200,26 năm.
Vậy sau 200,26 năm thì lư ng ợ ch t ấ Ce – 137 còn l i ạ 1% CT Lewis lai Dạng hình Vsepr hóa h c ọ HCHO sp2 Tam giác AX3 phẳng M i ỗ II.1 chất 1,0 sp2 Gấp khúc AX2E 0,25 điểm NO -2 0 0 1 1 0 0 O N O O N O H2S sp3 Gấp khúc AX2E2 NF3 sp3 Chóp tam AX3E giác
a. Khi hòa tan phân bón ure vào trong c c ố nư c ớ , thì th y ấ c c ố nư c ớ l nh ạ d n ầ 0,25 là vì khi tan vào nư c ớ ure đã h p ấ th ụ nhi t ệ t ừ môi trư ng ờ xung quanh hay M i
ọ thắc mắc vui lòng xin liên h h
ệ otline: 084 283 45 85
Đề HSG Hóa 10 Sở Hải Dương năm 2023 có đáp án
2.1 K
1 K lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Tài liệu được cập nhật liên tục trong gói này từ nay đến hết tháng 3/2024. Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Tailieugiaovien.com.vn giới thiệu Đề HSG Hóa 10 Sở Hải Dương năm 2023 có đáp án.
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(2077 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN Hóa Học
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Lớp 10
Xem thêmTài liệu bộ mới nhất

Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có đáp án)ả ử ệ ể ế
S GIỞ ÁO D C VỤ À ĐÀO T O Ạ H IẢ
D NGƯƠ
C M CÁC TR NG THPTỤ ƯỜ
Đ CHÍNH TH CỀ Ứ
KỲ THI TH CH N H CỬ Ọ Ọ SINH GI I Ỏ
L P 10 THPTỚ , NĂM H C 2022 - 2023Ọ
Môn thi: Hóa h cọ
Th i gian làm bài: 180 phút, không k th i gian giaoờ ể ờ
đề
(Đ thi có 05 câu, 0ề 2 trang)
- Cho bi t kh i l ng nguyên t (theo amu) c a các nguyên t :ế ố ượ ử ủ ố
H = 1; Mg = 24; C = 12; O = 16; N = 14; Na = 23; Si = 28; P = 31; S = 32; Cl = 35,5; K = 39; Ca = 40;
Al = 27 ; Cr = 52; Mn = 55; Fe = 56; Cu = 64; Zn = 65; Br = 80; Ag = 108; I = 127; Ba = 137; Hg = 201.
- Cho bi t s hi u nguyên t c a m t s nguyên t :ế ố ệ ử ủ ộ ố ố
1
H; 6C; 7N; 8O; 9F; 10Ne; 11Na;
12Mg; 13Al; 14Si; 15P; 16S; 17Cl; 18Ar; 19K; 20Ca.
Câu I: (2 đi m)ể
1. H p ch t X có công th c phân t Aợ ấ ứ ử
x
B
y
D
z
trong đó:
- B và D là 2 nguyên t thu c 2 nhóm A k ti p và 2 chu kì k ti p trong b ng tu n hoàn, Zố ộ ế ế ế ế ả ầ
D
<
Z
B
- T ng s nguyên t là 6.ổ ố ử
- Nguyên t D có s h t proton b ng s h t neutron.ử ố ạ ằ ố ạ
- T ng s h t c b n trong phân t X là 150, trong đó h t mang đi n nhi u h n h t không ổ ố ạ ơ ả ử ạ ệ ề ơ ạ
mang đi n là 50.ệ
- % kh i l ng nguyên t D trong X là 64%.ố ượ ố
a) Xác đ nh các nguyên t A, B, D và công th c c a X.ị ố ứ ủ
b) So sánh tính ch t c a nguyên t D v i nguyên t phosphorus, nguyên t sulfur.ấ ủ ố ớ ố ố
2. Xerium – 137 là m t đ ng v th ng có trong lò ph n ng h t nhân. Chu kì bán rã c a ộ ồ ị ườ ả ứ ạ ủ
137
Ce là 30,2 năm,
137
Ce là m t trong các đ ng v b phát tán m nh nhi u vùng t i Châu Âu sau tai ộ ồ ị ị ạ ề ạ
n n h t nhân trecnobun. Sau bao lâu, ch t đ c này còn l i 1,0% k t lúc x y ra tai n n?ạ ạ ấ ộ ạ ể ừ ả ạ
Câu II: (2 đi m)ể
1. Vi t công th c Lewis, xác đ nh tr ng thái lai hóa c a nguyên t trung tâm và d ng hình ế ứ ị ạ ủ ử ạ
h c c a các phân t và ion sau: HCHO, HCOọ ủ ử
3
-
, H
2
S
,
NF
3
.
2. Gi i thích hi n t ng sau:ả ệ ượ
a) Khi hòa tan phân bón ure vào trong c c n c, thì th y c c n c l nh d n.ố ướ ấ ố ướ ạ ầ
b) Khi th c hi n nung đá vôi trong các lò vôi, ng i ta th ng s p x p xen k đá vôi ự ệ ườ ườ ắ ế ẽ
(CaCO
3
) v i than ho c c i?ớ ặ ủ
c) Phân t NHử
3
có th liên k t v i nhau t o thành c m phân t (NHể ế ớ ạ ụ ử
3
)
n
.
d) C
2
H
5
OH có nhi t đ sôi cao h n Cệ ộ ơ
2
H
6
?
Câu III: (2 đi m)ể
1. Cân b ng các ph ng trình ph n ng sau theo ph ng pháp thăng b ng electron.ằ ươ ả ứ ươ ằ
a) NaI + H
2
SO
4 (đ c, nóng)ặ
H
2
S + I
2
+ Na
2
SO
4
+ H
2
O
b) FeSO
4
+ NaNO
3
+ NaHSO
4
Fe
2
(SO
4
)
3
+ NO + Na
2
SO
4
+ H
2
O
c) HCHO + AgNO
3
+ NH
3
+ H
2
O
0
t
(NH
4
)
2
CO
3
+ Ag + NH
4
NO
3
d) KClO
4
+ HCl
Cl
2
+ KCl + H
2
O
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ
Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có đáp án)ả ử ệ ể ế
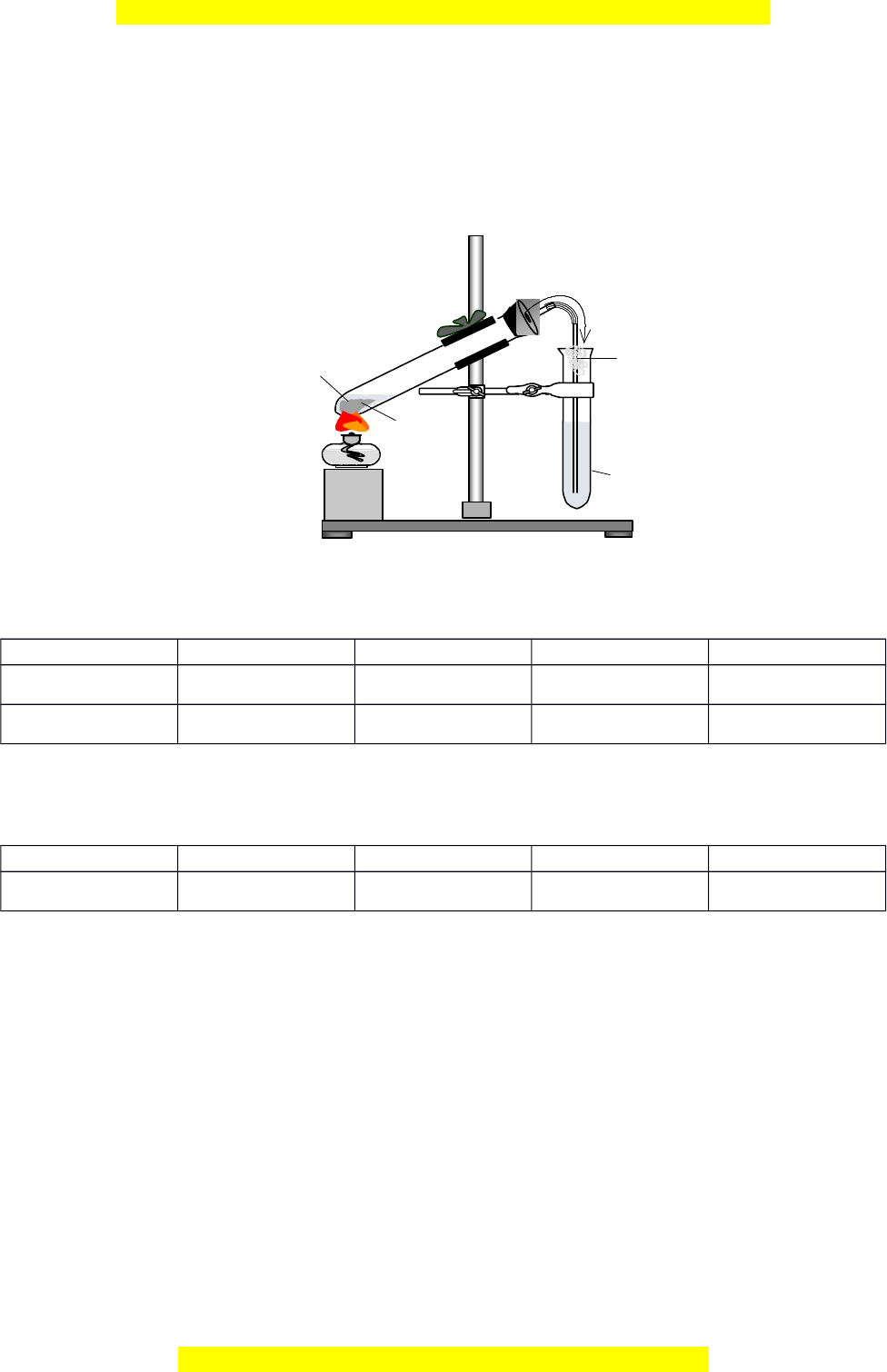
2. Cho hình v mô t quá trình đi u ch dung d ch X trong phòng thí nghi m:ẽ ả ề ế ị ệ
a) Hãy cho bi t dung d ch X thu đ c trong ng nghi m 2 là dung d ch gì?ế ị ượ ố ệ ị
b) Trong đi u ki n thích h p, dung d ch X trong ng nghi m 2 có th ph n ng đ c v i ề ệ ợ ị ố ệ ể ả ứ ượ ớ
nh ng ch t nào trong s các ch t sau: Kữ ấ ố ấ
2
MnO
4
, Fe
3
O
4
, NaHCO
3
, Cu, MgO, dung d ch AgNOị
3
, dung
d ch Ba(NOị
3
)
2
? Vi t ph ng trình ph n ng x y ra (n u có).ế ươ ả ứ ả ế
H
2
SO
4
ñaëc
NaCl
Boâng
HCl
(1)
(2)
H
2
O
khí
Câu IV: (2 đi m)ể
1. Cho trình ph n ng hóa h c: 2NaHCOả ứ ọ
3
(s) → Na
2
CO
3
(s) + CO
2
(g) + H
2
O (g)
Ch tấ NaHCO
3
(s) Na
2
CO
3
(s) CO
2
(g) H
2
O (g)
0
298
S
(J/mol·K)
101,7 135,0 213,8 188,7
0
f 298
H
(kJ/mol)
-950,8 -1130,7 -393,5 -241,8
a) Hãy tính
0
298
H
;
0
298
S
,
0
298
G
c a ph n ng? 25ủ ả ứ Ở
0
C Ph n ng có t x y ra không?ả ứ ự ả
b) Tính l ng Cượ
2
H
5
OH c n đ cung c p l ng nhi t cho ph n ng đi u ch 2,479 lít khí ầ ể ấ ượ ệ ả ứ ề ế
CO
2
(đkc) trên. Bi t: ở ế
Ch tấ C
2
H
5
OH (l) CO
2
(g) O
2
(g) H
2
O (g)
0
f 298
H
(kJ/mol)
-277,6 -393,5 0 -241,6
2. Đ hòa tan h t m t m u k m trong dung d ch HCl 20ể ế ộ ẫ ẽ ị ở
0
C c n 6 phút. Cũngầ m u k m đó ẫ ẽ
tan trong dung d ch axit nói trên 30ị ở
0
C trong 3 phút. H i đ hòa tan h t m u k m đó trong dung ỏ ể ế ẫ ẽ
d ch axit nói trên 80ị ở
0
C c n th i gian bao lâu?ầ ờ
Câu V: (2 đi m)ể
1. Tr n đ u 30,96 gam h n h p b t X g m MgCOộ ề ỗ ợ ộ ồ
3
và kim lo i R có hóa tr không đ i r i ạ ị ổ ồ
chia làm 2 ph n b ng nhau.ầ ằ
- Đ t nóng ph n 1 trong không khí, sau khi các ph n ng x y ra hoàn toàn thu đ c 15 gam ố ầ ả ứ ả ượ
h n h p các oxide kim lo i.ỗ ợ ạ
- Hòa tan h t ph n 2 b ng dung d ch HNOế ầ ằ ị
3
loãng, d , sau ph n ng thu đ c đ c dung ư ả ứ ượ ượ
d ch A và 7,9328 lít h n h p khí B g m 2 khí, trong đó có khí NO (đkc).ị ỗ ợ ồ
a) Xác đ nh kim lo i R và t kh i c a B so v i Hị ạ ỉ ố ủ ớ
2
.
b) N u hòa tan hoàn toàn l ng X trên vào dung d ch HCl d , cô c n dung d ch sau ph n ế ượ ị ư ạ ị ả
ng thu đ c bao nhiêu gam ch t r n khan.ứ ượ ấ ắ
2. Đun nóng h n h p X g m b t Fe và S trong đi u ki n khỗ ợ ồ ộ ề ệ ông có không khí, thu đ c h n ượ ỗ
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ
X

Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có đáp án)ả ử ệ ể ế
h p r n A. Cho A tác d ng v i m t l ng d dung d ch HCl thu đ c s n ph m khí Y cợ ắ ụ ớ ộ ượ ư ị ượ ả ẩ ó t kh i so ỉ ố
v i Hớ
2
là 13. L y 2,4ấ 79 lít (đo đi u ki nở ề ệ chu n) khí Y đem đ t cháy r i cho toàn b s n ph m ẩ ố ồ ộ ả ẩ
cháy đó đi qua 100 ml dung d ch Hị
2
O
2
5,1% (có kh i l ng riêng b ng 1gố ượ ằ am/mL), sau ph n ng thu ả ứ
đ c dung d ch B. Các ph n ng x y ra hoànượ ị ả ứ ả toàn.
a) Tính thành ph n % kh i l ng các ch t trong h n h pầ ố ượ ấ ỗ ợ X.
b) Xác đ nh n ng đ % các ch t trong dung d chị ồ ộ ấ ị B.
-------------H T-------------Ế
CÂU ĐÁP ÁN ĐI MỂ
I. 1
1,5
đi mể
G i s h t mang đi n trong h p ch t X là 2Z, h t không mang đi n là Nọ ố ạ ệ ợ ấ ạ ệ
- T ng s h t c b n trong phân t X là : 2Z + N = 150 (1)ổ ố ạ ơ ả ử
- H t mang đi n nhi u h n h t không mang đi n là 50ạ ệ ề ơ ạ ệ
2Z – N = 50 (2)
T (1) và (2): có Z = 50; ừ ⇒ Z
A
.x + Z
B
.y + Z
D
. z = 50 (3)
N = 50 = N
A
x + N
B
y + N
D
z
Có: M
X
= Z + N = 100 = M
A
.x + M
B
.y
+ M
D
.z
- Trong phân t X, nguyên t D chi m 64% ử ố ế
M
D
.z = 64 ⇒ M
D
= 64 : z (64 ⋮ z)
Do trong X có 6 nguyên t nên ta có: x + y + z = 6ử
⇒ 1 ≤ x, y, z ≤ 4;
M t khác trong D có s h t p = s h t Nặ ố ạ ố ạ
Z 1 2 4
M
D
64 32 16
Z
D
32 16 8
TH1: Nguyên t D có: z = 1; Z = 32 ử ⇒ D là nguyên t selenumố
T (*) có Zừ
A
.x + Z
B
.y = 18
x + y = 5
Z
B
< 3, 6
M t khác B và D là 2 nguyên t thu c 2 chu kì, 2 nhóm k ti p có Zặ ố ộ ế ế
B
> Z
D
lo iạ
TH2: Nguyên t D có: z = 2; Z = 16 ử ⇒ D là nguyên t sulfurố
T (*) có Zừ
A
.x + Z
B
.y = 18
x + y = 4
Z
B
≤ 6
M t khác B và D là 2 nguyên t thu c 2 chu kì, 2 nhóm k ti p có Zặ ố ộ ế ế
B
> Z
D
=
8
lo iạ
TH3: Nguyên t D có: z = 4; Z = 8 ử ⇒ D là nguyên t oxygenố
T (*) có Zừ
A
.x + Z
B
.y = 18
x + y = 2 ⇒ x = y = 1
0,25
0,25
0,25
0,25
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ

Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có đáp án)ả ử ệ ể ế
Z
A
+ Z
B
= 18 (4)
Z
A
< Z
B
≤ 17
M t khác B và D là 2 nguyên t thu c 2 chu kì, 2 nhóm k ti pặ ố ộ ế ế
* Z
B
- Z
D
= 7
Z
B
= 9 + 7 = 15
T (4) ừ ⇒ Z
A
= 3 ⇒ không th a mãnỏ
* Z
B
- Z
D
= 9
Z
B
= 8 + 9 = 17
⇒ Z
A
= 1 ⇒ Th a mãnỏ
V y CT X c n tìm là HClOậ ầ
4
b) So sánh tính ch t:ấ
Z
D
= 8: 1s
2
2s
2
2p
4
Z
S
= 16: 1s
2
2s
2
2p
6
3s
2
3p
4
Z
P
= 15: 1s
2
2s
2
2p
6
3s
2
3p
3
- Phosphorus, sulfur thu c cùng chu kì theo chi u tăng d n đi n tích h t ộ ề ầ ệ ạ
nhân, tính phi kim tăng nên tính phi kim c a P < S ủ
- D, S thu c cùng nhóm theo chi u tăng d n đi n tích h t nhân, tính phi kimộ ề ầ ệ ạ
gi m nên tính phi kim c a S < O ả ủ
P < S < O
0,25
0,25
I. 2
0,5
đi mể
G i kh i l ng ban đ u c a Ce – 137 là mọ ố ượ ầ ủ
- Sau th i gian t thì kh i l ng ờ ố ượ
137
Ce còn l i 0,1% so v i ban đ u: mạ ớ ầ
0
=
1,0%m
- Áp d ng CT: mụ
o
= m.
2
t
T
0,01m = m.
30,2
2
t
t = 200,26 năm.
V y sau 200,26 năm thì l ng ch t Ce – 137 còn l i 1%ậ ượ ấ ạ
0,25
0,25
II.1
1,0
đi mể
CT Lewis lai
hóa
D ng hình ạ
h cọ
Vsepr
HCHO sp
2
Tam giác
ph ngẳ
AX
3
NO
2
-
N
OO
1
0
0
N
OO
1
00
sp
2
G p khúcấ AX
2
E
H
2
S sp
3
G p khúcấ AX
2
E
2
NF
3
sp
3
Chóp tam
giác
AX
3
E
M i ỗ
ch t ấ
0,25
a. Khi hòa tan phân bón ure vào trong c c n c, thì th y c c n c l nh d nố ướ ấ ố ướ ạ ầ
là vì khi tan vào n c ure đã h p th nhi t t môi tr ng xung quanh hay ướ ấ ụ ệ ừ ườ
0,25
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ

Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có đáp án)ả ử ệ ể ế
II. 2
1,0
đi mể
thu nhi tệ
b. Khi th c hi n nung đá vôi trong các lò vôi, ng i ta th ng s p x p xen ự ệ ườ ườ ắ ế
k đá vôi (CaCOẽ
3
) v i than ho c c i: Ph n ng phân h y CaCOớ ặ ủ ả ứ ủ
3
là ph n ả
ng thu nhi t, c n l ng nhi t t các ch t cháy nh than, c i. Khi th c ứ ệ ầ ượ ệ ừ ấ ư ủ ự
hi n đ t các ch t than ho c c i là ph n ng t a nhi t.ệ ố ấ ặ ủ ả ứ ỏ ệ
- S p x p xen k đ CaCOắ ế ẽ ể
3
ti p xúc đ u v i nhi t, tránh tình tr ng bên ế ề ớ ệ ạ
d i l ng nhi t đ c cung c p nhi u gây cháy vôi, bên trên l ng nhi t ướ ượ ệ ượ ấ ề ượ ệ
ít gây tình tr ng s ng vôi ( ph n ng nhi t phân ch a hoàn toàn)ạ ố ả ứ ệ ư
c. Phân t NHử
3
có th liên k t v i nhau t o thành c m phân t (NHể ế ớ ạ ụ ử
3
)
n
vì:
Nguyên t N có 5e hóa tr , s d ng 3e đ t o liên k t v i 3 nguyên t H, ử ị ử ụ ể ạ ế ớ ử
v n còn 1 c p e ch a s d ng. Vì v y các phân t NHẫ ặ ư ử ụ ậ ử
3
có th liên k t v i ể ế ớ
nhau t o c m phân t (NHạ ụ ử
3
)
n
d. C
2
H
5
OH có nhi t đ sôi cao h n Cệ ộ ơ
2
H
6
vì C
2
H
5
OH có liên k t hydrogen ế
còn C
2
H
6
không có liên k t hydrogen và Cế
2
H
5
OH có phân t kh i l n h n ử ố ớ ơ
C
2
H
6
0,25
0,25
0,25
Câu
III. 1
1,0
đi mể
a) NaI + H
2
SO
4
H
2
S + I
2
+ Na
2
SO
4
+ H
2
O
0
2
6 2
2 2
8
I I e
S e S
4
1
x
x
8NaI + 5H
2
SO
4
H
2
S + 4I
2
+ 4Na
2
SO
4
+ 4H
2
O
b) FeSO
4
+ NaNO
3
+ NaHSO
4
Fe
2
(SO
4
)
3
+ NO + Na
2
SO
4
+ H
2
O
2 3
5 2
2 2 2
3
Fe Fe e
N e N
3
2
x
x
6FeSO
4
+ 2NaNO
3
+ NaHSO
4
3Fe
2
(SO
4
)
3
+ 2NO + Na
2
SO
4
+ H
2
O
K t h p đ i s :ế ợ ạ ố
6FeSO
4
+ 2NaNO
3
+ aNaHSO
4
3Fe
2
(SO
4
)
3
+ 2NO + bNa
2
SO
4
+ cH
2
O
BTNT Na: 2 + a = 2b
SO
4
: 6 + a = 9 + b
H: a = 2c
a = 8; b = 5; c = 4
6FeSO
4
+ 2NaNO
3
+ 8NaHSO
4
3Fe
2
(SO
4
)
3
+ 2NO + 5Na
2
SO
4
+ 4H
2
O
c) HCHO + AgNO
3
+ NH
3
+ H
2
O
0
t
(NH
4
)
2
CO
3
+ Ag + NH
4
NO
3
0 4
1 0
4
1
C C e
Ag e Ag
1
4
x
x
HCHO + 4AgNO
3
+ 6NH
3
+ 2H
2
O
0
t
(NH
4
)
2
CO
3
+ 4Ag + 2NH
4
NO
3
d) KClO
4
+ HCl
Cl
2
+ KCl + H
2
O
1 0
7 0
1
7
Cl Cl e
Cl e Cl
7
1
x
x
0,25
0,25
0,25
0,25
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ






















