Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t ế (có đáp án) SỞ GIÁO D C Ụ VÀ ĐÀO TẠO
KỲ THI HỌC SINH GIỎI TP HỒ CHÍ MINH C M Ụ CHUYÊN MÔN C M Ụ CHUYÊN MÔN IV NĂ M H C Ọ 2022- 2023
ĐỀ THI MÔN: HOÁ H C Ọ - KH I Ố 10 HƯ N Ớ G DẪN CHẤM Câu 1 (4 điểm)
1.1. Năm 1911, nhà vật lí ngư i
ờ New Zealand là E. Rutherford đã ti n
ế hành bắn phá lá vàng siêu m ng
ỏ bằng chùm hạt alpha ( kí hi u
ệ là α, đây là hạt nhân của nguyên tử helium, mang điện tích +2) lên m t ộ thì k t ế quả thu đư c ợ như sau: + Hầu h t
ế các hạt α xuyên qua lá vàng. + M t ộ số ít hạt α bị l c ệ h quỹ đạo so v i ớ ban đầu. + M t
ộ số rất ít hạt α bị bật ngư c ợ trở lại.
Hãy giải thích vì sao có 3 ki u ể đư ng
ờ đi như trên và cho bi t ế vai trò c a
ủ màn huỳnh quang trong thí nghiệm này. 1.2 a) Nguyên tử đư c
ợ tạo nên từ 3 loại hạt cơ bản, đi n
ề vào các ô còn trống trong bảng sau: hạt Đi n ệ tích tư ng ơ đối Khối lư ng ợ (amu) …………….. 0 ……………… ……………… ………………….. 0,00055 ……………… ……………… …………….. M i
ọ thắc mắc vui lòng xin liên h h
ệ otline: 084 283 45 85
Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t ế (có đáp án)
b) Dựa vào bảng trên , em hãy tính và so sánh khối lư ng
ợ nguyên tử và khối lư ng ợ hạt nhân c a
ủ nguyên1 3tử 27 Al ( theo amu), từ đó rút ra k t ế luận gì?
1.3 Vào những ngày hanh khô, cơ thể chúng ta có thể tích tụ điện tích khi đi bộ trên m t ộ số loại thảm ho c
ặ khi chải tóc . Giả sử cơ thể chúng ta tích m t ộ lư ng
ợ điện tích là -10C ( micrô culông) a) Hãy cho bi t ế trong trư ng ờ h p
ợ này , cơ thể chúng ta đã nhận thêm hay mất đi electron ? b) Tổng khối lư ng ợ c a
ủ các electron ( theo kg) mà cơ thể đã nhận thêm ( hoặc mất đi) là bao nhiêu kg? Cho bi t
ế 1 amu = 1,66.10-27 kg; điện tích của e = -1,602.10-19C ; 1 C= 10-6C Câu 1 Hướng d n ẫ Điể ch m ấ m 1.1 + Hầu h t
ế các hạt α xuyên qua lá vàng vì nguyên tử có cấu tạo rỗng 0,25đ 1,0 đ + M t ộ số ít h t ạ α bị l c ệ h qu ỹ đ o ạ so v i ớ ban đ u: ầ H t
ạ nhân nguyên 0,25đ tử có tích đi n ệ dư ng ơ nên đã đ y ẩ h t ạ α ( cũng mang đi n ệ dư ng) ơ đi l c ệ h hư ng ớ + M t
ộ số rất ít hạt α bị bật ngư c
ợ trở lại: vì phần mang điện 0,25đ tích dư ng ơ chỉ chi m ế m t ộ th ể tích rất nh ỏ trong nguyên t . ử
+ vai trò của màn huỳnh quang : Giúp phát hiện đư ng ờ đi c a ủ các 0,25đ hạt α Hạt Đi n ệ tích tư ng ơ đối Khối lư ng ợ (amu) 1.2 Neutron (n) 0 1 1,75đ 2,25 đ Electron (e) -1 0,00055 Proton +1 1 b) Khối lư ng ợ
hạt nhân= 13.1 + 14.1 = 27 ( amu) 0,5đ Khối lư ng ợ nguyên t =
ử 13.1 + 14.1 + 13.0,00055 = 27,0715 ( amu) Nhận xét : Kh i ố lư ng
ợ hạt nhân gần bằng khối lư ng ợ nguyên tử. 1.3 a) Do cơ thể tích m t ộ lư ng
ợ điện tích âm nên cơ thể đã nhận 0.75 đ thêm electron 0,25 đ b) Số lư ng ợ hạt electron ứng v i ớ lư ng ợ điện tích -10C là 0,25 đ 10.10 6 13 số h t ạ e = 6, 242.10 1, 602.1019 0,25đ Tổng khối lư ng ợ của các h t ạ electron mà c ơ th ể đã nh n ậ
thêm là 1,66.10-27 . 6,242.1013.0,00055 = 5,7.10-17 (kg) M i
ọ thắc mắc vui lòng xin liên h h
ệ otline: 084 283 45 85
Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t ế (có đáp án) Câu 2 (3,5 điểm)
A2 B . Nguyên tử 2.1.
Nguyên tố Boron (kí hiệu hóa h c
ọ là B) có hai đồng vị: 10B ( chi m ế 19%)
và khối trung bình của B bằng 10,81 a) Tính số khối A2
b) Khi có 57 nguyên tử đồng vị 10B thì có bao nhiêu nguyên tử đồng vị A2 B ?
c) Tính phần trăm khối lư ng
ợ 10B trong axit H3BO3 ( cho bi t ế nguyên tử khối c a ủ Hydrogen và oxygen lần lư t ợ là 1 và 16 ) 2.2. X, Y , R , A , B , M theo th
ứ tự là 6 nguyên tố liên ti p
ế trong bảng hệ thống tuần hoàn có tổng số đ n
ơ vị điện tích hạt nhân là 63 ( X có số đ n
ơ vị điện tích hạt nhân nhỏ nhất) a) Xác đ nh ị số đ n
ơ vị điện tích hạt nhân của X, Y , R , A , B , M b) Vi t ế cấu hình electron c a
ủ X2- , Y- , R , A+ , B2+ , M3+ . So sánh bán kính giữa X2- , Y- , B2+ , M3+ và giải thích.
2.3 Mg có khối lư ng
ợ riêng là 1,74 gam/cm3 , tính bán kính nguyên tử Mg bi t ế trong tinh thể Mg chi m
ế 74% thể tích. Xem nguyên tử Mg là những hình cầu.( cho NA = 6,022.1023) Câu 2 Hướng d n ẫ Đi m ể ch m ấ Ta có 10B chi m
ế 19% A2 B chi m ế 81% 0,25
10,81 = 0,19.10 + 0,81.A2 A2 = 11 Số nguyên tử c a ủ đồng vị 11B là 0,25 2.1 57.81% 243 1,0 đ 19% Phần trăm khối lư ng ợ c a ủ 10B : 0,5 đ 10.0,19 .100 3, 07% 3 10,8116.3 G i
ọ Z là số điện tích hạt nhân c a ủ X 0,25
Số điện tích hạt nhân c a
ủ Y, R , A , B , M lần lư t ợ là
(Z+1) ; (Z+2) ; (Z+ 3) ; (Z+4) ; (Z+5) 2.2 Theo giả thi t ế ta có: 1,0 đ
Z + Z+1 + Z+2 + Z+3 +Z+ 4 +Z+ 5 = 63 Z= 8 8X ; 9Y ; 10R ; 11A ; 12B ; 13M M i
ọ thắc mắc vui lòng xin liên h h
ệ otline: 084 283 45 85
Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t ế (có đáp án) (O) (F) (Ne) (Na) (Mg) (Al)
Các ion : X2- , Y- , B2+ , M3+ đ u
ề có cấu hình electron là : 1s22s22p6 0,25 đ
Bán kính : r X2- > r Y- > r B2+ > r M3+ 0,5 đ
Vì các ion này có cùng số l p
ớ nên bán kính phụ thu c ộ điện tích hạt
nhân, điện tích hạt nhân càng l n
ớ thì bán kính càng nhỏ
Lấy 1 mol Mg m Mg = 24 ( gam ) 0,5đ Th
ể tích tinh thể của 1 mol Mg = 13,79 ( cm3) Th ể tích c a
ủ 1 mol nguyên tử Mg : V = 13,79.0,74 =10,2046 (cm3) 0,25đ 2.3 Th ể tích c a ủ 1 nguyên tử Mg 0,5đ 10, 2046 1,5 đ V 1 nguyên tử= 1, 695.1023 (cm3) 6, 022.1023 Nguyên t
ử Mg xem như hình cầu có bán kính R: 0,25đ 4
V .R3 R = 1,59.10-8 ( cm) 3 Câu 3 (4,0 điểm): 3.1 Phân tử M đư c ợ t o ạ nên b i
ở ion X3+ và Y2-. Trong phân tử M có t ng ổ số h t ạ p,n,e là 224 h t; ạ trong đó số h t ạ mang đi n ệ nhi u ề h n ơ s ố h t ạ không mang đi n ệ là 72 h t. ạ T ng ổ s ố h t ạ trong ion X3+ ít h n ơ trong ion Y2- là 13 h t ạ . Số kh i ố c a ủ nguyên t ử Y l n ớ h n ơ s ố kh i ố c a ủ nguyên t ử X là 5 đ n ơ v .
ị Xác định số hạt từng loại của nguyên tử X , Y và tìm công th c ứ của M.
3.2 Cho nguyên tố R thu c ộ nhóm IVA trong b ng ả tu n ầ hoàn, trong h p ợ ch t ấ khí v i ớ hydrogen thì R chi m ế a% về khối lư ng ợ . Trong công th c
ứ oxide cao nhất thì R chi m ế b% về khối lư ng. ợ Bi t ế a % + 45 b% = .100% . Hãy xác đ nh ị nguyên tố R. 44 3.3 Nguyên tử c a ủ nguyên tố R ở tr ng ạ thái c ơ b n ả có t ng ổ s ố electron ở các phân l p ớ s là 7. Hãy vi t ế cấu hình electron c a ủ nguyên tử R ở tr ng ạ thái cơ b n ả và xác đ nh ị vị trí nguyên t ố R trong
bảng tuần hoàn các nguyên tố hóa h c ọ . Xác định số e đ c ộ thân c a ủ R. Câu Hướng d n ẫ Đi m ể 3 ch m ấ 3.1 Phân tử M tạo b i ở hai ion có công th c ứ là X2Y3 0,25 đ 2,0 đ
Tổng số hạt trong phân tử M: 0,25 đ
2.( 2.ZX + NX) + 3.( 2ZY + NY) = 224 (1) M i
ọ thắc mắc vui lòng xin liên h h
ệ otline: 084 283 45 85
Đề HSG Hóa 10 Sở TP Hồ Chí Minh năm 2023 có đáp án
2.1 K
1 K lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Tài liệu được cập nhật liên tục trong gói này từ nay đến hết tháng 3/2024. Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Tailieugiaovien.com.vn giới thiệu Đề HSG Hóa 10 Sở TP Hồ Chí Minh năm 2023 có đáp án.
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(2058 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN Hóa Học
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Lớp 10
Xem thêmTài liệu bộ mới nhất
Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có đáp án)ả ử ệ ể ế
SỞ
GIÁO D C VÀ ĐÀOỤ T OẠ KỲ THI H C SINHỌ GI IỎ
TP H CHÍỒ MINH C MỤ CHUYÊN MÔN
C MỤ CHUYÊN MÔN IV NĂM H CỌ 2022-2023
ĐỀ THI MÔN: HOÁ H CỌ - KH IỐ 10
H NGƯỚ D NẪ CH MẤ
Câu 1
(4
đi m)ể
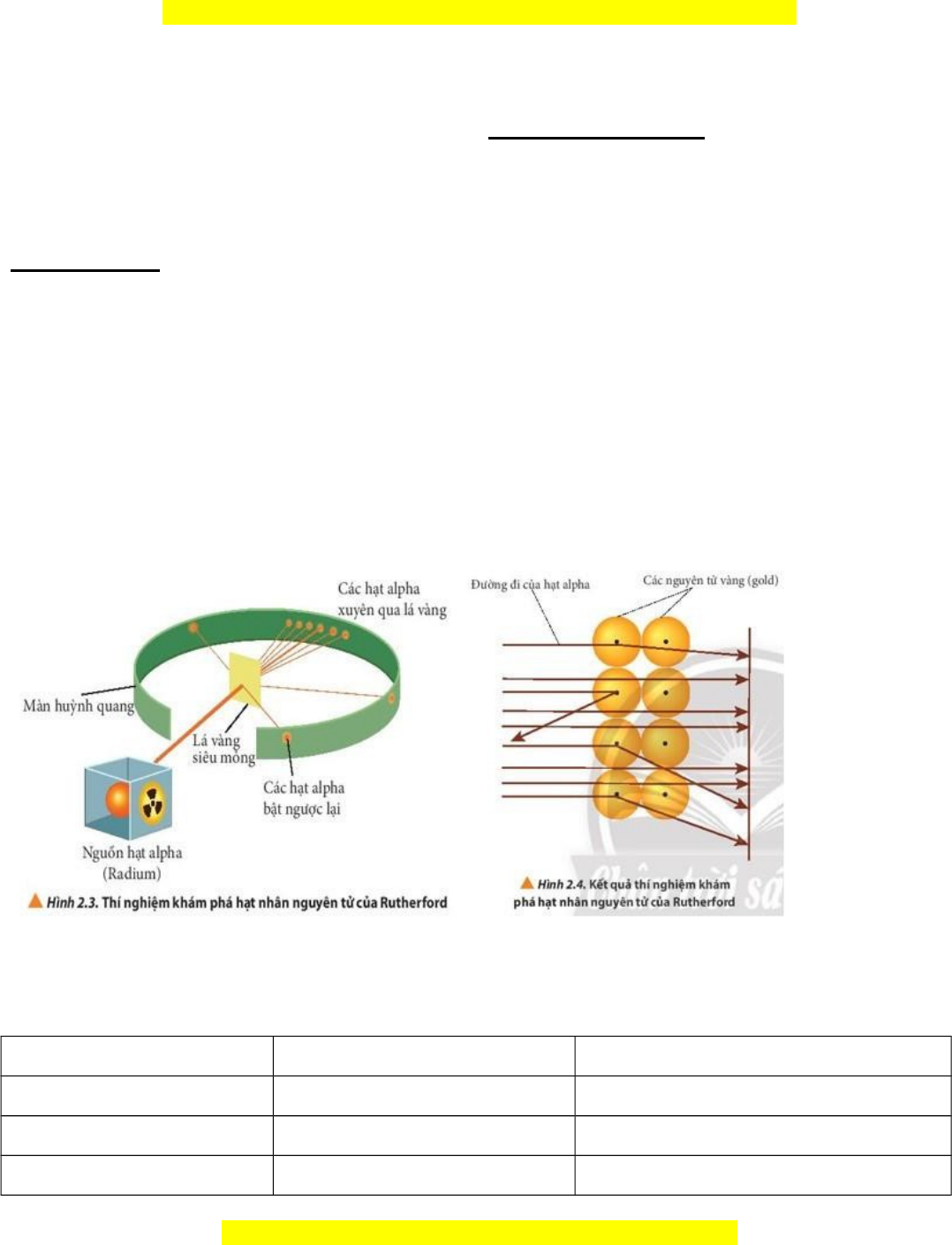
1.1. Năm 1911, nhà v tậ lí ng iườ New Zealand là E. Rutherford đã ti nế hành b nắ phá lá vàng siêu
m ng b ngỏ ằ chùm h tạ alpha ( kí hi u làệ α, đây là h tạ nhân c a nguyên tủ ử helium, mang đi nệ tích
+2) lên m t thìộ k tế qu thu đ cả ượ như sau:
+ H u h t cácầ ế h tạ α xuyên qua lá vàng.
+ M t sộ ố ít h tạ α bị l chệ quỹ đ oạ so v iớ ban đ u.ầ
+ M t sộ ố r tấ ít h tạ α bị b tậ ng cượ trở l i.ạ
Hãy gi iả thích vì sao có 3 ki uể đ ngườ đi như trên và cho bi tế vai trò c aủ màn huỳnh quang trong thí
nghi m này.ệ
1.2
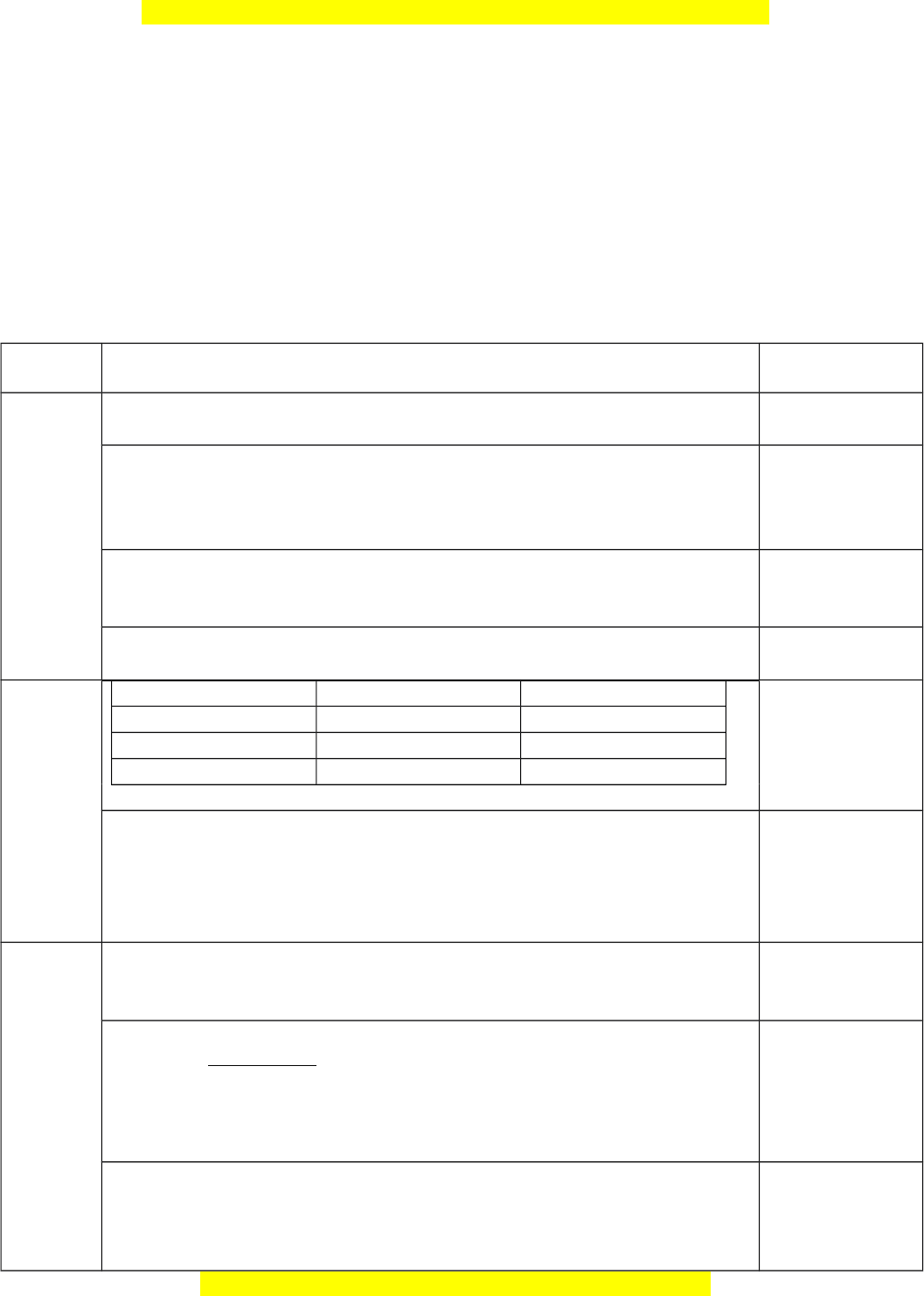
a) Nguyên tử đ c t oượ ạ nên từ 3 lo iạ h t cạ ơ b n,ả đi n vào cácề ô còn tr ngố trong b ngả sau:
h tạ Đi nệ tích t ng đ iươ ố Kh iố l ngượ (amu)
……………..
0
………………
……………… ………………….. 0,00055
……………… ……………… ……………..
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ
Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có đáp án)ả ử ệ ể ế
b) D aự vào b ngả trên , em hãy tính và so sánh kh iố l ngượ nguyên tử và kh iố l ngượ h tạ nhân
c aủ nguyên tử
27
Al ( theo amu), t đóừ rút ra k tế lu nậ gì?
1.3 Vào nh ngữ ngày hanh khô, cơ thể chúng ta có thể tích tụ đi nệ tích khi đi bộ trên m tộ số lo iạ
th mả ho cặ khi ch i tócả . Giả sử cơ thể chúng ta tích m t l ngộ ượ đi nệ tích là -10C ( micrô culông)
a) Hãy cho bi t trongế tr ngườ h p nàyợ , cơ thể chúng ta đã nh n thêmậ hay m tấ đi electron ?
b) T ngổ kh iố l ngượ c aủ các electron ( theo kg) mà cơ thể đã nh nậ thêm ( ho cặ m tấ đi) là bao
nhiêu kg? Cho bi t 1ế amu = 1,66.10
-27
kg; đi n tíchệ c aủ e = -1,602.10
-19
C ; 1 C= 10
-6
C
Câu 1 H ngướ d nẫ
ch mấ
Điể
m
1.1
1,0 đ
+ H u h tầ ế các h tạ α xuyên qua lá vàng vì nguyên tử có c uấ t o r ngạ ỗ 0,25đ
+ M t s ít h t α b l ch qu đ o so v i ban đ u: H t nhân nguyênộ ố ạ ị ệ ỹ ạ ớ ầ ạ
tử có tích đi n d ng nên đã đ y h t α ( cũng mang đi n d ng)ệ ươ ẩ ạ ệ ươ đi
l chệ h ngướ
0,25đ
+ M tộ số r tấ ít h tạ α bị b tậ ng cượ trở l i:ạ vì ph nầ mang đi nệ
tích
d ngươ ch chi mỉ ế m tộ th tíchể r tấ nh trongỏ nguyên t .ử
0,25đ
+ vai trò c aủ màn huỳnh quang : Giúp phát hi nệ đ ngườ đi c aủ các
h tạ α
0,25đ
1.2
2,25 đ
H tạ Đi nệ tích t ngươ đ iố Kh iố l ngượ (amu)
1,75đ
Neutron (n)
0 1
Electron (e) -1 0,00055
Proton +1
1
b)
Kh i l ng h t nhân=ố ượ ạ 13.1 + 14.1 = 27 ( amu)
Kh i l ng nguyên t = 13.1 + 14.1 + 13.0,00055 = 27,0715 ố ượ ử
( amu) Nh nậ xét : Kh i l ngố ượ h tạ nhân g n b ng kh iầ ằ ố l ngượ
nguyên t .ử
0,5đ
1.3
0.75 đ
a) Do cơ thể tích m tộ l ngượ đi nệ tích âm nên cơ thể đã nh nậ
thêm electron
0,25 đ
b) S l ngố ượ h tạ electron ngứ v iớ l ng đi nượ ệ tích -10C là
10.10
6
13
số h tạ e =
1, 602.10
19
6, 242.10
0,25 đ
T ng kh i l ng c a các h t electron mà c th đã nh n ổ ố ượ ủ ạ ơ ể ậ
thêm là 1,66.10
-27
. 6,242.10
13
.0,00055 = 5,7.10
-17
(kg)
0,25đ
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ
13

Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có đáp án)ả ử ệ ể ế
Câu 2
(3,5
đi m)ể
2.1. Nguyên tố Boron (kí hi uệ hóa h cọ là B) có hai đ ngồ v :ị
10
B ( chi mế 19%)
và kh i trungố bình c aủ B b ngằ 10,81
a)
Tính số kh i Aố
2
A
2
B . Nguyên tử
b) Khi có 57 nguyên t đ ngử ồ vị
10
B thì có bao nhiêu nguyên tử đ ng vồ ị
A
2
B ?
c) Tính ph nầ trăm kh iố l ngượ 10B trong axit H
3
BO
3
( cho bi tế nguyên tử kh iố c aủ Hydrogen
và
oxygen l nầ l tượ là 1 và 16 )
2.2. X, Y , R , A , B , M theo th tứ ự là 6 nguyên tố liên ti pế trong b ngả hệ th ngố tu n hoànầ có
t ngổ số đ n vơ ị đi nệ tích h tạ nhân là 63 ( X có số đ n vơ ị đi n tíchệ h t nhânạ nhỏ nh t)ấ
a) Xác đ nh sị ố đ nơ vị đi n tíchệ h t nhânạ c aủ X, Y , R , A , B , M
b) Vi tế c uấ hình electron c a Xủ
2-
, Y
-
, R , A
+
, B
2+
, M
3+
. So sánh bán kính gi aữ X
2-
, Y
-
, B
2+
, M
3+
và gi iả thích.
2.3 Mg có kh iố l ngượ riêng là 1,74 gam/cm
3
, tính bán kính nguyên tử Mg bi tế trong tinh thể Mg
chi m 74%ế thể tích. Xem nguyên tử Mg là nh ngữ hình c u.(ầ cho N
A
= 6,022.1023)
Câu 2 H ngướ d nẫ
ch mấ
Đi mể
Ta có
10
B chi mế 19%
A
2
B chi mế 81%
0,25
10,81 = 0,19.10 + 0,81.A
2
A
2
= 11
S nguyênố tử c aủ đ ngồ vị
11
B là
57.81%
243
19%
0,25
2.1
1,0 đ
Ph n trămầ kh iố l ngượ c a ủ
10
B : 0,5 đ
10.0,19
.100 3, 07%
3 10,8116.3
G iọ Z là s đi n tíchố ệ h t nhân c aạ ủ X
Số đi n tíchệ h t nhânạ c aủ Y, R , A , B , M l n l tầ ượ là
0,25
(Z+1) ; (Z+2) ; (Z+ 3) ; (Z+4) ; (Z+5)
2.2
Theo giả thi tế ta có:
1,0 đ
Z + Z+1 + Z+2 + Z+3 +Z+ 4 +Z+ 5 = 63
Z= 8
8
X ;
9
Y ;
10
R ;
11
A ;
12
B ;
13
M
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ
Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có đáp án)ả ử ệ ể ế
(O) (F) (Ne) (Na) (Mg) (Al)
Các ion : X
2-
, Y
-
, B
2+
, M
3+
đ uề có c uấ hình electron là : 1s
2
2s
2
2p
6
0,25 đ
Bán kính : r X
2-
> r Y
-
> r B
2+
> r M
3+
Vì các ion này có cùng số l pớ nên bán kính phụ thu cộ đi nệ tích h tạ
nhân, đi n tíchệ h t nhânạ càng l nớ thì bán kính càng nhỏ
0,5 đ
2.3
1,5 đ
L y 1 mol Mgấ m Mg = 24 ( gam )
Th tíchể tinh thể c aủ 1 mol Mg = 13,79 ( cm
3
)
0,5đ
Th tích c a 1 mol nguyênể ủ tử Mg : V = 13,79.0,74 =10,2046 (cm
3
) 0,25đ
Th tích c a 1 nguyênể ủ tử Mg
V 1 nguyên t =ử
10, 2046
1, 695.10
23
(cm
3
)
6, 022.10
23
0,5đ
Nguyên t Mg xemử nh hình c uư ầ có bán kính R:
V
4
.R
3
R = 1,59.10
-8
( cm)
3
0,25đ
Câu 3
(4,0
đi m):ể
3.1 Phân t M đ c t o nên b i ion Xử ượ ạ ở
3+
và Y
2-
. Trong phân t M có t ng s h t p,n,e là 224 h t;ử ổ ố ạ ạ
trong đó s h t mang đi n nhi u h n s h t không mang đi n là 72 h t. T ng s h t trong ion Xố ạ ệ ề ơ ố ạ ệ ạ ổ ố ạ
3+
ít h n trong ion Yơ
2-
là 13 h t. S kh i c a nguyên t Y l n h n s kh i c a nguyên t X là 5 đ nạ ố ố ủ ử ớ ơ ố ố ủ ử ơ
v .ị Xác đ nhị số h tạ t ng lo iừ ạ c aủ nguyên tử X , Y và tìm công th cứ c aủ M.
3.2 Cho nguyên t R thu c nhóm IVA trong b ng tu n hoàn, trong h p ch t khí v i hydrogen thì Rố ộ ả ầ ợ ấ ớ
chi mế a% về kh iố l ng.ượ Trong công th cứ oxide cao nh tấ thì R chi mế b% về kh iố l ng.ượ Bi tế a
% +
b% =
45
.100% . Hãy xác đ nhị nguyên tố R.
44
3.3 Nguyên t c a nguyên t R tr ng thái c b n có t ng s electron các phân l p s là 7. Hãyử ủ ố ở ạ ơ ả ổ ố ở ớ
vi tế c u hình electron c a nguyên t R tr ng thái c b n và xác đ nh v trí nguyên t R trongấ ủ ử ở ạ ơ ả ị ị ố
b ng tu nả ầ hoàn các nguyên tố hóa h c.ọ Xác đ nhị số e đ cộ thân c aủ R.
Câu
3
H ngướ d nẫ
ch mấ
Đi mể
3.1
2,0 đ
Phân tử M t oạ b iở hai ion có công th c là Xứ
2
Y
3 0,25 đ
T ngổ số h tạ trong phân tử M:
2.( 2.Z
X
+ N
X
) + 3.( 2Z
Y
+ N
Y
) = 224 (1)
0,25 đ
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ

Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có đáp án)ả ử ệ ể ế
Hi uệ s h tố ạ mang đi nệ và không mang đi nệ trong phân tử M: 0,25 đ
(4Z
X
+ 6Z
Y
) - ( 2N
X
+ 3N
Y
) = 72 (2)
Hi uệ s h t trongố ạ ion X
3+
và Y
2-
:
(2Z
Y
+ N
Y
+ 2) - ( 2Z
X
+ N
X
-3) = 13 (3)
0,25 đ
Hi uệ số kh iố trong nguyên tử X và Y ;
(Z
Y
+ N
Y
) – ( Z
X
+ N
X
) = 5 (4)
0,25 đ
L y (1)ấ + (2) ta đ cượ : 2Z
X
+ 3Z
Y
= 74 (5)
L y (ấ 3) - (4) ta đ cượ : Z
Y
– Z
X
= 3 (6)
Z
X
= 13 ; Z
Y
= 16
N
X
= 14 và N
Y
= 16
0,5 đ
X là Al ( Z= 13) và Y là S ( Z = 16)
Công th c M là Alứ
2
S
3
0,25 đ
3.2
1,0 đ
R thu cộ nhóm IVA nên suy ra
Công th c v i hidrogen là ứ ớ
RH
4
Công th cứ oxit cao nh tấ
là RO
2
0,25 đ
Trong h p ch t v iợ ấ ớ hidrogen:
%R a%
R
.100
R 4
Trong oxit cao nh tấ :
%R b%
R
.100
R 32
0,25 đ
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ