CHƯƠNG 6: KIM LOẠI KIỀM, KIM LOẠI KIỀM THỔ, NHÔM VÀ HỢP CHẤT CỦA CHÚNG
BÀI 12: KIM LOẠI KIỀM THỔ VÀ HỢP CHẤT QUAN TRỌNG CỦA KIM LOẠI KIỀM THỔ Mục tiêu Kiến thức
+ Biết được vị trí của kim loại kiềm thổ trong bảng tuần hoàn và cấu hình electron nguyên tử.
+ Nêu được tính chất vật lí chung của kim loại kiềm thổ và một số hợp chất quan trọng.
+ Trình bày được tính chất hóa học của kim loại kiềm thổ và một số hợp chất quan trọng của kim loại kiềm thổ.
+ Chỉ ra được một số ứng dụng các hợp chất quan trọng của kim loại kiềm thổ.
+ Trình bày được thế nào là nước cứng, tác hại của nước cứng và cách làm mềm nước cứng. Kĩ năng
+ Viết được cấu hình electron của nguyên tử kim loại kiềm thổ và ion tương ứng.
+ Xác định đúng sản phẩm các phản ứng của kim loại kiềm thổ và một số hợp chất của quan trọng.
+ Giải được các bài toán từ đơn giản đến phức tạp liên quan đến kim loại kiềm thổ và một số hợp
chất quan trọng của kim loại kiềm thổ.
+ Giải được các bài tập xác định loại nước cứng và cách làm mềm nước cứng.
+ Vận dụng kiến thức để giải quyết các bài toán thực tế.
I. LÍ THUYẾT TRỌNG TÂM
A. KIM LOẠI KIỀM THỔ 1. Cấu hình electron
Cấu hình electron: [Khí hiếm] .
Nguyên tử kim loại kiềm thổ dễ mất hai electron ở lớp ngoài cùng tạo thành ion có điện tích 2+.
Cấu hình electron của ion kim loại kiềm thổ là cấu hình electron của khí hiếm gần nhất đứng trước nó.
Ví dụ: Cấu hình electron của Mg( ):
2. Vị trí trong bảng tuần hoàn
Vị trí nguyên tố trong bảng tuần hoàn:
Số thứ tự = số hiệu nguyên tử. Chu kì = số lớp electron.
Nhóm IIA (vì có 2 electron lớp ngoài cùng).
Ví dụ: Cấu hình electron của nguyên tử Mg:
Nguyên tố Mg thuộc ô thứ 12, chu kì 3, nhóm IIA.
3. Tính chất vật lí
Các kim loại kiềm thổ có màu trắng bạc, có thể dát mỏng.
Nhiệt độ nóng chảy và nhiệt độ sôi tương đối thấp (nhưng cao hơn kim loại kiềm).
Khối lượng riêng tương đối nhỏ, độ cứng tương đối thấp.
Chú ý: Tính chất vật lí của kim loại kiềm thổ thay đổi không theo quy luật vì chúng có mạng tinh thể khác nhau
4. Tính chất hóa học
Kim loại kiềm thổ có tính khử mạnh và tính khử tăng dần từ Be đến Ba:
Trong hợp chất kim loại kiềm thổ chỉ có số oxi hóa +2.
Tính khử của kim loại kiềm thổ thể hiện qua các phản ứng với phi kim, axit, nước,...
Chú ý: Ở nhiệt độ thường, Be không tác dụng với nước, Mg phản ứng chậm.
B. MỘT SỐ HỢP CHẤT QUAN TRỌNG CỦA KIM LOẠI KIỀM THỔ 1. Canxi hiđroxit:
Là chất rắn màu trắng, ít tan trong nước. Tên gọi khác: vôi tôi Dung dịch
gọi là dung dịch nước vôi trong.
có đầy đủ tính chất của một bazơ.
Được dùng trong công nghiệp sản xuất amoniac, clorua vôi ; vật liệu xây dựng...
Chú ý:
1. Dung dịch nước vôi trong thường dùng để nhận biết
2. Phản ứng tạo clorua vôi. 2. Canxi cacbonat:
Là chất rắn, màu trắng, không tan trong nước, phân hủy ở .
Tan được trong các axit mạnh. Trong tự nhiên
tồn tại ở dạng đá vôi, đá hoa, đá phấn, và thành phần chính của vỏ và mai ốc, sò, hến...
Đá vôi được dùng làm vật liệu xây dựng, sản xuất vôi, xi măng, thủy tinh,... Chú ý: 1.
bị hòa tan trong nước có
2. Sự tạo thành thạch nhũ trong hang động, cặn trong ấm nước là do phản ứng: 3. Canxi sunfat: Canxi sunfat ( ) tồn tại ba dạng: Thạch cao sống: Thạch cao nung: hoặc Thạch cao khan:
Chú ý: Thạch cao nung được dùng để bó bột khi gãy xương, đúc khuôn, nặn tượng. 4. Nước cứng a. Khái niệm
Nước cứng là nước chứa nhiều ion hoặc hoặc cả hai ion đó.
Nước mềm là nước chứa ít hoặc không chứa ion và .
Chú ý: Nước cứng là khái niệm đánh giá nước tự nhiên.
b. Phân loại
Nước cứng có ba loại tính cứng:
Tính cứng tạm thời là tính cứng gây nên bởi ion , dưới dạng muối .
Tính cứng vĩnh cửu là tính cứng gây ra bởi ion ,
dưới dạng muối sunfat hoặc clorua.
Tính cứng toàn phần gồm cả tính cứng tạm thời và cả tính cứng vĩnh cửu. Chú ý:
1. Khi đun nóng mà mất tính cứng thì tính cứng đó được gọi là tính cứng tạm thời.
2. Các bài tập phân biệt tính cứng là dựa vào thành phần ion âm.
c. Tác dụng của nước cứng
Tạo cặn trong nồi hơi, trong ấm nước, trong ống dẫn nước.
Khi giặt quần áo với nước cứng thì xà phòng bị kết tủa, tốn xà phòng, làm quần áo nhanh hỏng do
kết tủa bám vào quần áo.
Làm giảm mùi vị của thức ăn, nước uống, làm thức ăn lâu chín.
d. Cách làm mềm nước cứng
Nguyên tắc làm mềm nước cứng là giảm nồng độ ion và trong nước cứng. Dùng các dung dịch muối
hoặc dùng phương pháp trao đổi ion làm mềm được tất cả các loại tính cứng.
Dùng cách đun nóng hoặc dùng dung dịch kiềm như NaOH, KOH, vừa đủ chỉ làm mềm
được tính cứng tạm thời.
Chú ý: Phương pháp làm mềm nước bằng cách tạo kết tủa với và
gọi là phương pháp kết tủa.
SƠ ĐỒ HỆ THỐNG HÓA
KIM LOẠI KIỀM THỔ (IIA): Cấu hình electron lớp ngoài cùng:
, các kim loại kiềm thổ: Be, Mg, Ca, Sr, Ba. TÍNH CHẤT VẬT LÝ Có màu trắng bạc.
Khối lượng riêng tương đối nhỏ.
Nhiệt độ nóng chảy, nhiệt độ sôi, tính cứng:
o Thấp nhưng cao hơn nhóm IA.
o Hơi cứng hơn kim loại kiềm nhưng vẫn tương đối mềm. TÍNH CHẤT HÓA HỌC - Tính khử mạnh
Chuyên đề luyện thi Hóa học 12 năm 2023 cực hay - Phần 6: Kim Loại Kiềm Thổ
877
439 lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Tài liệu được cập nhật liên tục trong gói này từ nay đến hết tháng 6/2023. Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Tailieugiaovien.com.vn giới thiệu bộ chuyên đề luyện thi môn Hóa học 12 bao gồm: " Phần 6: Kim Loại Kiềm, Kim Loại Kiềm Thổ, Nhôm" mới nhất năm 2022 - 2023 nhằm giúp Giáo viên có thêm tài liệu tham khảo chuyên đề luyện thi Hóa học 12.
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(877 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN Hóa Học
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Lớp 12
Xem thêmTài liệu bộ mới nhất

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết(có lời giải)
CHƯƠNG 6: KIM LOẠI KIỀM, KIM LOẠI KIỀM THỔ, NHÔM VÀ HỢP CHẤT CỦA CHÚNG
BÀI 12: KIM LOẠI KIỀM THỔ VÀ HỢP CHẤT QUAN TRỌNG CỦA KIM LOẠI KIỀM THỔ
Mục tiêu
Kiến thức
+ Biết được vị trí của kim loại kiềm thổ trong bảng tuần hoàn và cấu hình electron nguyên tử.
+ Nêu được tính chất vật lí chung của kim loại kiềm thổ và một số hợp chất quan trọng.
+ Trình bày được tính chất hóa học của kim loại kiềm thổ và một số hợp chất quan trọng của kim
loại kiềm thổ.
+ Chỉ ra được một số ứng dụng các hợp chất quan trọng của kim loại kiềm thổ.
+ Trình bày được thế nào là nước cứng, tác hại của nước cứng và cách làm mềm nước cứng.
Kĩ năng
+ Viết được cấu hình electron của nguyên tử kim loại kiềm thổ và ion tương ứng.
+ Xác định đúng sản phẩm các phản ứng của kim loại kiềm thổ và một số hợp chất của quan
trọng.
+ Giải được các bài toán từ đơn giản đến phức tạp liên quan đến kim loại kiềm thổ và một số hợp
chất quan trọng của kim loại kiềm thổ.
+ Giải được các bài tập xác định loại nước cứng và cách làm mềm nước cứng.
+ Vận dụng kiến thức để giải quyết các bài toán thực tế.
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết(có lời giải)
I. LÍ THUYẾT TRỌNG TÂM
A. KIM LOẠI KIỀM THỔ
1. Cấu hình electron
Cấu hình electron: [Khí hiếm] .
Nguyên tử kim loại kiềm thổ dễ mất hai electron ở lớp ngoài cùng tạo thành ion có điện tích 2+.
Cấu hình electron của ion kim loại kiềm thổ là cấu hình electron của khí hiếm gần nhất đứng trước nó.
Ví dụ: Cấu hình electron của Mg( ):
2. Vị trí trong bảng tuần hoàn
Vị trí nguyên tố trong bảng tuần hoàn:
Số thứ tự = số hiệu nguyên tử.
Chu kì = số lớp electron.
Nhóm IIA (vì có 2 electron lớp ngoài cùng).
Ví dụ: Cấu hình electron của nguyên tử Mg:
Nguyên tố Mg thuộc ô thứ 12, chu kì 3, nhóm IIA.
3. Tính chất vật lí
Các kim loại kiềm thổ có màu trắng bạc, có thể dát mỏng.
Nhiệt độ nóng chảy và nhiệt độ sôi tương đối thấp (nhưng cao hơn kim loại kiềm).
Khối lượng riêng tương đối nhỏ, độ cứng tương đối thấp.
Chú ý: Tính chất vật lí của kim loại kiềm thổ thay đổi không theo quy luật vì chúng có mạng tinh thể khác
nhau
4. Tính chất hóa học
Kim loại kiềm thổ có tính khử mạnh và tính khử tăng dần từ Be đến Ba:
Trong hợp chất kim loại kiềm thổ chỉ có số oxi hóa +2.
Tính khử của kim loại kiềm thổ thể hiện qua các phản ứng với phi kim, axit, nước,...
Chú ý: Ở nhiệt độ thường, Be không tác dụng với nước, Mg phản ứng chậm.
B. MỘT SỐ HỢP CHẤT QUAN TRỌNG CỦA KIM LOẠI KIỀM THỔ
1. Canxi hiđroxit:
Là chất rắn màu trắng, ít tan trong nước.
Tên gọi khác: vôi tôi
Dung dịch gọi là dung dịch nước vôi trong.
có đầy đủ tính chất của một bazơ.
Được dùng trong công nghiệp sản xuất amoniac, clorua vôi ; vật liệu xây dựng...
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết(có lời giải)
Chú ý:
1. Dung dịch nước vôi trong thường dùng để nhận biết
2. Phản ứng tạo clorua vôi.
2. Canxi cacbonat:
Là chất rắn, màu trắng, không tan trong nước, phân hủy ở .
Tan được trong các axit mạnh.
Trong tự nhiên tồn tại ở dạng đá vôi, đá hoa, đá phấn, và thành phần chính của vỏ và mai
ốc, sò, hến...
Đá vôi được dùng làm vật liệu xây dựng, sản xuất vôi, xi măng, thủy tinh,...
Chú ý:
1. bị hòa tan trong nước có
2. Sự tạo thành thạch nhũ trong hang động, cặn trong ấm nước là do phản ứng:
3. Canxi sunfat:
Canxi sunfat ( ) tồn tại ba dạng:
Thạch cao sống:
Thạch cao nung: hoặc
Thạch cao khan:
Chú ý: Thạch cao nung được dùng để bó bột khi gãy xương, đúc khuôn, nặn tượng.
4. Nước cứng
a. Khái niệm
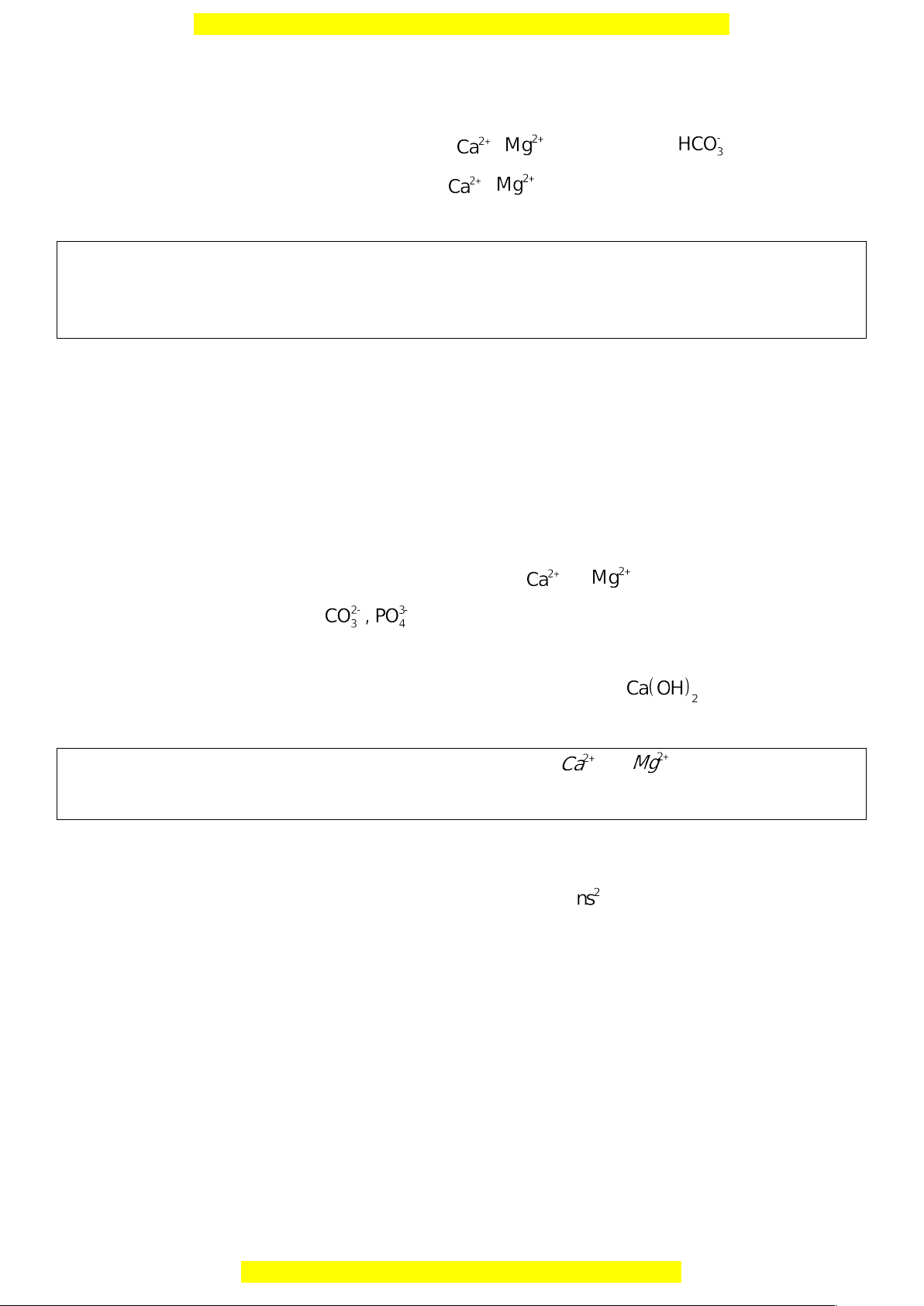
Nước cứng là nước chứa nhiều ion hoặc hoặc cả hai ion đó.
Nước mềm là nước chứa ít hoặc không chứa ion và .
Chú ý: Nước cứng là khái niệm đánh giá nước tự nhiên.
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết(có lời giải)
b. Phân loại
Nước cứng có ba loại tính cứng:
Tính cứng tạm thời là tính cứng gây nên bởi ion , dưới dạng muối .
Tính cứng vĩnh cửu là tính cứng gây ra bởi ion , dưới dạng muối sunfat hoặc clorua.
Tính cứng toàn phần gồm cả tính cứng tạm thời và cả tính cứng vĩnh cửu.
Chú ý:
1. Khi đun nóng mà mất tính cứng thì tính cứng đó được gọi là tính cứng tạm thời.
2. Các bài tập phân biệt tính cứng là dựa vào thành phần ion âm.
c. Tác dụng của nước cứng
Tạo cặn trong nồi hơi, trong ấm nước, trong ống dẫn nước.
Khi giặt quần áo với nước cứng thì xà phòng bị kết tủa, tốn xà phòng, làm quần áo nhanh hỏng do
kết tủa bám vào quần áo.
Làm giảm mùi vị của thức ăn, nước uống, làm thức ăn lâu chín.
d. Cách làm mềm nước cứng
Nguyên tắc làm mềm nước cứng là giảm nồng độ ion và trong nước cứng.
Dùng các dung dịch muối hoặc dùng phương pháp trao đổi ion làm mềm được tất cả
các loại tính cứng.
Dùng cách đun nóng hoặc dùng dung dịch kiềm như NaOH, KOH, vừa đủ chỉ làm mềm
được tính cứng tạm thời.
Chú ý: Phương pháp làm mềm nước bằng cách tạo kết tủa với và gọi là phương pháp kết
tủa.
SƠ ĐỒ HỆ THỐNG HÓA
KIM LOẠI KIỀM THỔ (IIA): Cấu hình electron lớp ngoài cùng: , các kim loại kiềm thổ: Be, Mg,
Ca, Sr, Ba.
TÍNH CHẤT VẬT LÝ
Có màu trắng bạc.
Khối lượng riêng tương đối nhỏ.
Nhiệt độ nóng chảy, nhiệt độ sôi, tính cứng:
o Thấp nhưng cao hơn nhóm IA.
o Hơi cứng hơn kim loại kiềm nhưng vẫn tương đối mềm.
TÍNH CHẤT HÓA HỌC
- Tính khử mạnh
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết(có lời giải)
Tác dụng phi kim
o Tác dụng với
Tác dụng nước
o Kim loại kiềm thổ (trừ Be, Mg) phản ứng với nước ở nhiệt độ thường:
Chú ý: Be không phản ứng với nước, Mg không phản ứng ở nhiệt độ thường nhưng phản
ứng được với nước ở nhiệt độ cao.
Tác dụng với axit
o Tác dụng với dung dịch loãng:
o Tác dụng với đặc (trừ Au, Pt)
Chú ý: Sản phẩm khử có thể xuống hoặc
MỘT SỐ HỢP CHẤT QUAN TRỌNG
(vôi tôi)
o Chất rắn màu trắng, ít tan trong nước.
o Dung dịch được gọi là nước vôi trong là một bazơ mạnh.
o Ứng dụng: chế tạo vữa; khử chua đất trồng; sản xuất , clorua vôi...
o : Thạch cao sống; dùng để sản xuất xi măng.
o hoặc : Thạch cao nung; thường dùng để làm phấn viết, bó
bột, đúc tượng.
o : Thạch cao khan.
( vôi sống)
o Chất rắn màu trắng, không tan trong nước, phân hủy ở nhiệt độ
o Sự xâm thực của nước mưa:
o Sự tạo thành thạch nhũ trong các hang động:
NƯỚC CỨNG ( CHỨA NHIỀU VÀ )
Phân loại
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85




















