SỞ GD&ĐT HƯNG YÊN
ĐÁP ÁN ĐỀ THI CHỌN HỌC SINH GIỎI
TRƯỜNG THPT CHUYÊN HƯNG
KHU VỰC DH&ĐB BẮC BỘ NĂM 2024 YÊN ĐỀ THI MÔN HOÁ LỚP 10
Thời gian làm bài 180 phút (Đề thi đề xuất)
Câu 1: (2,5 điểm) Cấu tạo nguyên tử. Phản ứng hạt nhân. Định luật tuần hoàn
1.1. Biết năng lượng cần cung cấp để tách cả hai electron ra khỏi nguyên tử He là:
79,0 eV. Khi chiếu một bức xạ có bước sóng 40,0 nm vào nguyên tử He thì thấy có
1 electron thoát ra. Tính vận tốc của electron này. Cho hằng số Plank h = 6,625.10- 34J.s; me = 9,1.10-31 kg.
1.2. Radium trong tự nhiên được biểu thị bởi một hạt nhân duy nhất, . 1 gam
radium bức xạ 3,42.1010 hạt α mỗi giây. Một mẫu radium có chứa 192 mg Ra, được
cho vào một thiết bị để đo thể tích He thoát ra. Sau 83 ngày làm thí nghiệm thu
được 6,58 mm3 khí He (0oC, 1atm). Ra phân rã phóng xạ theo sơ đồ cho dưới đây:
A, B, C, D, E, F là các sản phẩm trung gian của phân rã radon.
a. Viết năm phương trình phân rã phóng xạ đầu tiên.
b. Tính trị số gần đúng của số Avogadro từ số liệu trên.
1.3. Ở trạng thái cơ bản, electron cuối cùng của nguyên tử mỗi nguyên tố X, Y, Z
có bộ 4 số lượng tử đều thỏa mãn điều kiện n + l = 5 và ml.s = 1.
Viết cấu hình electron và gọi tên của X, Y, Z. CÂU NỘI DUNG ĐIỂM
1.1. Theo đề bài có: He He2+ + 2e ; I = + 79,00 eV
Mặt khác, He+ He2+ + 1e ; I2 = ‒ Ee trong He+ 0,25
mà He+ là hệ 1 hạt nhân 1 electron I2 = = + 54,4 eV 0,25
I1, He = I – I2 = 24,60 eV = 3,941.10-18 (J)
Năng lượng của bức xạ: 0,5 Wđ (e) =
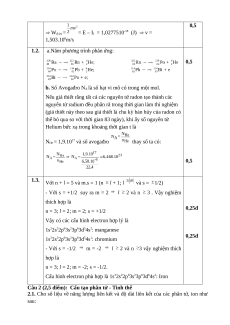
= E – I1 = 1,0277510-18 (J) v = 1,503.106m/s
1.2. a.Năm phương trình phản ứng: 0,5
b. Số Avogađro NA là số hạt vi mô có trong một mol.
Nếu giả thiết rằng tất cả các nguyên tử radon tạo thành các
nguyên tử radium đều phân rã trong thời gian làm thí nghiệm
(giả thiết này theo sau giả thiết là chu kỳ bán hủy của radon có
thể bỏ qua so với thời gian 83 ngày), khi ấy số nguyên tử
Helium bức xạ trong khoảng thời gian t là
NHe = 1,9.1017 và số avogađro thay số ta có: 0,5
1.3. Với n + l = 5 và m.s = 1 (n l + 1; l và s = 1/2) - Với s = +1/2 suy ra m = 2
l 2 và n 3 . Vậy nghiệm thích hợp là 0,25đ
n = 3; l = 2; m = 2; s = +1/2
Vậy có các cấu hình electron hợp lý là
1s22s22p63s23p63d54s2: manganese 0,25đ
1s22s22p63s23p63d54s1: chromium
- Với s = -1/2 m = -2 l 2 và n 3 vậy nghiệm thích hợp là
n = 3; l = 2; m = -2; s = -1/2.
Cấu hình electron phù hợp là 1s22s22p63s23p63d64s2: Iron
Câu 2 (2,5 điểm): Cấu tạo phân tử - Tinh thể
2.1. Cho số liệu về năng lượng liên kết và độ dài liên kết của các phân tử, ion như sau:
Năng lượng liên kết 945 841 498 623 (kJ.mol‒1)
Độ dài liên kết (pm) 110 112 121 112
Dữ kiện trên cho thấy khi N2 mất đi một electron để hình thành ion thì năng
lượng liên kết giảm, độ dài liên kết tăng; trong khi đó, khi O2 mất đi một electron để hình thành ion
thì năng lượng liên kết lại tăng còn độ dài liên kết giảm. Dựa
vào thuyết MO hãy giải thích hiện tượng này.
2.2. Trong các iron tinh thể (cấu trúc lập phương tâm khối) các nguyên tử carbon
có thể chiếm các mặt của ô mạng cơ sở.
a. Bán kính kim loại của iron là 1,24 . Tính độ dài cạnh a của ô mạng cơ sở.
b. Bán kính cộng hóa trị của carbon là 0,77 . Hỏi độ dài cạnh a sẽ tăng lên
bao nhiêu khi iron có chứa carbon so với cạnh a khi iron nguyên chất.
c. Tính độ dài cạnh ô mạng cơ sở cho iron (cấu trúc lập phương tâm diện) và
tính độ tăng chiều dài cạnh ô mạng biết rằng các nguyên tử C có thể chiếm
tâm của các ô mạng cơ sở và bán kính kim loại iron là 1,26 . Có thể kết
luận gì về khả năng xâm nhập của carbon vào 2 loại tinh thể iron trên. Câ Hướng dẫn chấm Điểm u
2.1 N có 5 electron hóa trị nên N2 có 10 electron hóa trị, có 9 electron hóa trị.
Cấu hình electron: N2: (kk)(σs)2(σ*s)2(πx)2(πy)2(σz)2 0,5
: (kk)(σs)2(σ*s)2(πx)2(πy)2(σz)1 Bậc liên kết: N2: :
Do 3 > 2,5 nên độ dài liên kết của > N2 0,5
và năng lượng liên kết < N2. 2.2
a. Iron : lập phương tâm khối 0,25 R = 1,24 a = 2,864
b. Độ dài đường chéo mặt bên
> 2R + 2r (tức là 4,05 > 0,5 2.1,24 + 2. 0,77)
Vậy khi C chiếm tâm của mặt bên thì không tiếp xúc với các quả cầu ở các đỉnh
Khoảng cách từ tâm của ô mạng đến tâm của mặt bên:
< R + r (tức là 1,432 < 1,24 + 0,77)
Vậy C ở tâm mặt bên thì tiếp xúc với quả cầu ở tâm
Vì vậy làm cạnh a tăng lên: [(1,24 + 0,77) – 1,432) * 2 = 1,156
(nói cách khác: 2R + 2r – a = 1,156)
c. Iron : lập phương tâm diện 0,5 Độ dài cạnh a’ = 4R’ a’ = 3,564
Khi C chiếm tâm của ô mạng làm cho cạnh tăng thêm: 1,26. 2 + 0,77.2 – 3,564 = 0,496
Kết luận: C xâm nhập vào iron dễ hơn iron 0,25
Câu 3 (2,5 điểm): Nhiệt hóa học
3.1. Người ta đưa 3,6 gam một hydrocarbons X (khí) cùng một lượng dư
oxygen vào một bom nhiệt kế ban đầu chứa 600 gam nước tại 200C. Sau phản ứng
xong nhiệt độ của nhiệt lượng kế lên tới 280C, thấy có 11 gam CO2 (khí) và 5,4
gam H2O (lỏng) tạo thành.
Cho biết: - Nhiệt sinh chuẩn của CO2 (khí) là -393,51 kJ/mol; của H2O (lỏng) là 285,83 kJ/mol.
- Nhiệt dung riêng của nước là 4,184 J/g.K
- Biến thiên nội năng của phản ứng trên là kJ/mol
a) Xác định công thức phân tử của X và tính nhiệt dung riêng của nhiệt lượng kế.
b) Xác định nhiệt sinh chuẩn của X.
3.2. Hoá lỏng 1mol khí oxygen ở -1830C bằng cách nén ở áp suất 1 atm.
Oxygen sau khi đã hoá lỏng được làm lạnh ở áp suất không đổi đến nhiệt độ nóng
chảy là -2180C, sau đó được hoá rắn thuận nghịch và chất rắn sau đó được làm lạnh
đến -2630C. Hãy tính H (hệ) và S (hệ) của toàn bộ quá trình trên.
Cho: Cp (l) = 54 J.K1.mol1; Cp (r) = 41 J.K1.mol1; H (hoá hơi) = 6,82 kJ.mol1; H
(nóng chảy) = 0,42 kJ.mol1.
Đề thi HSG Hóa học 10 Trường THPT Chuyên Hưng Yên
822
411 lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Tailieugiaovien.com.vn giới thiệu Tổng hợp đề thi chọn học sinh giỏi Hóa học 10 của các trường THPT Chuyên khu vực Duyên hải và Đồng bằng Bắc Bộ gồm 29 đề đề xuất và 1 đề chính thức có lời giải giúp giáo viên, học sinh có thêm tài liệu tham khảo.
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(822 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)