SỞ GD&ĐT BÌNH DƯƠNG
KỲ THI CHỌN HỌC SINH GIỎI TRƯỜNG THPT
KHU VỰC DUYÊN HẢI & ĐỒNG BẰNG BẮC BỘ
CHUYÊN HÙNG VƯƠNG BD LẦN THỨ XV
MÔN: HÓA HỌC - LỚP 10 HDC ĐỀ ĐỀ
Thời gian làm bài: 180 phút, không kể thời gian giao đề XUẤT
Câu 1 (2,5 điểm): Cấu tạo nguyên tử. Phản ứng hạt nhân. Định luật tuần hoàn
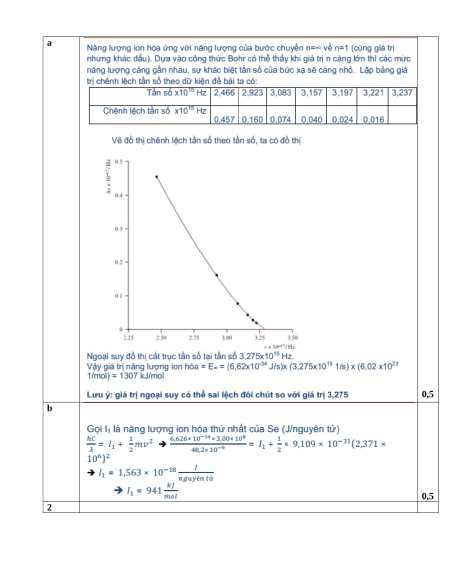
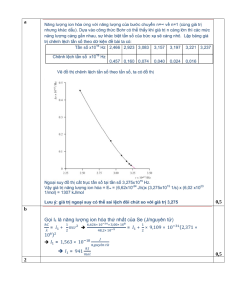
1. a) Tần số của các vạch phổ thuộc dãy Lyman (bước chuyển electron từ n>1 về n=1) của nguyên tử
hydrogen lần lượt là 2,466; 2,923; 3,083; 3,157; 3,197; 3,221; và 3,237 (x1015 Hz). Dựa vào các giá trị
này hãy xác định năng lượng ion hóa của nguyên tử hydrogen (kJ/mol)
b) Tính năng lượng ion hóa thứ nhất (kJ/mol) của các nguyên tử selen, biết khi chiếu chùm sáng
đơn sắc có bước sóng 48,2 nm vào các nguyên tử selen ở trạng thái cơ bản và ở thể khí thì tạo ra chùm
electron có vận tốc 2,371x106 m/s.
Biết khối lượng của 1 electron bằng 9,109x10-31 kg.
2. a) Đồng vị 238U có thời gian bán huỷ, t1/2 = 4,5 x 109 năm và 235U có thời gian bán huỷ, t1/2 =7,0 x 108
năm. Trong tự nhiên, 238U chiếm 99,28% còn 235U chiếm 0,72% về khối lượng. Một quặng được tìm thấy
chứa 50% urani theo khối lượng. Tính tỉ lệ phân rã (tỉ lệ hoạt độ phóng xạ) giữa hai đồng vị trong tự
nhiên. Xác định hoạt độ phóng xạ của 238U trong 1 kg quặng này.
b) Một chuỗi phân rã vô tình tìm thấy trong động người xưa: 97Ru 97Tc 97Mo (bền). Thời gian
bán rã của ruteni va tecneti lần lượt là 2,7 ngày và 2,6.106 năm. Tại thời điểm ban đầu, chỉ có 97Ru với
hoạt độ phóng xạ là 109 Bq. Cho biết sau bao lâu hoạt độ phóng xạ hạt nhân này gấp đôi hạt nhân kia, khi
đó hoạt độ phóng xạ của mỗi hạt nhân là bao nhiêu? Câu 1 Nội dung Đi ểm 1 a 0,5 b 0,5 2 a = 21,18
Khối lượng 238U trong quặng m = 1000.50%.99,28% = 496,4 (gam)
Số nguyên tử 238U trong quặng N = (496,4/238).6,022.1023 = 1,256.1024 (nguyên tử) 0,5
Hoạt độ phóng xạ của 238U trong quặng: A = N.k = 1,256.1024.ln2/(4,5.109)
= 1,9347.1014 phân rã/năm = 6,135.106 Bq b
k1 = kRu = ln2/tRu = 0,2567 ngày-1 k2 = kTc = ln2/tTc = 7,304.10-10 ngày-1 0,5
Do k1 » k2 nên ta có NTc = ATc =
Trường hợp 1: ARu/ATc = 2 t = 73,95 ngày ARu= =5,69; ATc = 2,845
Trường hợp 2: ARu/ATc = 1/2 t = 79,35 ngày ARu = 1,42; ATc = 2,84 0,5
Câu 2 (2,5 điểm): Cấu tạo phân tử. Tinh thể
1. Thiourea-S,S- dioxide là một chất bột màu trắng được sử dụng trong ngành dệt may và có công thức là O2SC(NH2)2.
a. Thiourea-S,S- dioxide được điều chế bằng cách oxid hóa thiourea bằng hydrogen peroxide.
Viết phương trình hóa học của phản ứng xảy ra.
b. Vẽ công thức Lewis của Thiourea-S,S- dioxide, biết rằng điện tích hình thức trên các nguyên tử đều bằng 0.
2. Mặc dù hợp chất “Mg2Fe” kém bền nhưng khi khám phá những vật liệu lưu trữ hydrogen,
hydride bền tương ứng của hợp chất này có khả năng lưu trữ hydrogen đáng kể đã được tổng
hợp. Cấu trúc của hydride này thuộc hệ tinh thể có kiểu mạng lập phương tâm diện, thông số
mạng a = 644,58 pm, và ô mạng đơn vị được biểu diễn như hình bên (chưa bao gồm các nguyên tử hydrogen).
Trong cấu trúc này, có thể xem các nguyên tử Fe sắp xếp
theo kiểu lập phương đặc khít. Các nguyên tử Mg chiếm các
hốc tứ diện và các nguyên tử H được phân bố đồng đều
quanh nguyên tử Fe theo phối trí bát diện đều. Khoảng cách ngắn nhất
giữa các nguyên tử H và Fe bằng ¼ thông số mạng.
(a) Xác định công thức hoá học của hydride và tổng số (m)
nguyên tử H trong ô mạng đơn vị.
(b) Tính độ dài liên kết Fe–H, Mg–H và khoảng cách H–H ngắn nhất. Xác định số (n) nguyên tử
H tạo phối trí với Mg.
(c) Tính khối lượng riêng ρ (theo g.cm–3) của hydrogen trong hydride và khối lượng riêng của ρo
của khí hydrogen ở điều kiện chuẩn (1 bar, 298 K). Từ đó, cho biết vì sao hydride này được sử
dụng làm vật liệu lưu trữ hydrogen? Câu 2 Nội dung Điểm 1 Phương trình hóa học: 0,25
S=C(NH2)2 + 2H2O2 O2S=C(NH2)2 + H2O 0,25 2
Công thức hóa học: Mg2FeH6 0,5
Tổng số nguyên tử hydrogen trong một ô mạng cơ sở: m = 831/4 + 6 (41/2 + 1) = 24
Độ dài liên kết Fe-H: dFe-H = ¼ a = ¼ 644,58 = 161,145 (pm) 0.5
Độ dài liên kết Mg-H: dMg-H = =
Khoảng cách H-H ngắn nhất: dH-H (min) = =
Số nguyên tử H phối trí với Mg: 12
Khối lượng riêng của hydrogen trong hydride này: 1,0
Khối lượng riêng của khí hydrogen ở điều kiện chuẩn (1 bar, 298K): Tỉ số R = /o =
Tỉ số R = /o cho biết mật độ hydrogen trong hydride lớn hơn 1000 lần so với
trong điều kiện chuẩn nên hydride này phù hợp sử dụng làm vật liệu lưu trữ hydrogen.
Câu 3 (2,5 điểm) : Nhiệt hóa học.
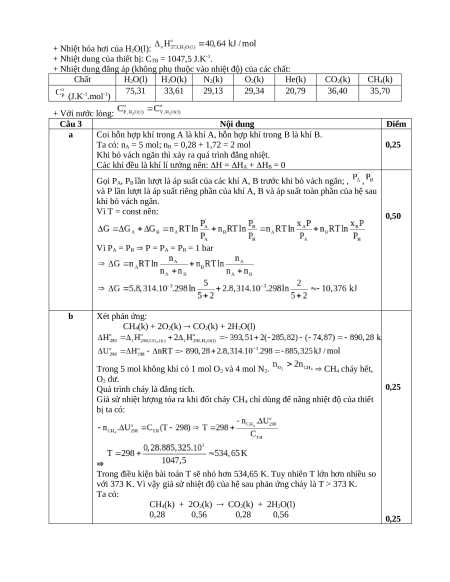
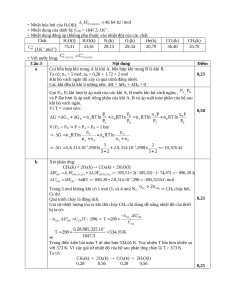
Một thiết bị hình trụ (không bị biến dạng) được chia thành hai khoang A và B bằng một vách ngăn
(có thể tích không đáng kể). Khoang A chứa 5 mol không khí ở 1,0 bar, 298 K. Khoang B chứa
0,28 mol CH4 và 1,72 mol He ở 1,0 bar, 298 K.
a. Bỏ vách ngăn để các khí ở hai khoang trộn lẫn vào nhau. Tính H và G của quá trình trộn.
b. Đốt cháy hoàn toàn lượng CH4 có trong bình. Tính áp suất của bình (theo bar) sau khi phản ứng cháy diễn ra.
Giả sử: - Không có sự trao đổi nhiệt giữa thiết bị và môi trường; H2O(l) chỉ hóa hơi và hóa hơi
hoàn toàn tại 373 K; có thể bỏ qua thể tích của H2O(l).
- Mỗi chất khí và hỗn hợp khí đều xử sự như khí lí tưởng; O2 chiếm 20% thể tích không khí, còn lại là N2. Cho biết:
+ Nhiệt hình thành chuẩn của các chất: ;
Đề thi HSG Hóa học 10 Trường THPT Chuyên HV - Bình Dương
1.1 K
569 lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Tailieugiaovien.com.vn giới thiệu Tổng hợp đề thi chọn học sinh giỏi Hóa học 10 của các trường THPT Chuyên khu vực Duyên hải và Đồng bằng Bắc Bộ gồm 29 đề đề xuất và 1 đề chính thức có lời giải giúp giáo viên, học sinh có thêm tài liệu tham khảo.
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(1138 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)