111Equation Chapter 1 Section 1ĐẠI
ĐỀ THI TUYỂN SINH LỚP 10 HỌC QUỐC GIA TP HCM Năm học 2023
TRƯỜNG PHỔ THÔNG NĂNG KHIẾU Môn thi: HÓA HỌC
HỘI ĐỒNG TUYỂN SINH LỚP 10
Thời gian làm bài: 120 phút, không kể thời gian phát đề
Thí sinh không được sử dụng tài liệu, kể cả bảng phân loại tuần hoàn Câu 1 (1,5 điểm).
Nung muối mangan (II) nitrat ở 300oC thu được một chất rắn A và một chất khí B
màu nâu đỏ. Chất rắn A được dùng làm pin khô. Đun nóng nhẹ A với dung dịch HCl
đậm đặc thu được chất C và khí D. Cho khí D phản ứng với dung dịch NaOH thu
được dung dịch E. Kim loại sắt nung đỏ phản ứng với D tạo thành chất F. Dung dịch
muối mangan (II) nitrat phản ứng với amoniac và cacbon đioxit tạo kết tủa G và dung
dịch chứa chất tan H. Chất H thường được dùng làm phân bón hóa học. Xác định
công thức từng chất và viết phương trình hóa học. Câu 2 (1,5 điểm).
Diamoni hidrophotphat (DAP) là một loại phân bón hóa học
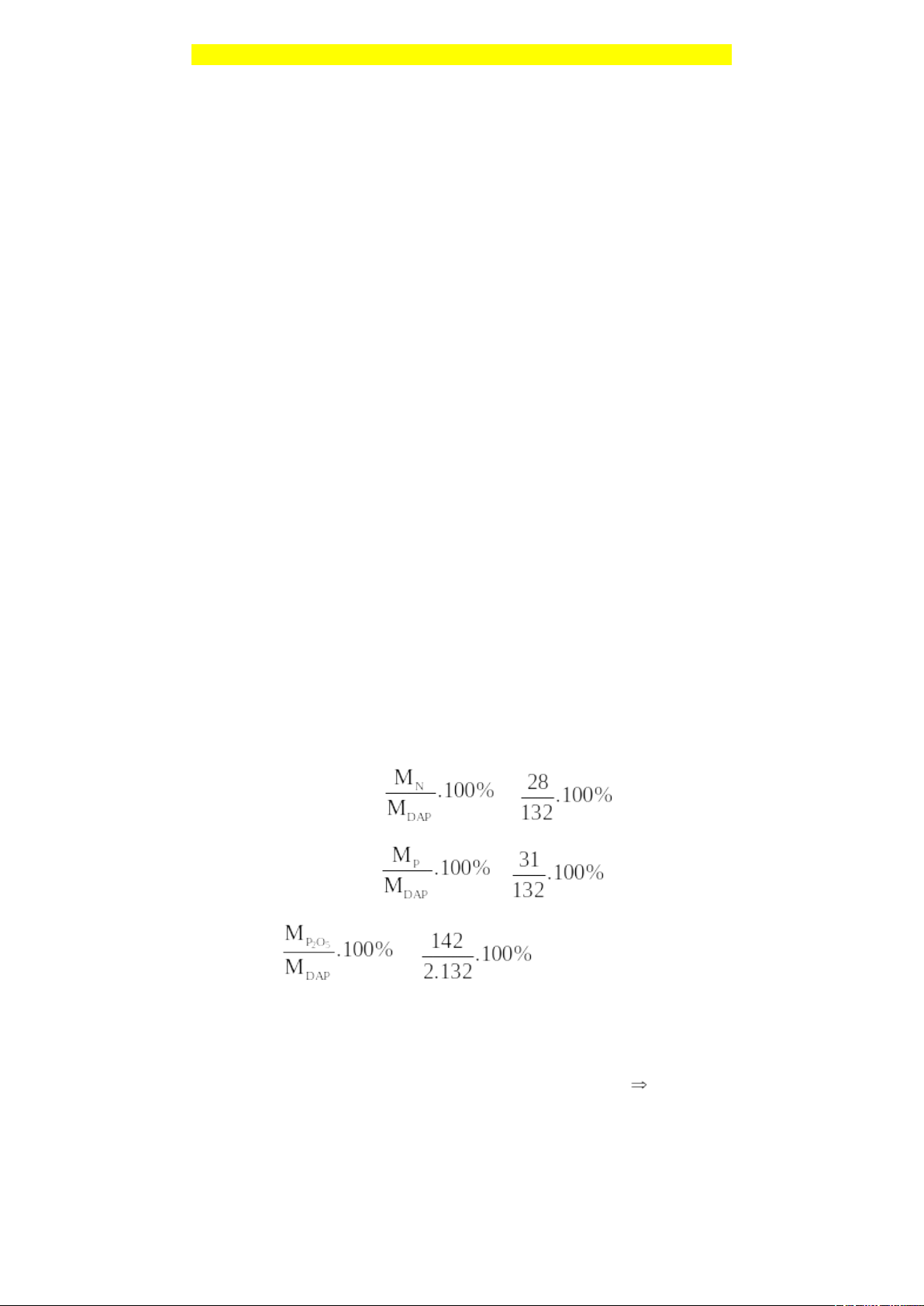
a) Phân bón hóa học này cung cấp nguyên tố dinh dưỡng nào cho cây trồng? Xác
định hàm lượng các nguyên tố đó trong công thức của DAP?
b) Trên bao bì phân bón DAP thương mại có ghi các chữ số 18 – 46 – 0. Cho biết ý
nghĩa của các chữ số này? Tính các chữ số tương ứng của một mẫu DAP tinh khiết,
từ đó nhận xét gì về độ tinh khiết của phân bón DAP thương mại.
c) DAP được điều chế từ một hợp chất có tính bazo và một hợp chất có tính axit. Viết phương trình hóa học.
d) DAP còn được điều chế từ ure và một dung dịch axit (như câu c). Viết phương trình hóa học.
e) Ở 70oC, DAP phân hủy dần thành một chất khí và một chất rắn. Viết phương trình hóa học. Câu 3 (1 điểm).
Nung một khoáng chất A có trong tự nhiên (sau khi loại bỏ các tạp chất) chỉ thu được
chất rắn là MgO. Phản ứng của 9,32 gam chất A với 100ml dung dịch HCl 2,5 M, tạo
thành 1,792 lít khí CO2 (đktc), dung dịch B chỉ chứa muối và HCl dư. Lượng HCl dư
này phản ứng vừa đủ với 20ml dung dịch NaOH 2,5M. Xác định công thức phân tử
của chất A và viết các phương trình hóa học. Tính phần trăm khối lượng chất rắn thu
được so với khối lượng chất rắn A trước khi nung. Câu 4 (2 điểm)
Polime có nguồn gốc ngoài từ dầu khí, còn có thể được tổng hợp từ nguồn sinh khối
như tinh bột, xenlulozơ. Một ví dụ minh họa cho quá trình tổng hợp polime từ nguồn
gốc sinh khối được trình bày như sau: Trước hết tinh bột hoặc xenlulozơ được chuyển
hóa thành đường, tiếp theo thành rượu etylic và sau đó thành axit axetic. Đun nóng
rượu etylic với axit sunfuric đặc ở 180oC thu được A và nước. Phản ứng của A với
dung dịch brom thu được B. Tác dụng của bazo mạnh lên B tạo thành chất C không
còn chứa brom. Phản ứng của C với axit axetic xúc tác thủy ngân(II) tạo thành este D.
Cũng có thể tổng hợp D bằng cách cho A phản ứng với axit axetic, oxi, xúc tác Pd.
Tiến hành polime hóa D trong điều kiện xúc tác thích hợp tạo thành polime E. Đun
nóng E trong dung dịch kiềm, sau đó axit hóa thu được polime F. Polime F được ứng
dụng phổ biến làm keo dán, chất tạo đặc, sơn…Viết các phương trình hóa học để mô
tả quá trình chuyển hóa từ tinh bột, xenlulozơ thành polime F. Câu 5 (2 điểm).
a) Thành phần chính của bông vải là gì? Viết công thức phân tử?
b) Bông vải được tạo thành trong cây từ các chất nào? Viết phương trình hóa học tương ứng?
c) Bông vải có cho phản ứng với H2SO4 đặc, nóng không? Nếu có mô tả hiện tượng
và viết các phương trình hóa học.
d) Cho bông vải phản ứng với hỗn hợp HNO3 và H2SO4. Viết phương trình hóa học.
Để làm verni, phim, chất dẻo hàm lượng nitơ trong sản phẩm cần 12%. Đề nghị công
thức hóa học của sản phẩm.
Câu 6 (2 điểm).
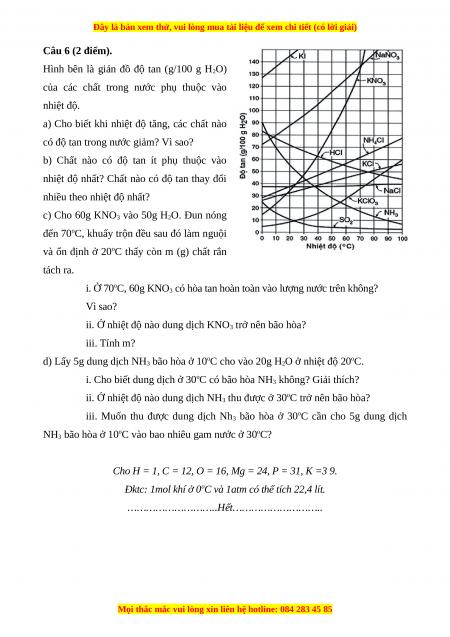
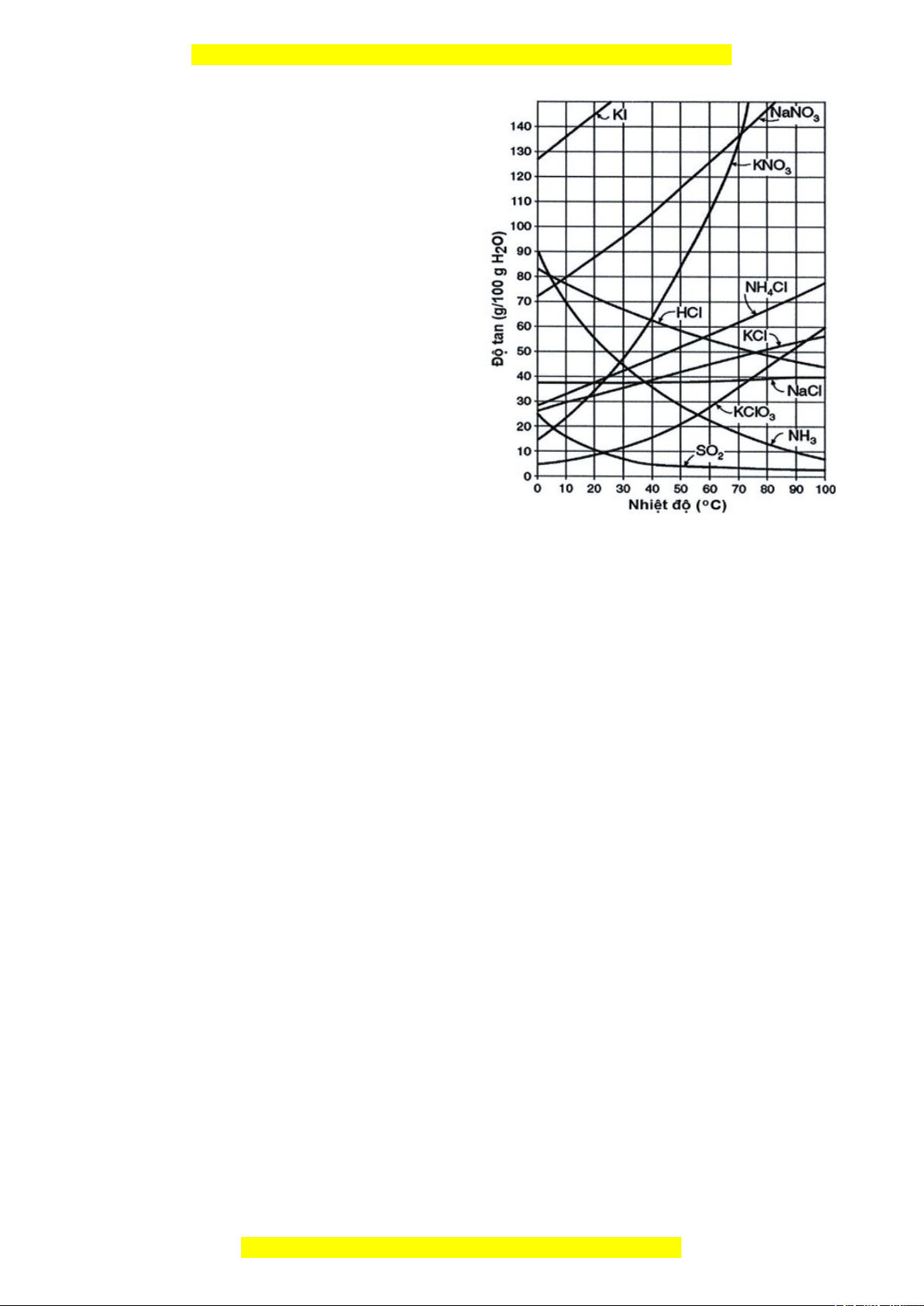
Hình bên là giản đồ độ tan (g/100 g H2O)
của các chất trong nước phụ thuộc vào nhiệt độ.
a) Cho biết khi nhiệt độ tăng, các chất nào
có độ tan trong nước giảm? Vì sao?
b) Chất nào có độ tan ít phụ thuộc vào
nhiệt độ nhất? Chất nào có độ tan thay đổi
nhiều theo nhiệt độ nhất?
c) Cho 60g KNO3 vào 50g H2O. Đun nóng
đến 70oC, khuấy trộn đều sau đó làm nguội
và ổn định ở 20oC thấy còn m (g) chất rắn tách ra.
i. Ở 70oC, 60g KNO3 có hòa tan hoàn toàn vào lượng nước trên không? Vì sao?
ii. Ở nhiệt độ nào dung dịch KNO3 trở nên bão hòa? iii. Tính m?
d) Lấy 5g dung dịch NH3 bão hòa ở 10oC cho vào 20g H2O ở nhiệt độ 20oC.
i. Cho biết dung dịch ở 30oC có bão hòa NH3 không? Giải thích?
ii. Ở nhiệt độ nào dung dịch NH3 thu được ở 30oC trở nên bão hòa?
iii. Muốn thu được dung dịch Nh3 bão hòa ở 30oC cần cho 5g dung dịch
NH3 bão hòa ở 10oC vào bao nhiêu gam nước ở 30oC?
Cho H = 1, C = 12, O = 16, Mg = 24, P = 31, K =3 9.
Đktc: 1mol khí ở 0oC và 1atm có thể tích 22,4 lít.
………………………..Hết………………………..
HƯỚNG DẪN CHẤM ĐỀ TUYỂN SINH LỚP 10 CHUYÊN HÓA
THPT NĂNG KHIẾU THÀNH PHỐ HỒ CHÍ MINH
Năm học 2022 – 2023 Môn thi: HÓA HỌC Câu 1 (1,5 điểm).
Nung muối mangan(II) nitrat ở 300oC thu được một chất rắn A và một chất khí B
màu nâu đỏ. Chất rắn A được dùng làm pin khô. Đun nóng nhẹ A với dung dịch HCl
đậm đặc thu được chất C và khí D. Cho khí D phản ứng với dung dịch NaOH thu
được dung dịch E. Kim loại sắt nung đỏ phản ứng với D tạo thành chất F. Dung dịch
muối mangan (II) nitrat phản ứng với amoniac và cacbon đioxit tạo kết tủa G và dung
dịch chứa chất tan H. Chất H thường được dùng làm phân bón hóa học. Xác định
công thức từng chất và viết phương trình hóa học. Hướng dẫn giải:
Các phương trình phản ứng hóa học xảy ra là 1. Mn(NO3)2 MnO2 + 2NO2 ↑. 2. MnO2 + 4HClđặc MnCl2 + Cl2↑ + 2H2O.
3. Cl2 + 2NaOH → NaCl + NaClO + H2O. 4. 2Fe + 3Cl2 2FeCl3.
5. Mn(NO3)2 + NH3 + CO2 + H2O → MnCO3 + NH4NO3.
Vậy theo thứ tự các chất lần lượt là
A: MnO2 – chất làm pin khô
B: NO2 – khí màu nâu đỏ C: MnCl2 D: Cl2
E: NaCl, NaClO, H2O – nước giaven F: FeCl3
G: MnCO3 – chất kết tủa
H: NH4NO3 – chất dùng làm phân bón
Document Outline
- Nung muối mangan (II) nitrat ở 300oC thu được một chất rắn A và một chất khí B màu nâu đỏ. Chất rắn A được dùng làm pin khô. Đun nóng nhẹ A với dung dịch HCl đậm đặc thu được chất C và khí D. Cho khí D phản ứng với dung dịch NaOH thu được dung dịch E. Kim loại sắt nung đỏ phản ứng với D tạo thành chất F. Dung dịch muối mangan (II) nitrat phản ứng với amoniac và cacbon đioxit tạo kết tủa G và dung dịch chứa chất tan H. Chất H thường được dùng làm phân bón hóa học. Xác định công thức từng chất và viết phương trình hóa học.
- Câu 2 (1,5 điểm).
- Diamoni hidrophotphat (DAP) là một loại phân bón hóa học
- a) Phân bón hóa học này cung cấp nguyên tố dinh dưỡng nào cho cây trồng? Xác định hàm lượng các nguyên tố đó trong công thức của DAP?
- b) Trên bao bì phân bón DAP thương mại có ghi các chữ số 18 – 46 – 0. Cho biết ý nghĩa của các chữ số này? Tính các chữ số tương ứng của một mẫu DAP tinh khiết, từ đó nhận xét gì về độ tinh khiết của phân bón DAP thương mại.
- c) DAP được điều chế từ một hợp chất có tính bazo và một hợp chất có tính axit. Viết phương trình hóa học.
- d) DAP còn được điều chế từ ure và một dung dịch axit (như câu c). Viết phương trình hóa học.
- e) Ở 70oC, DAP phân hủy dần thành một chất khí và một chất rắn. Viết phương trình hóa học.
- Câu 3 (1 điểm).
- Nung một khoáng chất A có trong tự nhiên (sau khi loại bỏ các tạp chất) chỉ thu được chất rắn là MgO. Phản ứng của 9,32 gam chất A với 100ml dung dịch HCl 2,5 M, tạo thành 1,792 lít khí CO2 (đktc), dung dịch B chỉ chứa muối và HCl dư. Lượng HCl dư này phản ứng vừa đủ với 20ml dung dịch NaOH 2,5M. Xác định công thức phân tử của chất A và viết các phương trình hóa học. Tính phần trăm khối lượng chất rắn thu được so với khối lượng chất rắn A trước khi nung.
- Câu 4 (2 điểm)
- Polime có nguồn gốc ngoài từ dầu khí, còn có thể được tổng hợp từ nguồn sinh khối như tinh bột, xenlulozơ. Một ví dụ minh họa cho quá trình tổng hợp polime từ nguồn gốc sinh khối được trình bày như sau: Trước hết tinh bột hoặc xenlulozơ được chuyển hóa thành đường, tiếp theo thành rượu etylic và sau đó thành axit axetic. Đun nóng rượu etylic với axit sunfuric đặc ở 180oC thu được A và nước. Phản ứng của A với dung dịch brom thu được B. Tác dụng của bazo mạnh lên B tạo thành chất C không còn chứa brom. Phản ứng của C với axit axetic xúc tác thủy ngân(II) tạo thành este D. Cũng có thể tổng hợp D bằng cách cho A phản ứng với axit axetic, oxi, xúc tác Pd. Tiến hành polime hóa D trong điều kiện xúc tác thích hợp tạo thành polime E. Đun nóng E trong dung dịch kiềm, sau đó axit hóa thu được polime F. Polime F được ứng dụng phổ biến làm keo dán, chất tạo đặc, sơn…Viết các phương trình hóa học để mô tả quá trình chuyển hóa từ tinh bột, xenlulozơ thành polime F.
- Câu 5 (2 điểm).
- a) Thành phần chính của bông vải là gì? Viết công thức phân tử?
- b) Bông vải được tạo thành trong cây từ các chất nào? Viết phương trình hóa học tương ứng?
- c) Bông vải có cho phản ứng với H2SO4 đặc, nóng không? Nếu có mô tả hiện tượng và viết các phương trình hóa học.
- d) Cho bông vải phản ứng với hỗn hợp HNO3 và H2SO4. Viết phương trình hóa học. Để làm verni, phim, chất dẻo hàm lượng nitơ trong sản phẩm cần 12%. Đề nghị công thức hóa học của sản phẩm.
- Câu 6 (2 điểm).
- Hình bên là giản đồ độ tan (g/100 g H2O) của các chất trong nước phụ thuộc vào nhiệt độ.
- a) Cho biết khi nhiệt độ tăng, các chất nào có độ tan trong nước giảm? Vì sao?
- b) Chất nào có độ tan ít phụ thuộc vào nhiệt độ nhất? Chất nào có độ tan thay đổi nhiều theo nhiệt độ nhất?
- c) Cho 60g KNO3 vào 50g H2O. Đun nóng đến 70oC, khuấy trộn đều sau đó làm nguội và ổn định ở 20oC thấy còn m (g) chất rắn tách ra.
- i. Ở 70oC, 60g KNO3 có hòa tan hoàn toàn vào lượng nước trên không?
- Vì sao?
- ii. Ở nhiệt độ nào dung dịch KNO3 trở nên bão hòa?
- iii. Tính m?
- d) Lấy 5g dung dịch NH3 bão hòa ở 10oC cho vào 20g H2O ở nhiệt độ 20oC.
- i. Cho biết dung dịch ở 30oC có bão hòa NH3 không? Giải thích?
- ii. Ở nhiệt độ nào dung dịch NH3 thu được ở 30oC trở nên bão hòa?
- iii. Muốn thu được dung dịch Nh3 bão hòa ở 30oC cần cho 5g dung dịch NH3 bão hòa ở 10oC vào bao nhiêu gam nước ở 30oC?
- Cho H = 1, C = 12, O = 16, Mg = 24, P = 31, K =3 9.
- Đktc: 1mol khí ở 0oC và 1atm có thể tích 22,4 lít.
- ………………………..Hết………………………..
- Câu 2 (1,5 điểm).
- Diamoni hidrophotphat (DAP) là một loại phân bón hóa học
- a) Phân bón hóa học này cung cấp nguyên tố dinh dưỡng nào cho cây trồng? Xác định hàm lượng các nguyên tố đó trong công thức của DAP?
- b) Trên bao bì phân bón DAP thương mại có ghi các chữ số 18 – 46 – 0. Cho biết ý nghĩa của các chữ số này? Tính các chữ số tương ứng của một mẫu DAP tinh khiết, từ đó nhận xét gì về độ tinh khiết của phân bón DAP thương mại.
- c) DAP được điều chế từ một hợp chất có tính bazơ và một hợp chất có tính axit. Viết phương trình hóa học.
- d) DAP còn được điều chế từ ure và một dung dịch axit (như câu c). Viết phương trình hóa học.
- (7) C2H2 + CH3COOH CH3COOCH=CH2.
- Câu 5 (2điểm).
- a) Thành phần chính của bông vải là gì? Viết công thức phân tử?
- b) Bông vải được tạo thành trong cây từ các chất nào? Viết phương trình hóa học tương ứng?
- c) Bông vải có cho phản ứng với H2SO4 đặc, nóng không? Nếu có mô tả hiện tượng và viết các phương trình hóa học.
- Câu 6 (2 điểm).
- Hình bên là giản đồ độ tan (g/100 g H2O) của các chất trong nước phụ thuộc vào nhiệt độ.
- a) Cho biết khi nhiệt độ tăng, các chất nào có độ tan trong nước giảm? Vì sao?
- b) Chất nào có độ tan ít phụ thuộc vào nhiệt độ nhất? Chất nào có độ tan thay đổi nhiều theo nhiệt độ nhất?
- c) Cho 60g KNO3 vào 50g H2O. Đun nóng đến 70oC, khuấy trộn đều sau đó làm nguội và ổn định ở 20oC thấy còn m (g) chất rắn tách ra.
- i. Ở 70oC, 60g KNO3 có hòa tan hoàn toàn vào lượng nước trên không?
- Vì sao?
- ii. Ở nhiệt độ nào dung dịch KNO3 trở nên bão hòa?
- iii. Tính m?
- d) Lấy 5g dung dịch NH3 bão hòa ở 10oC cho vào 20g H2O ở nhiệt độ 20oC.
- i. Cho biết dung dịch ở 30oC có bão hòa NH3 không? Giải thích?
- ii. Ở nhiệt độ nào dung dịch NH3 thu được ở 30oC trở nên bão hòa?
- iii. Muốn thu được dung dịch Nh3 bão hòa ở 30oC cần cho 5g dung dịch NH3 bão hòa ở 10oC vào bao nhiêu gam nước ở 30oC?