Bảng đặc tả, ma trận và đề kiểm tra cuối học kì II (có đáp án chi tiết) Môn: Hoá học 10
Bộ sách: Kết nối tri thức với cuộc sống
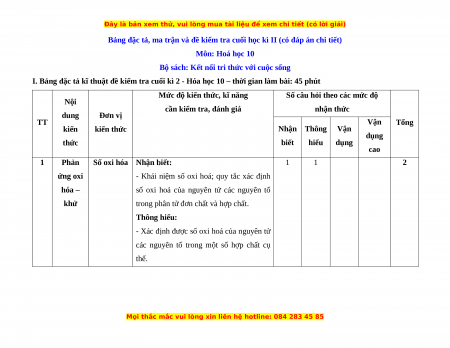
I. Bảng đặc tả kĩ thuật đề kiểm tra cuối kì 2 - Hóa học 10 – thời gian làm bài: 45 phút
Mức độ kiến thức, kĩ năng
Số câu hỏi theo các mức độ Nội
cần kiểm tra, đánh giá nhận thức dung Đơn vị TT Vận Tổng kiến kiến thức Nhận Thông Vận dụng thức biết hiểu dụng cao 1 Phản
Số oxi hóa Nhận biết: 1 1 2 ứng oxi
- Khái niệm số oxi hoá; quy tắc xác định hóa –
số oxi hoá của nguyên tử các nguyên tố khử
trong phân tử đơn chất và hợp chất. Thông hiểu:
- Xác định được số oxi hoá của nguyên tử
các nguyên tố trong một số hợp chất cụ thể.
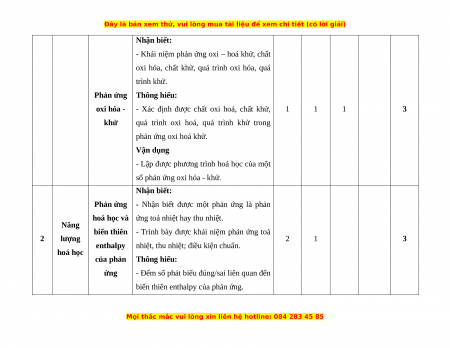
Nhận biết:
- Khái niệm phản ứng oxi – hoá khử, chất
oxi hóa, chất khử, quá trình oxi hóa, quá trình khử. Phản ứng Thông hiểu: oxi hóa -
- Xác định được chất oxi hoá, chất khử, 1 1 1 3 khử
quá trình oxi hoá, quá trình khử trong phản ứng oxi hoá khử. Vận dụng
- Lập được phương trình hoá học của một
số phản ứng oxi hóa - khử. Nhận biết: Phản ứng
- Nhận biết được một phản ứng là phản
hoá học và ứng toả nhiệt hay thu nhiệt. Năng
biến thiên - Trình bày được khái niệm phản ứng toả 2 lượng 2 1 3 enthalpy
nhiệt, thu nhiệt; điều kiện chuẩn. hoá học của phản Thông hiểu: ứng
- Đếm số phát biểu đúng/sai liên quan đến
biến thiên enthalpy của phản ứng.
Nhận biết:
- Nêu được ý nghĩa của dấu và giá trị .
Ý nghĩa và - Dựa vào biến thiên enthalpy của phản cách tính
ứng xác định phản ứng là toả nhiệt hay
biến thiên thu nhiệt. enthalpy Thông hiểu: 2 1 1 4 của phản
- Đếm số phát biểu đúng sai liên quan đến ứng hoá
ý nghĩa biến thiên enthalpy của phản ứng. học Vận dụng cao: - Tính được
của một phản ứng dựa
vào bảng số liệu năng lượng liên kết hoặc
nhiệt tạo thành cho sẵn.
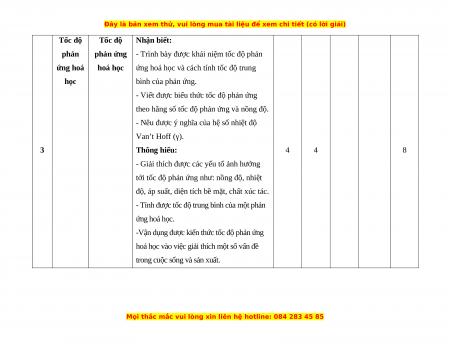
Tốc độ Tốc độ Nhận biết: phản phản ứng
- Trình bày được khái niệm tốc độ phản ứng hoá hoá học
ứng hoá học và cách tính tốc độ trung học bình của phản ứng.
- Viết được biểu thức tốc độ phản ứng
theo hằng số tốc độ phản ứng và nồng độ.
- Nêu được ý nghĩa của hệ số nhiệt độ Van’t Hoff (γ). 3 Thông hiểu: 4 4 8
- Giải thích được các yếu tố ảnh hưởng
tới tốc độ phản ứng như: nồng độ, nhiệt
độ, áp suất, diện tích bề mặt, chất xúc tác.
- Tính được tốc độ trung bình của một phản ứng hoá học.
-Vận dụng được kiến thức tốc độ phản ứng
hoá học vào việc giải thích một số vấn đề
trong cuộc sống và sản xuất.
Document Outline
- 0