Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t ế (có l i ờ gi i ả ) SỞ GIÁO D C Ụ VÀ ĐÀO T O Ạ KỲ THI CH N Ọ HSG C P Ấ T N Ỉ H LỚP 12 QU N Ả G NGÃI NĂM H C Ọ 2022-2023 Ngày thi: 09/02/2023 Đ Ề CHÍNH TH C Ứ Môn thi: Hóa h c ọ (H ệ THPT) (Đề có 03 trang)
Thời gian làm bài: 180 phút Câu 1. (2 đi m) ể
1.1. Anion X2- có c u ấ hình electron l p ớ ngoài cùng là 3p6. Vi t ế c u ấ hình electron
nguyên tử X và xác đ nh
ị v ịtrí (ô, chu kì, nhóm) c a
ủ X trong bảng tu n ầ hoàn các nguyên tố hoá h c ọ . 1.2. Tổng s ố hạt proton, n tr
ơ on, electron trong anion AB2 bằng 89 hạt, trong đó số hạt mang đi n ệ nhi u ề h n ơ số h t ạ không mang đi n ệ là 29 h t. ạ Vi t ế công th c ứ phân tử h p ợ chất tạo b i ở A, B. Câu 2. (2 đi m) ể 2.1. Vi t ế phư ng ơ trình ph n ả ng ứ (dư i ớ d ng
ạ phân tử và ion thu g n) ọ khi cho các dung dịch sau tác d ng u v i ớ nhau theo t il ệ mol 1 : 1. a) Ca(H2PO4)2 + KOH b) Ba(HCO3)2 + KHSO4
2.2. Cho 200 ml dung d c ị h A ch a
ứ HCl 1M và HNO3 2M tác d ng u v i ớ 300 ml dung dịch B ch a
ứ NaOH 0,8M và KOH aM, thu đư c ợ dung d c ị h C. Trung hòa h t ế 200 ml
dung dịch C cần 120 ml dung dịch HCl 1M. Tính a? Câu 3. (2 đi m) ể 3.1. S c u m t ộ lư ng ợ v a
ừ đủ khí H2S vào dung d c ị h FeCl3, thu đư c ợ m t ộ k t ế t a ủ
màu vàng A và dung d c
ị h X. Thêm từ từ đ n ế dư dung d c
ị h AgNO3 vào X, thu đư c ợ khí NO, k t ế t a ủ B và dung d c ị h Y. Cho dung d c ị h NaOH đ n ế d ư vào dung d c ị h Y, thu đư c ợ k t ế t a ủ C và dung d c ị h Z. Xác đ nh ị thành ph n ầ c a
ủ A, B, C, X, Y, Z và vi t ế các phư ng ơ trình phản ứng xảy ra. 3.2. Thêm m t ộ cách c n ẩ th n ậ 0,5 gam ch t ấ r n
ắ A vào 100 ml dung d c ị h HCl 0,2M, phản ứng xong, thu đư c ợ dung d c
ị h T và 0,28 lít khí H2 thoát ra (ở đktc). Xác đ nh ị A. Câu 4. (2 đi m) ể 4.1. Cho 29,6 gam h n ỗ h p
ợ X gồm Cu và Fe3O4 tan h t ế vào dung d c ị h ch a ứ H2SO4 loãng (d ) ư . Sau ph n ả ng ứ , thu đư c ợ dung d c ị h X ch a ứ hai mu i ố và axit d . ư Vi t ế phư ng ơ
trình phản ứng xảy ra và tính % kh i ố lư ng ợ c a ủ Cu trong X.
4.2. Cho m gam hỗn h p
ợ T gồm Al, Mg và Al2O3 phản ng ứ h t ế v i ớ 610 ml dung dịch HNO3 1M, thu đư c ợ dung d c
ị h T1 và 0,672 lít (ở đktc) h n ỗ h p ợ khí X có kh i ố lư ng ợ 1,18 gam g m
ồ hai khí không màu, có m t
ộ khí hóa nâu trong không khí. Cô c n ạ
dung dịch T1, thu đư c ợ ch t ấ r n
ắ T2, nung T2 đ n ế khối lư ng ợ không đ i ổ đư c ợ (m + 1,84) gam ch t ấ r n
ắ T3. Mặt khác, để tác d ng u t i ố đa v i ớ các ch t ấ trong dung d c ị h T1 cần v a ừ đủ 665 ml dung d c ị h KOH 1M, thu đư c ợ 5,8 gam k t ế t a ủ Y. Tính ph n ầ trăm khối lư ng ợ của Al trong hỗn h p ợ T ban đầu. Câu 5. (2 đi m) ể M i ọ thắc m c
ắ vui lòng xin liên h h
ệ otline: 084 283 45 85
Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t ế (có l i ờ gi i ả ) 5.1. Xác đ nh ị các ch t ấ A, B, D, F và vi t ế các phư ng ơ trình hóa h c ọ để hoàn thành s ơ đồ bi n ế hóa sau: (1) (2) (3) (4) (5) Al 4C3 A B D F TNT. 5.2. Đ t
ố cháy hoàn toàn hiđrocacbon X, thu đư c ợ t il ệ s ố mol H2O và CO2 tư n ơ g n ứ g b n ằ g 1,125. a) Xác đ n ị h công th c ứ phân t ử c a ủ X. b) X1 là đ n ồ g phân c a ủ X, khi tác d n u g v i ớ Cl2 trong đi u ề ki n ệ thích h p ợ v i ớ ti lệ mol 1:1 thu đư c ợ m t ộ d n ẫ xu t ấ mono clo duy nh t ấ (X2). G i
ọ tên X1, X2 và vi t ế phư n ơ g trình ph n ả n ứ g x y ả ra. Câu 6. (2 đi m) ể 6.1. Giải thích ng n ắ g n, ọ tại sao các ancol đ u ầ dãy đ ng ồ đ ng ẳ tan t t ố trong nư c ớ và có nhi t ệ đ ộ sôi cao h n ơ so v i ớ các hiđrocacbon tư ng ơ ng ứ ?
6.2. Đốt cháy hoàn toàn 7,44 gam ancol m c
ạ h hở A, thu đư c
ợ 2V lít CO2 (ở đktc).
Mặt khác, cho 7,44 gam A vào bình ch a ứ Na d , ư sau ph n ả ng ứ thu đư c ợ V lít H2 ( ở đktc) và th y ấ kh i ố lư ng ợ bình đ ng
ự natri tăng 7,2 gam. Từ A tách nư c ớ ở 170 0C có mặt H2SO4 đặc, thu đư c ợ ch t ấ h u
ữ cơ B. Oxi hóa A bằng CuO d , ư đun nóng, thu đư c ợ chất h u ữ cơ C, ti p ế t c
u oxi hóa C bằng nư c ớ brom, thu đư c ợ ch t ấ h u ữ cơ D. Xác đ nh ị công th c ứ c u ấ t o ạ và g i ọ tên các ch t
ấ A, B, C, D. 6.3. Hỗn h p ợ T gồm hai ch t ấ h u ữ cơ m c ạ h hở (đ u ề ch a ứ C, H, O) trong phân tử mỗi ch t ấ đ u ề có hai nhóm ch c ứ trong s
ố các nhóm: –CHO, -CH2OH, -COOH. Đ t ố cháy
hoàn toàn 17,1 gam T thu đư c
ợ 11,2 lít CO2 (ở đktc) và m gam H2O. N u ế cho 17,1 gam T tác d ng u h t ế v i ớ Na dư thì thu đư c
ợ 2,8 lít H2 (ở đktc). M t
ặ khác 17,1 gam T phản ứng hoàn toàn v i ớ lư ng ợ dư dung d c
ị h AgNO3 trong NH3, thu đư c ợ 54 gam Ag. Xác định công th c ứ c u ấ t o ạ c a ủ hai ch t
ấ đã cho và tính giá tr ịc a ủ m. Câu 7. (2 đi m) ể
7.1. Thủy phân 7,2 gam vinyl fomat trong môi trư ng ờ axit H2SO4 loãng v i ớ hi u ệ suất phản ng ứ là 60%, thu đư c ợ dung d c
ị h A. Trung hòa các axit trong A bằng NaOH rồi cho h n ỗ h p ợ thu đư c ợ vào lư ng ợ dư dung d c
ị h AgNO3 trong NH3, đun nóng. Vi t ế các phư ng ơ trình ph n ả ng ứ đã x y ả ra và tính kh i ố lư ng ợ Ag thu đư c ợ . 7.2. Cho s ơ đồ các ph n ả ng ứ theo đúng t i l ệ mol: o (1) E + 3NaOH t
X + 2Y + Z (2) 2Y + H 2SO4 Na2SO4 + 2T (3) 2X + H 2SO4 Na2SO4 + 2R Bi t ế E là este no, m c ạ h h ở có công th c ứ phân t
ử CnH8On. T là axit cacboxylic, Z là ancol đa ch c ứ . L p ậ lu n ậ xác đ nh ị công th c ứ c u ấ t o ạ c a
ủ E, X, Y, Z, T, R. 7.3. Hỗn h p ợ T gồm glucoz , ơ saccarozơ và xenluloz . ơ Đ t ố m gam h n ỗ h p ợ T cần
V lít O2 (ở đktc), thu đư c ợ t ng ổ kh i ố lư ng
ợ CO2 và H2O là (2m +1,212) gam. M t ặ khác, đun nóng m gam h n ỗ h p ợ T v i ớ dung d c ị h H2SO4 cho đ n ế khi ph n ả ng ứ x y ả ra hoàn toàn, trung hoà dung d c ị h sau ph n ả ng ứ r i ồ cho tác d ng u v i ớ dung d c ị h AgNO3 trong
NH3 dư (đun nóng), thu đư c
ợ (3m -16,524) gam k t ế t a ủ . Tính giá tr ịc a ủ V và m. Câu 8. (2 đi m) ể M i ọ thắc m c
ắ vui lòng xin liên h h
ệ otline: 084 283 45 85
Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t ế (có l i ờ gi i ả ) 8.1. Khi th y
ủ phân hoàn toàn 43,40 gam m t ộ peptit X (m c ạ h h ) ở thu đư c ợ 35,60 gam
alanin và 15,00 gam glyxin. Vi t ế công th c ứ c u ấ t o ạ có th ể có c a ủ X. 8.2. Hỗn h p
ợ E gồm metyl aminoaxetat và m t
ộ -amino axit X có d ng ạ
H2NR(COOH)2. Cho m gam E tác d ng u v a ừ đủ v i ớ dung d c ị h NaOH, đun nóng, thu đư c ợ dung d c ị h Y ch a
ứ (m+6) gam mu i. ố Dung d c ị h Y tác d ng u t i ố đa v i ớ dung d c ị h chứa 0,7 mol HCl, thu đư c ợ dung d c ị h Z ch a ứ 64,05 gam mu i.
ố Tính m và xác đ nh ị công th c ứ c u ấ t o ạ c a ủ X. Câu 9. (2 đi m) ể 9.1. Có m t ộ dung d c ị h h n ỗ h p
ợ anilin và phenol trong ancol etylic. Mu n ố trung hoà 10 gam dung d c ị h đó c n ầ 49,02 ml dung d c
ị h KOH 2,24% (D = 1,02g/ml). N u ế l y ấ lư ng ợ gấp đôi dung d c ị h đó tác d ng u v i ớ nư c ớ brom d , ư thu đư c ợ 31,06 gam k t ế t a ủ . Tính nồng đ ộ phần trăm c a
ủ anilin và phenol trong dung d c ị h trên?
9.2. Đốt cháy hoàn toàn m gam h n ỗ h p
ợ X gồm andehit malonic (OHC-CH2-CHO), andehit acrylic và m t ộ este đ n ơ ch c ứ mạch hở c n
ầ dùng 3192 ml O2 (ở đktc) và thu đư c
ợ 3024 ml CO2 (ở đktc) và 1,62 gam H2O. M t
ặ khác, m gam X tác d ng u v a ừ đủ v i ớ 150 ml dung d c ị h NaOH 0,15M, thu đư c ợ dung d c ị h Y (giả thi t ế chi xảy ra phản
ứng xà phòng hóa). Cho Y tác dung v i ớ lư ng ợ dư dung d c ị h AgNO3 trong NH3, đun nóng, thu đư c
ợ a gam Ag. Tính giá trị của m, a. Câu 10. (2 đi m) ể 10.1. Có hai l , ọ m i ỗ l ọ ch ich a ứ riêng bi t ệ t ng ừ dung d c
ị h: NaOH, AlCl3. Trình bày thao tác thí nghi m ệ nhanh g n ọ để nh n ậ bi t ế đư c ợ m i ỗ lọ ch a ứ dung d c ị h nào? (không đư c ợ dùng thêm thu c ố th ử nào khác).
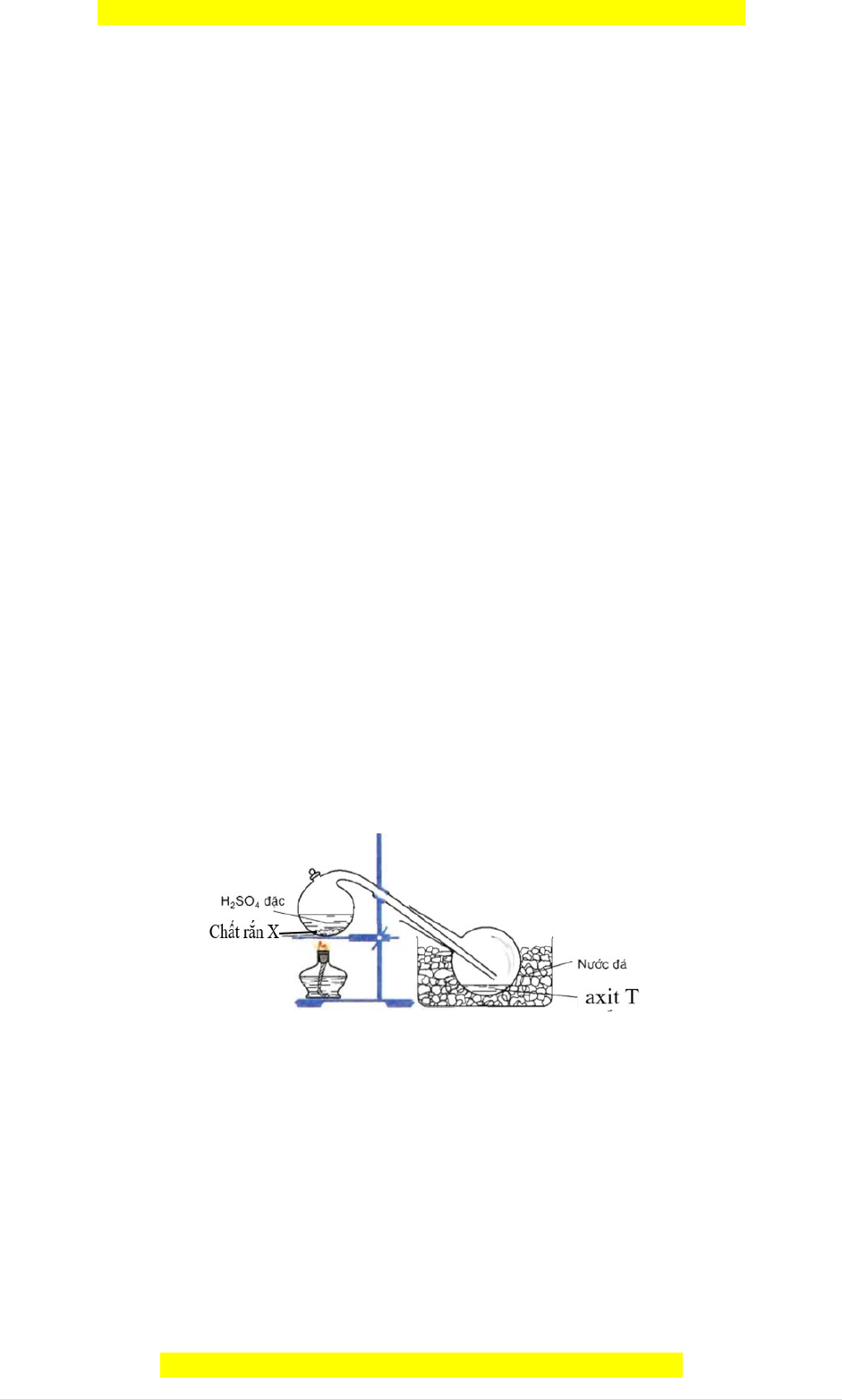
10.2. Hình vẽ mô tả thí nghiệm điều chế axit T theo phư ng ơ pháp sunfat trong phòng thí nghi m ệ nh ư sau: a) Ch n ọ ch t ấ r n ắ X thích h p ợ để đi u ề chế đư c
ợ 2 axit T khác nhau, vi t ế các phư ng ơ trình hóa h c ọ xảy ra. b) Có thể ch n ọ r n
ắ X là NaBr, NaI để đi u ề chế axit HBr, HI đư c ợ không? gi i ả thích. -----------H T Ế -----------
Ghi chú: Cán b
ộ coi thi không gi i ả thích gì thêm. M i ọ thắc m c
ắ vui lòng xin liên h h
ệ otline: 084 283 45 85
Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t ế (có l i ờ gi i ả ) SỞ GIÁO D C Ụ VÀ ĐÀO T O Ạ KỲ THI CH N Ọ HSG C P Ấ T N Ỉ H L P Ớ 12 QU N Ả G NGÃI NĂM HỌC 2022-2023 Ngày thi: 09/02/2023 HDC Đ Ề CHÍNH TH C Ứ Môn thi: Hóa h c ọ (Hệ THPT) (HDC có 09 trang) Th i ờ gian làm bài: 180 phút Câu 1. (2 đi m) ể
1.1. Anion X2- có c u ấ hình electron l p ớ ngoài cùng là 3p6. Vi t ế c u ấ hình electron
nguyên tử X và xác đ nh
ị v ịtrí (ô, chu kì, nhóm) c a
ủ X trong bảng tu n ầ hoàn các nguyên tố hoá h c ọ . 1.2. Tổng s ố hạt proton, n tr
ơ on, electron trong anion AB2 bằng 89 hạt, trong đó số hạt mang đi n ệ nhi u ề h n ơ số h t ạ không mang đi n ệ là 29 h t. ạ Vi t ế công th c ứ phân tử h p ợ chất tạo b i ở A, B. Câ Nộ Điể i dung u m 1 2,0 1.1 1,0 - C u ấ hình electron c a ủ X: 1s22s22p63s23p4 0,5 - Vị trí c a
ủ X: Ô 16; chu kì 3, nhóm VIA 0,5 1.2 1,0
- Ta có: 2ZA + NA + 2(2ZB + NB) +1 = 89 (1) 2Z 0,5
A + 4ZB + 1 - (NA + 2NB) = 29 (2)------------------------ T
ừ (1) và (2) suy ra:ZA + 2ZB = 29 - Ch n ọ nghi m ệ thích h p
ợ : ZB =8 , ZA = 13 A: Al; B: O ------------ 0,25 - CTPT tạo b i
ở A,B là: Al2O3------------------------------------------------- 0,25 Câu 2. (2 đi m) ể 2.1. Vi t ế phư ng ơ trình ph n ả ng ứ (dư i ớ d ng
ạ phân tử và ion thu g n) ọ khi cho các dung dịch sau tác d ng u v i ớ nhau theo t il ệ mol 1 : 1. a) Ca(H2PO4)2 + KOH b) Ba(HCO3)2 + KHSO4 M i ọ thắc m c
ắ vui lòng xin liên h h
ệ otline: 084 283 45 85
Đề HSG Hóa 12 Quảng Ngãi năm 2023 có đáp án
2.8 K
1.4 K lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Tài liệu được cập nhật liên tục trong gói này từ nay đến hết tháng 3/2024. Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Tailieugiaovien.com.vn giới thiệu Đề HSG Hóa 12 Quảng Ngãi năm 2023 có đáp án.
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(2843 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN Hóa Học
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Lớp 12
Xem thêmTài liệu bộ mới nhất

Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có l i gi i)ả ử ệ ể ế ờ ả
S GIÁO D C VÀ ĐÀOỞ Ụ T OẠ
QU NG NGÃIẢ
(Đề có 03 trang)
KỲ THI CH N Ọ HSG C P T NH L P 1Ấ Ỉ Ớ 2
NĂM H C 202Ọ 2-2023
Ngày thi: 09/02/2023
Môn thi: Hóa h cọ (H THPT)ệ
Th i gianờ làm bài: 180 phút
Câu 1. (2 đi m)ể
1.1. Anion X
2-
có c u hình electron l p ngoài cùng là 3pấ ớ
6
. Vi t c u hình electronế ấ
nguyên t ử X và xác đ nh v trí (ô, chu kì, nhóm) c a ị ị ủ X trong b ng tu n hoàn các nguyênả ầ
t hoá h c.ố ọ
1.2. T ng s h t proton, n tron, electron trong anion ổ ố ạ ơ
2
AB
b ng 89 h t, trong đó sằ ạ ố
h t mang đi n nhi u h n s h t khạ ệ ề ơ ố ạ ông mang đi n là 29 h t.ệ ạ Vi t ế công th c phân tứ ử
h p ch tợ ấ t o b i ạ ở A, B.
Câu 2. (2 đi m)ể
2.1. Vi t ph ng trình ph n ng (d i d ng phân t và ion thu g n) khi cho cácế ươ ả ứ ướ ạ ử ọ
dung d ch sau tác d ng v i nhau theo t l mol 1 : 1.ị u ớ i ệ
a) Ca(H
2
PO
4
)
2
+ KOH
b) Ba(HCO
3
)
2
+ KHSO
4
2.2. Cho 200 ml dung d ch ị A ch a HCl 1M và HNOứ
3
2M tác d ng v i 300 ml dungu ớ
d ch ị B ch a NaOH 0,8M và KOH ứ aM, thu đ c dung d ch ượ ị C. Trung hòa h t 200 mlế
dung d ch ị C c n 120 ml dung d ch HCl 1M. Tính ầ ị a?
Câu 3. (2 đi m)ể
3.1. S c m t l ng v a đ khí Hu ộ ượ ừ ủ
2
S vào dung d ch FeClị
3
, thu đ c m t k t t aượ ộ ế ủ
màu vàng A và dung d ch ị X. Thêm t t đ n d dung d ch AgNOừ ừ ế ư ị
3
vào X, thu đ c khíượ
NO, k t t a ế ủ B và dung d ch ị Y. Cho dung d ch NaOH đ n d vào dung d ch ị ế ư ị Y, thu đ cượ
k t t a ế ủ C và dung d ch ị Z. Xác đ nh thành ph n c a ị ầ ủ A, B, C, X, Y, Z và vi t cácế
ph ng trình ph n ng x y ra.ươ ả ứ ả
3.2. Thêm m t cách c n th n 0,5 gam ch t r n ộ ẩ ậ ấ ắ A vào 100 ml dung d ch HCl 0,2M,ị
ph n ng xong, thu đ c dung d ch ả ứ ượ ị T và 0,28 lít khí H
2
thoát ra ( đktc). Xác đ nh ở ị A.
Câu 4. (2 đi m)ể
4.1. Cho 29,6 gam h n h p ỗ ợ X g m Cu và Feồ
3
O
4
tan h t vào dung d ch ch a Hế ị ứ
2
SO
4
loãng (d ). Sau ph n ng, thu đ c dung d ch ư ả ứ ượ ị X ch a hai mu i và axit d . Vi tứ ố ư ế
ph ng trình ph n ng x y ra và tính % kh i l ng c a Cu trong ươ ả ứ ả ố ượ ủ X.
4.2. Cho m gam h n h p ỗ ợ T g m Al, Mg và Alồ
2
O
3
ph n ng h t v i 610 ml dungả ứ ế ớ
d ch HNOị
3
1M, thu đ c dung d ch ượ ị T
1
và 0,672 lít ( đktc) h n h p khí ở ỗ ợ X có kh iố
l ng 1,18 gam g m hai khí không màu, có m t khí hóa nâu trong không khí. Cô c nượ ồ ộ ạ
dung d ch ị T
1
, thu đ c ch t r n ượ ấ ắ T
2
, nung T
2
đ n kh i l ng không đ i đ c (ế ố ượ ổ ượ m +
1,84) gam ch t r n ấ ắ T
3
. M t khác, đ tác d ng t i đa v i các ch t trong dung d ch ặ ể u ố ớ ấ ị T
1
c n v a đ 665 ml dung d ch KOH 1M, thu đ c 5,8 gam k t t a ầ ừ ủ ị ượ ế ủ Y. Tính ph n trămầ
kh i l ng c a Al trong h n h p ố ượ ủ ỗ ợ T ban đ u.ầ
Câu 5. (2 đi m)ể
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ
Đ CHÍNH TH CỀ Ứ

Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có l i gi i)ả ử ệ ể ế ờ ả
5.1. Xác đ nh các ch t ị ấ A, B, D, F và vi t các ph ng trình hóa h c đ hoàn thànhế ươ ọ ể
s đ bi n hóa sau: ơ ồ ế
Al
4
C
3
(1)
A
(2)
B
(3)
D
(4)
F
(5)
TNT.
5.2. Đ t cháy hoàn toàn hiđrocacbon ố X, thu đ c t l s mol Hượ i ệ ố
2
O và CO
2
t ng ngươ ứ
b ng 1,125.ằ
a) Xác đ nh công th c phân t c a ị ứ ử ủ X.
b) X
1
là đ ng phân c a ồ ủ X, khi tác d ng v i Clu ớ
2
trong đi u ki n thích h pề ệ ợ v i t lớ i ệ
mol 1:1 thu đ c m t d n xu t mono clo duy nh t (ượ ộ ẫ ấ ấ X
2
). G i tên ọ X
1
, X
2
và vi t ph ngế ươ
trình ph n ng x y ra.ả ứ ả
Câu 6. (2 đi m)ể
6.1. Gi i thích ng n g n, tả ắ ọ i sao các ancol đ u dãy đ ng đ ng tan t t trong n cạ ầ ồ ẳ ố ướ
và có nhi t đ sôi cao h n so v i các hiđrocacbon t ng ng?ệ ộ ơ ớ ươ ứ
6.2. Đ t cháy hoàn toàn 7,44 gam ancol m ch h ố ạ ở A, thu đ c ượ 2V lít CO
2
( đktc).ở
M t khác, cho 7,44 gam ặ A vào bình ch a Na d , sau ph n ng thu đ c ứ ư ả ứ ượ V lít H
2
( ở
đktc) và th y kh i l ng bình đ ng natri tăng 7,2 gam. T ấ ố ượ ự ừ A tách n c 170 ướ ở
0
C có
m t Hặ
2
SO
4
đ c, thu đ c ch t h u c ặ ượ ấ ữ ơ B. Oxi hóa A b ng CuO d , đun nóng, thu đ cằ ư ượ
ch t h u c ấ ữ ơ C, ti p t c oxi hóa ế u C b ng n c brom, thu đ c ch t h u c ằ ướ ượ ấ ữ ơ D. Xác đ nhị
công th c c u t o và g i tên các ch t ứ ấ ạ ọ ấ A, B, C, D.
6.3. H n h p ỗ ợ T g m hai ch t h u c m ch h (đ u ch a C, H, O) trong phân tồ ấ ữ ơ ạ ở ề ứ ử
m i ch t đ u có hai nhóm ch c trong s các nhóm: –CHO, -CHỗ ấ ề ứ ố
2
OH, -COOH. Đ t cháyố
hoàn toàn 17,1 gam T thu đ c 11,2 lít COượ
2
( đktc) và ở m gam H
2
O. N u cho 17,1 gamế
T tác d ng h t v i Na d thì thu đ c 2,8 lít Hu ế ớ ư ượ
2
( đktc). M t khác 17,1 gam ở ặ T ph nả
ng hoàn toàn v i l ng d dung d ch AgNOứ ớ ượ ư ị
3
trong NH
3
, thu đ c 54 gam Ag. Xácượ
đ nh công th c c u t o c a hai ch t đã cho và tính giá tr c a ị ứ ấ ạ ủ ấ ị ủ m.
Câu 7. (2 đi m)ể
7.1. Th y phân 7,2 gam vinyl fomat trong môi tr ng axit Hủ ườ
2
SO
4
loãng v i hi uớ ệ
su t ph n ng là 60%, thu đ c dung d ch ấ ả ứ ượ ị A. Trung hòa các axit trong A b ng NaOHằ
r i cho h n h p thu đ c vào l ng d dung d ch AgNOồ ỗ ợ ượ ượ ư ị
3
trong NH
3
, đun nóng. Vi tế
các ph ng trình ph n ng đã x y ra và tính kh i l ng Ag thu đ c.ươ ả ứ ả ố ượ ượ
7.2. Cho s đ các ph n ng theo đúng t l mol:ơ ồ ả ứ i ệ
(1) E + 3NaOH
o
t
X + 2Y + Z
(2) 2Y + H
2
SO
4
Na
2
SO
4
+ 2T
(3) 2X + H
2
SO
4
Na
2
SO
4
+ 2R
Bi t ế E là este no, m ch h có công th c phân t Cạ ở ứ ử
n
H
8
O
n
. T là axit cacboxylic, Z là ancol
đa ch c. L p lu n xác đ nh công th c c u t o c a ứ ậ ậ ị ứ ấ ạ ủ E, X, Y, Z, T, R.
7.3. H n h p ỗ ợ T g m glucoz , saccaroz và xenluloz . Đ t ồ ơ ơ ơ ố m gam h n h p ỗ ợ T c nầ
V lít O
2
( đktc), thu đ c t ng kh i l ng COở ượ ổ ố ượ
2
và H
2
O là (2m +1,212) gam. M t khác,ặ
đun nóng m gam h n h p ỗ ợ T v i dung d ch Hớ ị
2
SO
4
cho đ n khi ph n ng x y ra hoànế ả ứ ả
toàn, trung hoà dung d ch sau ph n ng r i cho tác d ng v i dung d ch AgNOị ả ứ ồ u ớ ị
3
trong
NH
3
d (đun nóng), thu đ c (3ư ượ m -16,524) gam k t t a. Tính giá tr c a ế ủ ị ủ V và m.
Câu 8. (2 đi m)ể
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ
Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có l i gi i)ả ử ệ ể ế ờ ả
8.1. Khi th y phân ủ hoàn toàn 43,40 gam m t peptit ộ X (m ch h ) thu đ c 35,60 gamạ ở ượ
alanin và 15,00 gam glyxin. Vi t công th c c u t o có th có c a ế ứ ấ ạ ể ủ X.
8.2. H n h p ỗ ợ E g m metyl aminoaxetat và m t ồ ộ
-amino axit X có d ngạ
H
2
NR(COOH)
2
. Cho m gam E tác d ng v a đ v i dung d ch NaOH, đun nóng, thuu ừ ủ ớ ị
đ c dung d ch ượ ị Y ch a (ứ m+6) gam mu i. Dung d ch ố ị Y tác d ng t i đa v i dung d chu ố ớ ị
ch a 0,7 mol HCl, thu đ c dung d ch ứ ượ ị Z ch a 64,05 gam mu i. Tính ứ ố m và xác đ nhị
công th c c u t o c a ứ ấ ạ ủ X.
Câu 9. (2 đi m)ể
9.1. Có m t dung d ch h n h p anilin và phenol trong ancol etylic. Mu n trung hoàộ ị ỗ ợ ố
10 gam dung d ch đó c n 49,02 ml dung d ch KOH 2,24% (D = 1,02g/ml). N u l yị ầ ị ế ấ
l ng g p đôi dung d ch đó tác d ng v i n c brom d , thu đ c 31,0ượ ấ ị u ớ ướ ư ượ 6 gam k t t a.ế ủ
Tính n ng đ ph n trăm c a anilin và phenol trong dung d ch trên? ồ ộ ầ ủ ị
9.2.
Đ t cháy ố hoàn toàn m gam h n h p ỗ ợ X g m andehitồ malonic (OHC-CH
2
-CHO),
andehit acrylic và m t ộ este đ n ơ ch c m chứ ạ h ở c n dùngầ 3192 ml O
2 ( đktc)ở và thu
đ c ượ 3024 ml CO2 ( đktc)ở và 1,62 gam H2O. M t khác,ặ m gam X tác d ng v a đu ừ ủ
v i 150 ml dung d ch ớ ị NaOH 0,15M, thu đ c dung d ch ượ ị Y (giả thi t ch ế i x y ả ra ph nả
ng ứ xà phòng hóa). Cho Y tác d ng v i l ng d dung d ch u ớ ượ ư ị AgNO3 trong NH3, đun
nóng, thu đ c ượ a gam Ag. Tính giá tr c aị ủ m, a.
Câu 10. (2 đi m)ể
10.1. Có hai l , m i l ch ch a riêng bi t t ng dung d ch: NaOH, AlClọ ỗ ọ i ứ ệ ừ ị
3
. Trình bày
thao tác thí nghi m nhanh g n đ nh n bi t đ c m i l ch a dung d ch nàoệ ọ ể ậ ế ượ ỗ ọ ứ ị ? (không
đ c dùng thêm thu c th nào khác).ượ ố ử
10.2.
Hình vẽ mô t thí nghiả ệm đi u ch axit ề ế T theo ph ng pháp sunfat trongươ
phòng thí nghi m nh sau:ệ ư
a) Ch n ch t r n ọ ấ ắ X thích h p đ đi u ch đ c 2 axit ợ ể ề ế ượ T khác nhau, vi t cácế
ph ng trình hóa h c x y ra.ươ ọ ả
b) Có th ch n r n ể ọ ắ X là NaBr, NaI đ đi u ch axit HBr, HI đ c không? gi iể ề ế ượ ả
thích.
-----------H T-----------Ế
Ghi chú: Cán b coi thi không gi i thích gì thêm.ộ ả
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ
Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có l i gi i)ả ử ệ ể ế ờ ả
S GIÁO D C VÀ ĐÀOỞ Ụ T OẠ
QU NG NGÃIẢ
(HDC có 09 trang)
KỲ THI CH N Ọ HSG C P T NH L P 1Ấ Ỉ Ớ 2
NĂM H C 202Ọ 2-2023
Ngày thi: 09/02/2023
Môn thi: Hóa h cọ (H THPT)ệ
Th i gianờ làm bài: 180 phút
Câu 1. (2 đi m)ể
1.1. Anion X
2-
có c u hình electron l p ngoài cùng là 3pấ ớ
6
. Vi t c u hình electronế ấ
nguyên t ử X và xác đ nh v trí (ô, chu kì, nhóm) c a ị ị ủ X trong b ng tu n hoàn các nguyênả ầ
t hoá h c.ố ọ
1.2. T ng s h t proton, n tron, electron trong anion ổ ố ạ ơ
2
AB
b ng 89 h t, trong đó sằ ạ ố
h t mang đi n nhi u h n s h t khạ ệ ề ơ ố ạ ông mang đi n là 29 h t.ệ ạ Vi t ế công th c phân tứ ử
h p ch tợ ấ t o b i ạ ở A, B.
Câ
u
N i dungộ
Điể
m
1 2,0
1.1 1,0
- C u hình electron c a X: 1sấ ủ
2
2s
2
2p
6
3s
2
3p
4
- V trí c a X: Ô 16; chu kì 3, nhóm VIAị ủ
0,5
0,5
1.2 1,0
- Ta có: 2Z
A
+ N
A
+ 2(2Z
B
+ N
B
) +1 = 89 (1)
2Z
A
+ 4Z
B
+ 1 - (N
A
+ 2N
B
) = 29 (2)------------------------
T (1) và (2) suy ra:Zừ
A
+ 2Z
B
= 29
- Ch n nghi m thích h p : Zọ ệ ợ
B
=8 , Z
A
= 13 A: Al; B: O ------------
- CTPT t o b i A,B là: Alạ ở
2
O
3
-------------------------------------------------
0,5
0,25
0,25
Câu 2. (2 đi m)ể
2.1. Vi t ph ng trình ph n ng (d i d ng phân t và ion thu g n) khi cho cácế ươ ả ứ ướ ạ ử ọ
dung d ch sau tác d ng v i nhau theo t l mol 1 : 1.ị u ớ i ệ
a) Ca(H
2
PO
4
)
2
+ KOH
b) Ba(HCO
3
)
2
+ KHSO
4
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ
HDC Đ CHÍNH TH CỀ Ứ

Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có l i gi i)ả ử ệ ể ế ờ ả
2.2. Cho 200 ml dung d ch ị A ch a HCl 1M và HNOứ
3
2M tác d ng v i 300 ml dungu ớ
d ch ị B ch a NaOH 0,8M và KOH ứ aM thu đ c dung d ch ượ ị C. Trung hòa 200 ml dung
d ch ị C c n 120 ml dung d ch HCl 1M. Tính ầ ị a?
Câu N i dungộ Đi mể
2 2,0
2.1 1,0
a)
Ca(H
2
PO
4
)
2
+ KOH
→
CaHPO
4
↓
+ KH
2
PO
4
+ H
2
O
Ca
2+
+ H
2
PO
4
-
+ OH
-
→
CaHPO
4
↓
+ H
2
O
-----------------------------
b)
Ba(HCO
3
)
2
+ KHSO
4
→
BaSO
4
↓
+ KHCO
3
+ CO
2
↑
+
H
2
O
Ba
2+
+ HCO
3
-
+ H
+
+ SO
4
2-
→
BaSO
4
↓
+ CO
2
↑
+
H
2
O--------
(hs vi t d ng HSOế ạ
4
-
v n ch p nh n đúng)ẫ ấ ậ
0,5
0,5
2.2 1,0
- H
+
+ OH
-
→
H
2
O
( ) ( )
0,6 ; (0,24 0,3 )
H A OH B
n mol n a mol
→
( )OH C
n
d = 0,3a – 0,36 ư
- Trong 200ml dung d ch C: ị
( )OH C
n
d = ư
H
n
= 0,12 mol
→
OH
n
(500ml C) = 0,3mol → 0,3a – 0,36 = 0,3→ a = 2,2
0,25
0,25
0,25
0,25
Câu 3. (2 đi m)ể
3.1. S c m t l ng v a đ khí Hu ộ ượ ừ ủ
2
S vào dung d ch FeClị
3
, thu đ c m t k t t aượ ộ ế ủ
màu vàng A và dung d ch ị X. Thêm t t đ n d dung d ch AgNOừ ừ ế ư ị
3
vào X, thu đ c khíượ
NO, k t t a ế ủ B và dung d ch ị Y. Cho dung d ch NaOH đ n d vào dung d ch ị ế ư ị Y, thu đ cượ
k t t a ế ủ C và dung d ch ị Z. Xác đ nh thành ph n c a ị ầ ủ A, B, C, X, Y, Z và vi t cácế
ph ng trình ph n ng x y ra.ươ ả ứ ả
3.2. Thêm m t cách c n th n 0,5 gam ch t r n ộ ẩ ậ ấ ắ A vào 100 ml dung d ch HCl 0,2M,ị
ph n ng xong, thu đ c dung d ch ả ứ ượ ị T và 0,28 lít khí H
2
thoát ra ( đktc). Xác đ nh ở ị A.
Câu N i dungộ Đi mể
3 2,0
3.1. 1,0
- H
2
S + 2FeCl
3
→ 2FeCl
2
+ S↓ + 2HCl
=> A là S, X ch a FeClứ
2
và HCl có mol b ng nhau. -------------------------ằ
- AgNO
3
+ X:
FeCl
2
+ 2AgNO
3
→ 2AgCl↓ + Fe(NO
3
)
2
HCl + AgNO
3
→ AgCl↓ + HNO
3
(mol Fe(NO
3
)
2
= mol HNO
3
)
3Fe(NO
3
)
2
+ 4HNO
3
→3 Fe(NO
3
)
3
+ NO + 2H
2
O --------------------------
Fe(NO
3
)
2(d )ư
+ AgNO
3
→ Fe(NO
3
)
3
+ Ag↓
0,25
0,25
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ