SỞ GIÁO DỤC VÀ ĐÀO TẠO ĐỀ THI TUYỂN SINH VÀO LỚP 10 THPT ĐĂK LĂK NĂM HỌC 2023 ĐỀ CHÍNH THỨC
MÔN: HÓA HỌC - CHUYÊN
Thời gian làm bài: 150 phút
Cho biết nguyên tử khối của các nguyên tố: H = 1; C = 12; O = 16; Na = 23; Mg =
24; Al = 27; Ca = 40; Fe = 56; Cu = 64; Zn = 65; Br = 80; Sr = 88; Ba = 137.
Các thể tích khí đều đo ở điều kiện tiêu chuẩn; giả thiết các khí sinh ra không tan trong nước. Câu 1. (2,0 điểm)
1. Viết các phương trình hóa học của các phản ứng xảy ra khi:
a. Sục từ từ khí CO2 đến dư vào dung dịch nước vôi trong.
b. Cho KHCO3 rắn vào dung dịch H2SO4 đặc dư.
c. Cho oxit Fe3O4 tác dụng với dung dịch HCl dư. d. Đốt cháy than gỗ.
2. Hoàn thành các sơ đồ phản ứng sau đây:
(X1) + H2SO4 → (X2) + SO2↑ + H2O (1) (X3) + KOH → (X2) + (X4) (2)
(X5) + KOH → (X2) + (X6) + H2O (3)
Biết M(X1) = M(X3) = M(X5) = 120 g/mol. Câu 2. (1,5 điểm)
1. Hình vẽ sau đây mô tả thí nghiệm điều chế khí Cl2 trong phòng thí nghiệm: B E D
a. Hãy chọn các hóa chất A, B, D, E phù hợp và viết phương trình hóa học điều chế khí Cl2.
b. Cho biết vai trò của bình (1), bình (2) trong quá trình điều chế trên.
2. Trình bày phương pháp hóa học để làm sạch khí CO2 có lẫn tạp chất SO2. Câu 3 (2,0 điểm)
1. Nung hỗn hợp X gồm a gam Al và 24 gam Fe2O3 trong điều kiện không có không
khí, sau phản ứng thu được hỗn hợp chất rắn Y. Cho Y tác dụng với 500 ml dung
dịch NaOH bM thu được 6,72 lít khí H2, chất rắn không tan Z và dung dịch T gồm 2
chất tan có cùng nồng độ mol. Biết các phản ứng xảy ra hoàn toàn. Tìm giá trị của a và b.
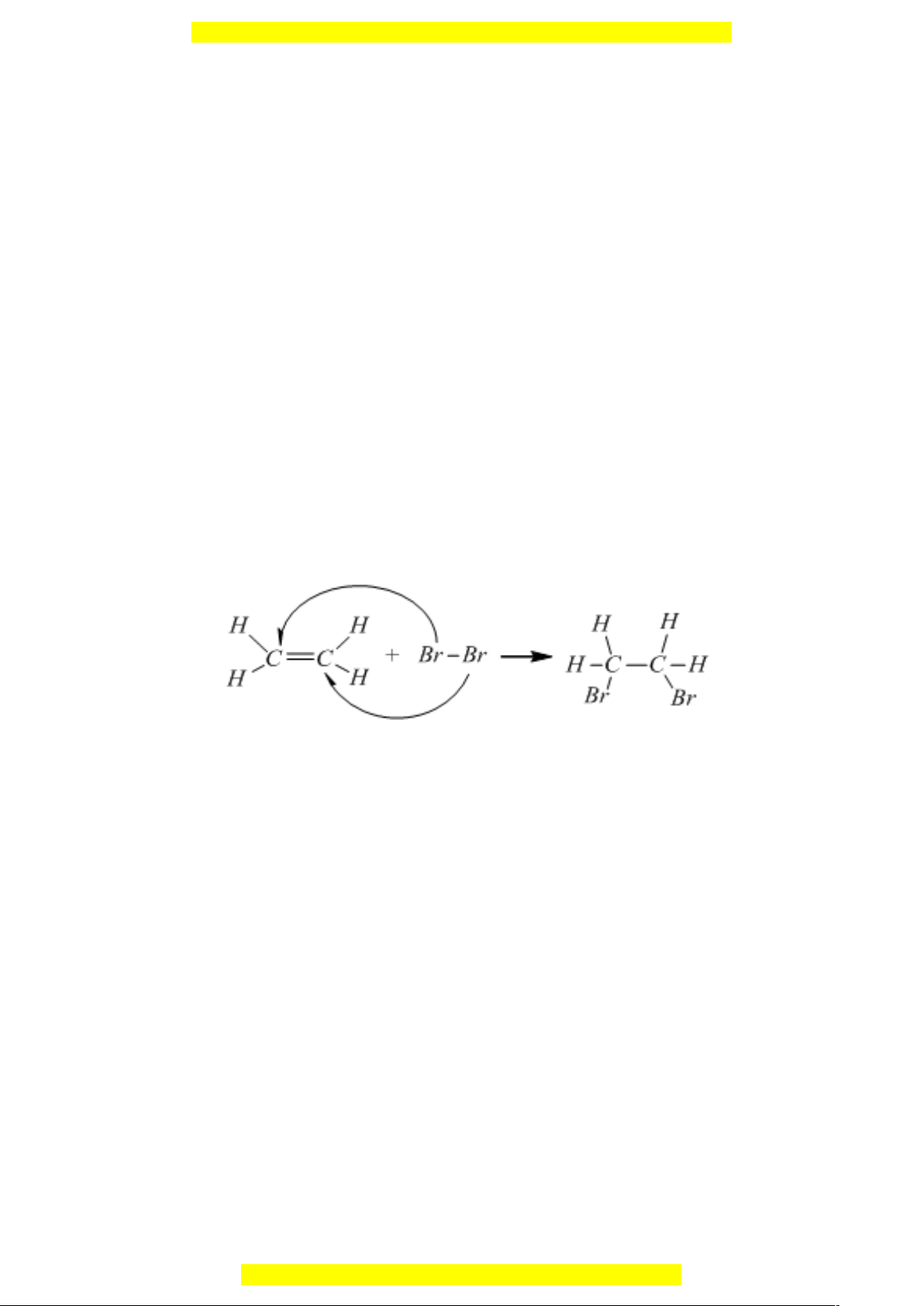
2. Etilen và các chất tương tự etilen có chứa 1 liên kết đôi trong phân tử nên dễ tham
gia phản ứng cộng. Phản ứng cộng với brom, liên kết kém bền trong liên kết đôi bị
đứt ra và mỗi phân tử etilen đã kết hợp thêm một phân tử brom:
Dẫn khí P (có công thức phân tử C4H8, chứa liên kết đôi tương tự etilen) đi qua dung
dịch brom màu da cam, sau phản ứng thấy dung dịch brom bị mất màu và thu được
sản phẩm hữu cơ Q (C4H8Br2). Viết công thức cấu tạo có thể có của Q. Câu 4 (2,5 điểm)
1. Cho G, I và K là các hợp chất no, mạch hở có công thức đơn giản nhất là C2H3O2.
Biết các chất trên chỉ chứa nhóm chức phản ứng được với dung dịch NaOH (đun nóng).
a. Xác định công thức phân tử của G, I, K.
b. Viết công thức cấu tạo có thể có của G, I và K. Biết G, I và K tham gia các phản
ứng theo đúng tỉ lệ mol như sau:
(G) + 2NaHCO3 → (G1) + 2CO2↑ + 2H2O (I) + 2NaOH → (I1) + 2CH3OH
(K) + 2NaOH → (I1) + (K1) + H2O
2. Hỗn hợp T gồm 2 chất hữu cơ U (RCOOH) và V (R’(OH)2), trong đó R, R’ là các
gốc hiđrocacbon mạch hở. Lấy 0,05 mol hỗn hợp T tác dụng với Na dư thấy giải
phóng 0,896 lít khí. Mặt khác, đốt cháy hoàn toàn 0,25 mol hỗn hợp T, sau phản ứng
thu được 15,68 lít CO2 và 13,5 gam H2O. Tìm công thức phân tử và viết công thức cấu tạo của U và V. Câu 5 (2,0 điểm)
1. Khoáng chất X có công thức dạng MCO3.M(OH)2.nH2O (M là kim loại có hóa trị
không đổi, n là số nguyên và n ≤ 10). Nung 19,2 gam X đến khối lượng không đổi
thu được 8,0 gam chất rắn MO và hỗn hợp Y (gồm khí và hơi).
a. Xác định công thức của khoáng chất X.
b. Dẫn toàn bộ hỗn hợp Y vào 100 ml dung dịch Z gồm NaOH 1M và Ba(OH)2 0,3M
đến khi phản ứng hoàn toàn thu được m1 gam kết tủa, khối lượng dung dịch tăng lên
so với ban đầu là m2 gam. Tính m1, m2.
2. Dẫn hỗn hợp khí A gồm 2 hidrocacbon mạch hở N (CnH2n+2) và M (CmH2m+2-2k) vào
bình đựng 250 ml dung dịch Br2 1M, chỉ xảy ra phản ứng:
CmH2m+2-2k + kBr2 → CmH2m+2-2kBr2k
Sau phản ứng hoàn toàn thấy khối lượng bình brom tăng lên 7,0 gam, đồng thời có
14,6 gam khí thoát ra khỏi bình. Đốt cháy hoàn toàn khí thoát ra thu được 21,952 lít CO2.
a. Xác định công thức phân tử của N và M.
b. Tính thành phần phần trăm về thể tích của các khí trong hỗn hợp A. ---------Hết---------
Ghi chú: Thí sinh không được sử dụng tài liệu. Cán bộ coi thi không giải thích gì thêm.
Họ và tên thí sinh: …………………………….
Số báo danh: ……………………………………
Chữ kí cán bộ coi thi 1: ……………………….
Chữ kí cán bộ coi thi 2: …………………………
SỞ GIÁO DỤC VÀ ĐÀO TẠO
HƯỚNG DẪN GIẢI ĐỀ THI VÀO LỚP 10 ĐĂK LĂK
NĂM HỌC 2022 – 2023
MÔN: HÓA HỌC - CHUYÊN Câu 1. (2,0 điểm)
1. Viết các phương trình hóa học của các phản ứng xảy ra khi:
a. Sục từ từ khí CO2 đến dư vào dung dịch nước vôi trong.
b. Cho KHCO3 rắn vào dung dịch H2SO4 đặc dư.
c. Cho oxit Fe3O4 tác dụng với dung dịch HCl dư. d. Đốt cháy than gỗ.
2. Hoàn thành các sơ đồ phản ứng sau đây:
(X1) + H2SO4 → (X2) + SO2↑ + H2O (1) (X3) + KOH → (X2) + (X4) (2)
(X5) + KOH → (X2) + (X6) + H2O (3)
Biết M(X1) = M(X3) = M(X5) = 120 g/mol. Hướng dẫn giải 1.1.
Các phương trình hóa học xảy ra:
a. CO2 + Ca(OH)2 → CaCO3↓ + H2O
CO2 + CaCO3↓ + H2O → Ca(HCO3)2
b. 2KHCO3 + H2SO4 → K2SO4 + 2H2O + 2CO2↑
c. Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O d. C + O2 CO2 1.2.
X1: KHSO3; X3: MgSO4; X5: NaHSO4; X2: K2SO4; X4: Mg(OH)2; X6: Na2SO4.
Các phản ứng xảy ra trong sơ đồ:
2KHSO3 + H2SO4 → K2SO4 + 2SO2↑ + 2H2O
MgSO4 + 2KOH → K2SO4 + Mg(OH)2↓
2NaHSO4 + 2KOH → K2SO4 + Na2SO4 + 2H2O
Đề thi vào 10 môn Hóa học năm 2023 - Trường THPT Chuyên Đắk Lắk
2.3 K
1.2 K lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Đề thi được cập nhật liên tục trong gói này từ nay đến hết tháng 6/2023. Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Tailieugiaovien.com.vn giới thiệu bộ 29 đề thi vào 10 chuyên Hóa học có lời giải chi tiết, mới nhất năm 2022 - 2023 nhằm giúp Giáo viên có thêm tài liệu tham khảo ra đề thi môn Hóa học ôn vào 10.
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(2339 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN Hóa Học
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Ôn vào 10
Xem thêmTài liệu bộ mới nhất

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
SỞ GIÁO DỤC VÀ ĐÀO TẠO
ĐĂK LĂK
ĐỀ THI TUYỂN SINH VÀO LỚP 10 THPT
NĂM HỌC 2023
ĐỀ CHÍNH THỨC MÔN: HÓA HỌC - CHUYÊN
Thời gian làm bài: 150 phút
Cho biết nguyên tử khối của các nguyên tố: H = 1; C = 12; O = 16; Na = 23; Mg =
24; Al = 27; Ca = 40; Fe = 56; Cu = 64; Zn = 65; Br = 80; Sr = 88; Ba = 137.
Các thể tích khí đều đo ở điều kiện tiêu chuẩn; giả thiết các khí sinh ra không
tan trong nước.
Câu 1. (2,0 điểm)
1. Viết các phương trình hóa học của các phản ứng xảy ra khi:
a. Sục từ từ khí CO
2
đến dư vào dung dịch nước vôi trong.
b. Cho KHCO
3
rắn vào dung dịch H
2
SO
4
đặc dư.
c. Cho oxit Fe
3
O
4
tác dụng với dung dịch HCl dư.
d. Đốt cháy than gỗ.
2. Hoàn thành các sơ đồ phản ứng sau đây:
(X
1
) + H
2
SO
4
→ (X
2
) + SO
2
↑ + H
2
O (1)
(X
3
) + KOH → (X
2
) + (X
4
) (2)
(X
5
) + KOH → (X
2
) + (X
6
) + H
2
O (3)
Biết M(X
1
) = M(X
3
) = M(X
5
) = 120 g/mol.
Câu 2. (1,5 điểm)
1. Hình vẽ sau đây mô tả thí nghiệm điều chế khí Cl
2
trong phòng thí nghiệm:
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
B
E
D
Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
a. Hãy chọn các hóa chất A, B, D, E phù hợp và viết phương trình hóa học điều chế
khí Cl
2
.
b. Cho biết vai trò của bình (1), bình (2) trong quá trình điều chế trên.
2. Trình bày phương pháp hóa học để làm sạch khí CO
2
có lẫn tạp chất SO
2
.
Câu 3 (2,0 điểm)
1. Nung hỗn hợp X gồm a gam Al và 24 gam Fe
2
O
3
trong điều kiện không có không
khí, sau phản ứng thu được hỗn hợp chất rắn Y. Cho Y tác dụng với 500 ml dung
dịch NaOH bM thu được 6,72 lít khí H
2
, chất rắn không tan Z và dung dịch T gồm 2
chất tan có cùng nồng độ mol. Biết các phản ứng xảy ra hoàn toàn. Tìm giá trị của a
và b.
2. Etilen và các chất tương tự etilen có chứa 1 liên kết đôi trong phân tử nên dễ tham
gia phản ứng cộng. Phản ứng cộng với brom, liên kết kém bền trong liên kết đôi bị
đứt ra và mỗi phân tử etilen đã kết hợp thêm một phân tử brom:
Dẫn khí P (có công thức phân tử C
4
H
8
, chứa liên kết đôi tương tự etilen) đi qua dung
dịch brom màu da cam, sau phản ứng thấy dung dịch brom bị mất màu và thu được
sản phẩm hữu cơ Q (C
4
H
8
Br
2
). Viết công thức cấu tạo có thể có của Q.
Câu 4 (2,5 điểm)
1. Cho G, I và K là các hợp chất no, mạch hở có công thức đơn giản nhất là C
2
H
3
O
2
.
Biết các chất trên chỉ chứa nhóm chức phản ứng được với dung dịch NaOH (đun
nóng).
a. Xác định công thức phân tử của G, I, K.
b. Viết công thức cấu tạo có thể có của G, I và K. Biết G, I và K tham gia các phản
ứng theo đúng tỉ lệ mol như sau:
(G) + 2NaHCO
3
→ (G
1
) + 2CO
2
↑ + 2H
2
O
(I) + 2NaOH → (I
1
) + 2CH
3
OH
(K) + 2NaOH → (I
1
) + (K
1
) + H
2
O
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
2. Hỗn hợp T gồm 2 chất hữu cơ U (RCOOH) và V (R’(OH)
2
), trong đó R, R’ là các
gốc hiđrocacbon mạch hở. Lấy 0,05 mol hỗn hợp T tác dụng với Na dư thấy giải
phóng 0,896 lít khí. Mặt khác, đốt cháy hoàn toàn 0,25 mol hỗn hợp T, sau phản ứng
thu được 15,68 lít CO
2
và 13,5 gam H
2
O. Tìm công thức phân tử và viết công thức
cấu tạo của U và V.
Câu 5 (2,0 điểm)
1. Khoáng chất X có công thức dạng MCO
3
.M(OH)
2
.nH
2
O (M là kim loại có hóa trị
không đổi, n là số nguyên và n ≤ 10). Nung 19,2 gam X đến khối lượng không đổi
thu được 8,0 gam chất rắn MO và hỗn hợp Y (gồm khí và hơi).
a. Xác định công thức của khoáng chất X.
b. Dẫn toàn bộ hỗn hợp Y vào 100 ml dung dịch Z gồm NaOH 1M và Ba(OH)
2
0,3M
đến khi phản ứng hoàn toàn thu được m
1
gam kết tủa, khối lượng dung dịch tăng lên
so với ban đầu là m
2
gam. Tính m
1
, m
2
.
2. Dẫn hỗn hợp khí A gồm 2 hidrocacbon mạch hở N (C
n
H
2n+2
) và M (C
m
H
2m+2-2k
) vào
bình đựng 250 ml dung dịch Br
2
1M, chỉ xảy ra phản ứng:
C
m
H
2m+2-2k
+ kBr
2
→ C
m
H
2m+2-2k
Br
2k
Sau phản ứng hoàn toàn thấy khối lượng bình brom tăng lên 7,0 gam, đồng thời có
14,6 gam khí thoát ra khỏi bình. Đốt cháy hoàn toàn khí thoát ra thu được 21,952 lít
CO
2
.
a. Xác định công thức phân tử của N và M.
b. Tính thành phần phần trăm về thể tích của các khí trong hỗn hợp A.
---------Hết---------
Ghi chú: Thí sinh không được sử dụng tài liệu. Cán bộ coi thi không giải thích gì
thêm.
Họ và tên thí sinh: …………………………….
Số báo danh: ……………………………………
Chữ kí cán bộ coi thi 1: ……………………….
Chữ kí cán bộ coi thi 2: …………………………
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
SỞ GIÁO DỤC VÀ ĐÀO TẠO
ĐĂK LĂK
HƯỚNG DẪN GIẢI ĐỀ THI VÀO LỚP 10
NĂM HỌC 2022 – 2023
MÔN: HÓA HỌC - CHUYÊN
Câu 1. (2,0 điểm)
1. Viết các phương trình hóa học của các phản ứng xảy ra khi:
a. Sục từ từ khí CO
2
đến dư vào dung dịch nước vôi trong.
b. Cho KHCO
3
rắn vào dung dịch H
2
SO
4
đặc dư.
c. Cho oxit Fe
3
O
4
tác dụng với dung dịch HCl dư.
d. Đốt cháy than gỗ.
2. Hoàn thành các sơ đồ phản ứng sau đây:
(X
1
) + H
2
SO
4
→ (X
2
) + SO
2
↑ + H
2
O (1)
(X
3
) + KOH → (X
2
) + (X
4
) (2)
(X
5
) + KOH → (X
2
) + (X
6
) + H
2
O (3)
Biết M(X
1
) = M(X
3
) = M(X
5
) = 120 g/mol.
Hướng dẫn giải
1.1.
Các phương trình hóa học xảy ra:
a. CO
2
+ Ca(OH)
2
→ CaCO
3
↓ + H
2
O
CO
2
+ CaCO
3
↓ + H
2
O → Ca(HCO
3
)
2
b. 2KHCO
3
+ H
2
SO
4
→ K
2
SO
4
+ 2H
2
O + 2CO
2
↑
c. Fe
3
O
4
+ 8HCl → 2FeCl
3
+ FeCl
2
+ 4H
2
O
d. C + O
2
CO
2
1.2.
X
1
: KHSO
3
; X
3
: MgSO
4
; X
5
: NaHSO
4
; X
2
: K
2
SO
4
; X
4
: Mg(OH)
2
; X
6
: Na
2
SO
4
.
Các phản ứng xảy ra trong sơ đồ:
2KHSO
3
+ H
2
SO
4
→ K
2
SO
4
+ 2SO
2
↑ + 2H
2
O
MgSO
4
+ 2KOH → K
2
SO
4
+ Mg(OH)
2
↓
2NaHSO
4
+ 2KOH → K
2
SO
4
+ Na
2
SO
4
+ 2H
2
O
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
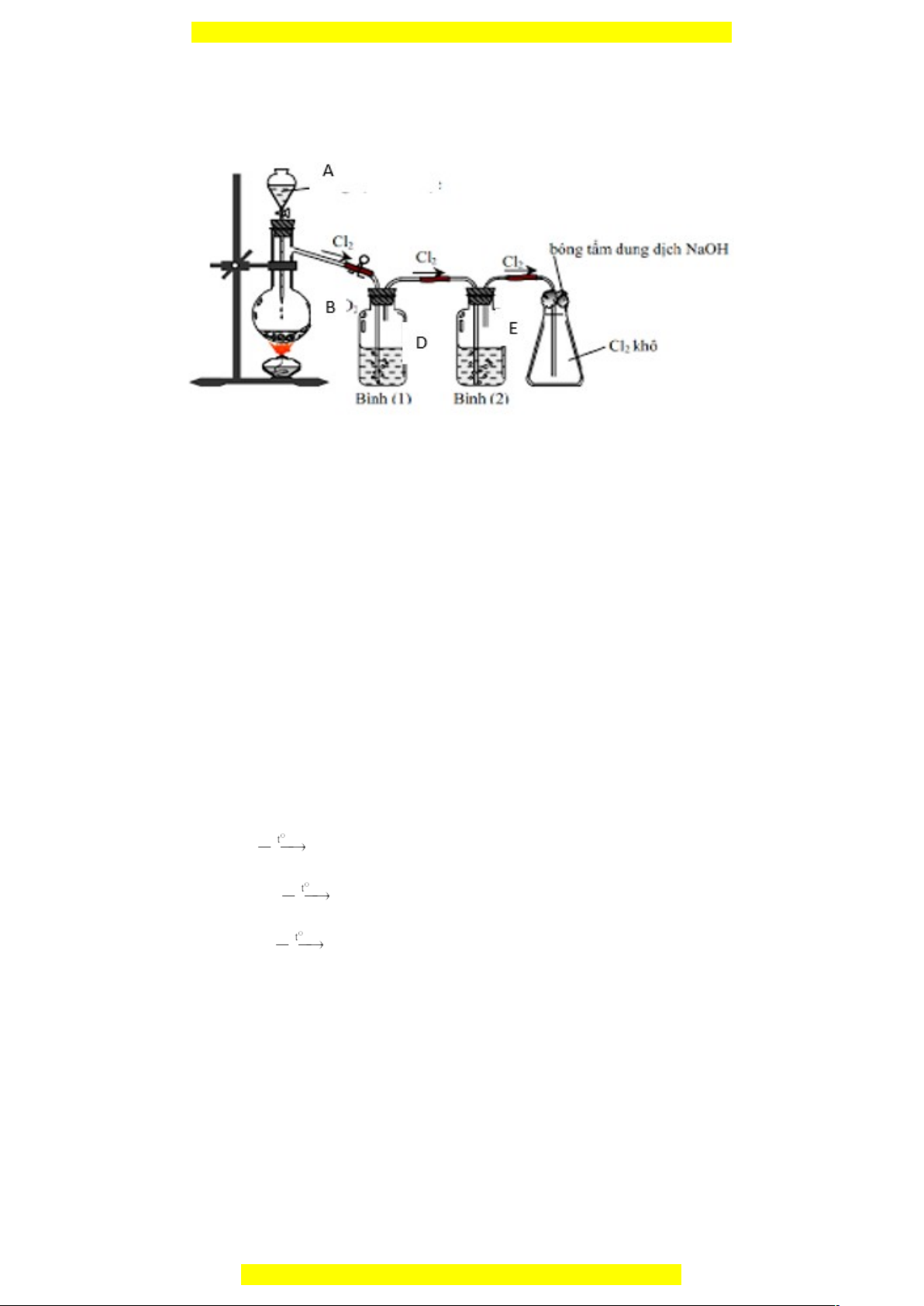
Câu 2. (1,5 điểm)
1. Hình vẽ sau đây mô tả thí nghiệm điều chế khí Cl
2
trong phòng thí nghiệm:
a. Hãy chọn các hóa chất A, B, D, E phù hợp và viết phương trình hóa học điều chế
khí Cl
2
.
b. Cho biết vai trò của bình (1), bình (2) trong quá trình điều chế trên.
2. Trình bày phương pháp hóa học để làm sạch khí CO
2
có lẫn tạp chất SO
2
.
Hướng dẫn giải
a. A: dung dịch HCl đặc.
B: Các chất oxi hóa mạnh như: MnO
2
, KMnO
4
, K
2
Cr
2
O
7
, CaOCl
2
, …
D: dung dịch NaCl bão hòa.
E: dung dịch H
2
SO
4
đặc.
Một số phương trình hóa học điều chế Cl
2
:
MnO
2
+ 4HCl đặc MnCl
2
+ Cl
2
+ 2H
2
O
2KMnO
4
+ 16HCl
đặc
2KCl + 2MnCl
2
+ 5Cl
2
+ 8H
2
O
K
2
Cr
2
O
7
+ 14HCl
đặc
2KCl + 2CrCl
3
+ 3Cl
2
+ 7H
2
O
b. Vai trò của bình 1 (dung dịch NaCl bão hòa): để giữ lại hơi HCl trong hỗn hợp khí
và hơi thoát ra từ bình cầu.
Vai trò của bình 2 (dung dịch H
2
SO
4
đặc): để giữ lại hơi nước.
2.
Cho hỗn hợp khí đi qua dung dịch brom dư, SO
2
bị giữ lại theo phương trình:
SO
2
+ Br
2
+ 2H
2
O → H
2
SO
4
+ 2HBr
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85























