SỞ GIÁO DỤC VÀ ĐÀO
KỲ THI TUYỂN SINH VÀO LỚP 10 THPT TẠO NĂM HỌC 2023 TỈNH QUẢNG NINH
Môn thi: Hóa học (chuyên)
Dành cho thí sinh thi vào Trường THPT Chuyên Hạ Long
Thời gian làm bài: 120 phút Câu 1. (2,5 điểm)
1. Nêu hiện tượng quan sát được và viết các phương trình hóa học của phản ứng xảy
ra (nếu có) khi tiến hành các thí nghiệm sau:
a) Cho lượng dư CuSO4 khan vào rượu etylic 90°.
b) Nhỏ vài giọt oleum (H2SO4.3SO3) vào dung dịch Ba(HCO3)2.
c) Đưa bình đựng hỗn hợp khí metan và clo ra ánh sáng. Sau một thời gian, cho nước
vào bình. lắc nhẹ rồi thêm vào một mẩu giấy quỳ tím.
d) Lấy nước ép quả nho chín cho vào ống nghiệm có chứa dung dịch AgNO3/NH3,
đặt ống nghiệm vào cốc nước nóng.
2. Chỉ dùng tối đa 2 thuốc thử hãy trình bày cách phân biệt các kim loại đựng trong
các lọ riêng biệt gồm: Ba, Ag, Al, Fe, Mg.
3. Cho hỗn hợp các khí gồm: CO2, SO2, C2H4, C2H2, CH4.
Trình bày phương pháp hóa học để thu được CH4 tinh khiết từ hỗn hợp khí trên. Viết
các phương trình hóa học của phản ứng xảy ra. Câu 2. (2,5 điểm)
1. Chất A được tạo ra do quá trình quang hợp của cây xanh. Thủy phân chất A trong
môi trường axit được chất A1. Lên men chất A1 được ancol (rượu) A2. Tiếp tục lên
men ancol A2 được axit A3. Cho axit A3 phản ứng với ancol A2 trong điều kiện thích
hợp được hợp chất hữu cơ A4.
Xác định các chất A, A1, A2, A3, A4 và viết các phương trình hóa học của phản ứng xảy ra.
2. Hòa tan hoàn toàn 8,56 gam một muối clorua (muối Y) vào nước được 200 mL
dung dịch Y. Lấy 50 mL dung dịch Y tác dụng với dung dịch AgNO3 dư thu được
5,74 gam muối kết tủa trắng.
a) Tìm công thức muối Y.
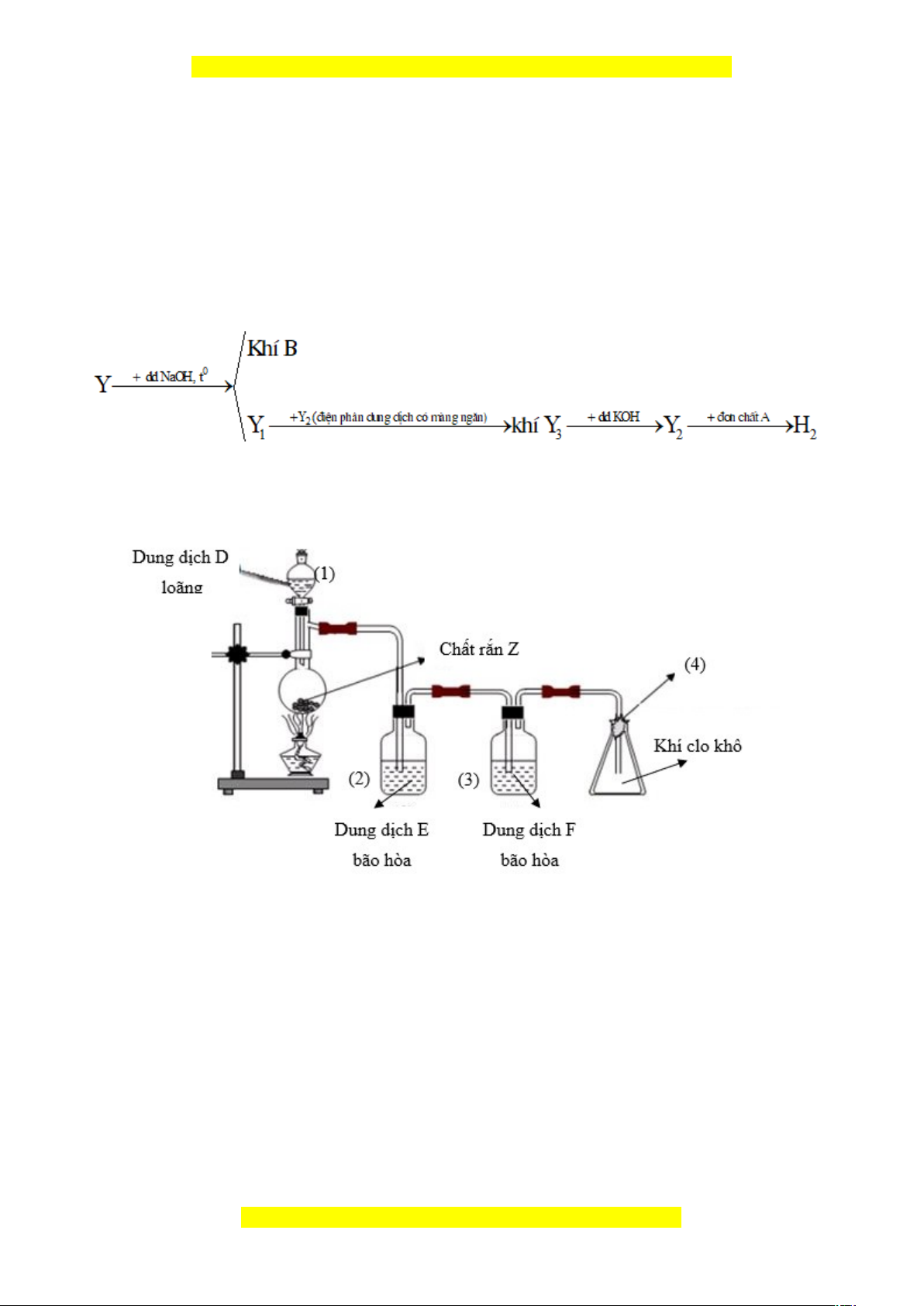
b) Từ muối Y viết các phương trình hóa học thực hiện sơ đồ sau (dung dịch viết tắt là dd)
3. Cho sơ đồ thí nghiệm điều chế khí clo như sau:
a) Viết một phương trình hóa học điều chế khí clo trong phòng thí nghiệm.
b) Chỉ ra chi tiết còn thiếu hoặc chưa chính xác ở vị trí (1), (2), (3), (4) trong sơ đồ
trên, giải thích tại sao. Xác định các chất D, E, F, Z phù hợp với sơ đồ đúng.
Câu 3. (2,5 điểm).
1. Hòa tan hoàn toàn 25,6 gam hỗn hợp D gồm MgO và Fe bằng dung dịch H2SO4
loãng, dư thu được dung dịch E và V lít H2(đktc). Thêm từ từ dung dịch NaOH đến
dư vào dung dịch E, kết thúc phản ứng lọc lấy kết tủa, nung trong không khí đến khối
lượng không đổi thu được 28 gam chất rắn M.
Tính giá trị của V.
2. Chất dẻo PVC được dùng làm vật liệu cách điện, ống dẫn nước, vải che mưa, … do
cách điện tốt, bền với axit, PVC có thể được điều chế theo sơ đồ sau: CH4 → A → B → PVC.
a) Viết các phương trình hóa học của phản ứng (dạng công thức cấu tạo thu gọn) theo sơ đồ trên.
b) Biết CH4 chiếm 90% thể tích khí thiên nhiên và hiệu suất tương ứng với mỗi giai
đoạn lần lượt là 50%, 80%, 80%.
Tính số m3 (đktc) khí thiên nhiên cần để điều chế 1 tấn PVC.
3. Chia hỗn hợp X gồm bột Cu và Fe3O4 (đã trộn đều) thành 2 phần bằng nhau và tiến hành các thí nghiệm sau:
+ Thí nghiệm 1: (được thực hiện trong, môi trường không có không khí)
Cho phần I vào dung dịch HCl loãng, dư thu được dung dịch Y và chất rắn không tan.
Cô cạn dung dịch Y thu được 46,08 gam chất rắn Z. Nung chất rắn Z ở điều kiện
thích hợp thu được 30,96 gam chất rắn T chỉ gồm các muối khan. Giả thiết hiệu suất cho các quá trình là 100%, + Thí nghiệm 2:
Hòa tan hoàn toàn phần 2 bằng dung dịch H2SO4 đặc, nóng dư thu được khí SO2 (sản
phẩm khử duy nhất). Hấp thụ hết lượng SO2 này vào bình đựng dung dịch Ca(OH)2
dư, thấy khối lượng bình tăng 7,04 gam.
a) Viết các phương trình hóa học và tỉnh phần trăm khối lượng Cu trong hỗn hợp X.
b) Tìm công thức phân tử của các chất trong Z. Biết các chất trong Z đều có khối
lượng mol phân tử nhỏ hơn 220 g/mol. Câu 4. (1,5 điểm)
1. COVID-19 là bệnh đường hô hấp cấp tính truyền nhiễm gây ra bởi chủng virut
SARS-CoV 2. Tổ chức Y tế thế giới (WHO) đã tuyên bố dịch viêm phổi do virut
Corona (chủng mới) là đại dịch toàn cầu. Một trong những biện pháp phòng ngừa
nguy cơ lây nhiễm là thường xuyên rửa tay bằng dung dịch rửa tay khô. Tổ chức Y tế
thế giới đã có hướng dẫn người dân tự pha chế nước rửa tay khô với lượng dùng là lít
có công thức pha chế như sau: cồn (C2H5OH) 96o: 830 ml; oxi già (H2O2) 3%: 40 ml;
chất X: 15 ml; tinh dầu: 5 ml; nước cất hoặc nước đun sôi để nguội 110 ml.
a) Tính phần trăm thể tích của C2H5OH trong dung dịch thu được sau khi pha trộn các
nguyên liệu trên với nhau.
b) Trong nước rửa tay khô, X có tác dụng giữ ẩm, dưỡng da. Biết X là ancol có công
thức tổng quát CxHy(OH)n và 1 nguyên tử C trong X chỉ có thể liên kết tối đa 1 nhóm
-OH. Cho m gam X vào bình chứa Na (dư), sau khi kết thúc phản ứng thấy có 3,36 lít
(đktc) khí thoát ra và khối lượng bình tăng 8,9 gam so với ban đầu. Nếu đốt cháy
hoàn toàn 0,1 mol X, khối lượng CO2 thu được không vượt quá 22,0 gam. Tìm công thức cấu tạo của X.
2. Khí SO2 được sinh ra do sự đốt cháy các nhiên liệu hóa thạch (than, dầu, khí
đốt,...) là nguyên nhân quan trọng nhất gây ô nhiễm không khí. Tiêu chuẩn quốc tế
quy định nếu trong không khí nồng độ SO2 vượt quá 30.10-6 mol/m3 thì coi như
không khí bị ô nhiễm SO2. Khi tiến hành phân tích 50 lít không khí ở một thành phố
thấy có chứa 0,08 mg SO2. Hãy cho biết thành phố đó có bị ô nhiễm SO2 hay không?
3. Nicotin là một chất tìm thấy trong các cây họ Cà (Solanaceae), chủ
yếu trong cây thuốc lá (0,6 đến 3% trọng lượng cây thuốc lá khô).
Nó là một chất độc thần kinh rất mạnh, có thể khiến giấc ngủ bị rối
loạn, nhức đầu, chóng mặt, có nguy cơ hạn chế dòng máu chảy lên
não. Hình bên cho thấy công thức cấu tạo thu gọn của nicotin.
- Tính thành phần phần trăm về khối lượng của nitơ trong nicotin, biết nitơ có hóa trị III trong nicotin. Câu 5. (1,0 điểm)
Dẫn 1 luồng hơi nước qua than nóng đỏ thì thu được hỗn hợp khí X gồm CO2, CO,
H2, tỉ khối hơi của X so với CH4 là 0,975. Toàn bộ hỗn hợp khí X trên khử vừa đủ
27,6 gam hỗn hợp Y gồm CuO, Fe3O4 nung nóng thu được rắn Z chỉ có 2 kim loại,
cho toàn bộ Z vào dung dịch HCl dư thấy có 3,36 lít H2 bay ra (đktc).
Xác định phần trăm thể tích của CO trong hỗn hợp X. Giả thiết các phản ứng xảy ra hoàn toàn
Đề thi vào 10 môn Hóa học năm 2023 - Trường THPT Chuyên Quang Ninh
2 K
1 K lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Đề thi được cập nhật liên tục trong gói này từ nay đến hết tháng 6/2023. Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Tailieugiaovien.com.vn giới thiệu bộ 29 đề thi vào 10 chuyên Hóa học có lời giải chi tiết, mới nhất năm 2022 - 2023 nhằm giúp Giáo viên có thêm tài liệu tham khảo ra đề thi môn Hóa học ôn vào 10.
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(2041 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN Hóa Học
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Ôn vào 10
Xem thêmTài liệu bộ mới nhất

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
SỞ GIÁO DỤC VÀ ĐÀO
TẠO
TỈNH QUẢNG NINH
KỲ THI TUYỂN SINH VÀO LỚP 10 THPT
NĂM HỌC 2023
Môn thi: Hóa học (chuyên)
Dành cho thí sinh thi vào Trường THPT
Chuyên Hạ Long
Thời gian làm bài: 120 phút
Câu 1. (2,5 điểm)
1. Nêu hiện tượng quan sát được và viết các phương trình hóa học của phản ứng xảy
ra (nếu có) khi tiến hành các thí nghiệm sau:
a) Cho lượng dư CuSO
4
khan vào rượu etylic 90°.
b) Nhỏ vài giọt oleum (H
2
SO
4
.3SO
3
) vào dung dịch Ba(HCO
3
)
2
.
c) Đưa bình đựng hỗn hợp khí metan và clo ra ánh sáng. Sau một thời gian, cho nước
vào bình. lắc nhẹ rồi thêm vào một mẩu giấy quỳ tím.
d) Lấy nước ép quả nho chín cho vào ống nghiệm có chứa dung dịch AgNO
3
/NH
3
,
đặt ống nghiệm vào cốc nước nóng.
2. Chỉ dùng tối đa 2 thuốc thử hãy trình bày cách phân biệt các kim loại đựng trong
các lọ riêng biệt gồm: Ba, Ag, Al, Fe, Mg.
3. Cho hỗn hợp các khí gồm: CO
2
, SO
2
, C
2
H
4
, C
2
H
2
, CH
4
.
Trình bày phương pháp hóa học để thu được CH
4
tinh khiết từ hỗn hợp khí trên. Viết
các phương trình hóa học của phản ứng xảy ra.
Câu 2. (2,5 điểm)
1. Chất A được tạo ra do quá trình quang hợp của cây xanh. Thủy phân chất A trong
môi trường axit được chất A
1
. Lên men chất A
1
được ancol (rượu) A
2
. Tiếp tục lên
men ancol A
2
được axit A
3
. Cho axit A
3
phản ứng với ancol A
2
trong điều kiện thích
hợp được hợp chất hữu cơ A
4
.
Xác định các chất A, A
1
, A
2
, A
3
, A
4
và viết các phương trình hóa học của phản ứng
xảy ra.
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
2. Hòa tan hoàn toàn 8,56 gam một muối clorua (muối Y) vào nước được 200 mL
dung dịch Y. Lấy 50 mL dung dịch Y tác dụng với dung dịch AgNO
3
dư thu được
5,74 gam muối kết tủa trắng.
a) Tìm công thức muối Y.
b) Từ muối Y viết các phương trình hóa học thực hiện sơ đồ sau (dung dịch viết tắt là
dd)
3. Cho sơ đồ thí nghiệm điều chế khí clo như sau:
a) Viết một phương trình hóa học điều chế khí clo trong phòng thí nghiệm.
b) Chỉ ra chi tiết còn thiếu hoặc chưa chính xác ở vị trí (1), (2), (3), (4) trong sơ đồ
trên, giải thích tại sao. Xác định các chất D, E, F, Z phù hợp với sơ đồ đúng.
Câu 3. (2,5 điểm).
1. Hòa tan hoàn toàn 25,6 gam hỗn hợp D gồm MgO và Fe bằng dung dịch H
2
SO
4
loãng, dư thu được dung dịch E và V lít H
2
(đktc). Thêm từ từ dung dịch NaOH đến
dư vào dung dịch E, kết thúc phản ứng lọc lấy kết tủa, nung trong không khí đến khối
lượng không đổi thu được 28 gam chất rắn M.
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Tính giá trị của V.
2. Chất dẻo PVC được dùng làm vật liệu cách điện, ống dẫn nước, vải che mưa, … do
cách điện tốt, bền với axit, PVC có thể được điều chế theo sơ đồ sau:
CH
4
→ A → B → PVC.
a) Viết các phương trình hóa học của phản ứng (dạng công thức cấu tạo thu gọn) theo
sơ đồ trên.
b) Biết CH
4
chiếm 90% thể tích khí thiên nhiên và hiệu suất tương ứng với mỗi giai
đoạn lần lượt là 50%, 80%, 80%.
Tính số m
3
(đktc) khí thiên nhiên cần để điều chế 1 tấn PVC.
3. Chia hỗn hợp X gồm bột Cu và Fe
3
O
4
(đã trộn đều) thành 2 phần bằng nhau và tiến
hành các thí nghiệm sau:
+ Thí nghiệm 1: (được thực hiện trong, môi trường không có không khí)
Cho phần I vào dung dịch HCl loãng, dư thu được dung dịch Y và chất rắn không tan.
Cô cạn dung dịch Y thu được 46,08 gam chất rắn Z. Nung chất rắn Z ở điều kiện
thích hợp thu được 30,96 gam chất rắn T chỉ gồm các muối khan. Giả thiết hiệu suất
cho các quá trình là 100%,
+ Thí nghiệm 2:
Hòa tan hoàn toàn phần 2 bằng dung dịch H
2
SO
4
đặc, nóng dư thu được khí SO
2
(sản
phẩm khử duy nhất). Hấp thụ hết lượng SO
2
này vào bình đựng dung dịch Ca(OH)
2
dư, thấy khối lượng bình tăng 7,04 gam.
a) Viết các phương trình hóa học và tỉnh phần trăm khối lượng Cu trong hỗn hợp X.
b) Tìm công thức phân tử của các chất trong Z. Biết các chất trong Z đều có khối
lượng mol phân tử nhỏ hơn 220 g/mol.
Câu 4. (1,5 điểm)
1. COVID-19 là bệnh đường hô hấp cấp tính truyền nhiễm gây ra bởi chủng virut
SARS-CoV 2. Tổ chức Y tế thế giới (WHO) đã tuyên bố dịch viêm phổi do virut
Corona (chủng mới) là đại dịch toàn cầu. Một trong những biện pháp phòng ngừa
nguy cơ lây nhiễm là thường xuyên rửa tay bằng dung dịch rửa tay khô. Tổ chức Y tế
thế giới đã có hướng dẫn người dân tự pha chế nước rửa tay khô với lượng dùng là lít
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
có công thức pha chế như sau: cồn (C
2
H
5
OH) 96
o
: 830 ml; oxi già (H
2
O
2
) 3%: 40 ml;
chất X: 15 ml; tinh dầu: 5 ml; nước cất hoặc nước đun sôi để nguội 110 ml.
a) Tính phần trăm thể tích của C
2
H
5
OH trong dung dịch thu được sau khi pha trộn các
nguyên liệu trên với nhau.
b) Trong nước rửa tay khô, X có tác dụng giữ ẩm, dưỡng da. Biết X là ancol có công
thức tổng quát C
x
H
y
(OH)
n
và 1 nguyên tử C trong X chỉ có thể liên kết tối đa 1 nhóm
-OH. Cho m gam X vào bình chứa Na (dư), sau khi kết thúc phản ứng thấy có 3,36 lít
(đktc) khí thoát ra và khối lượng bình tăng 8,9 gam so với ban đầu. Nếu đốt cháy
hoàn toàn 0,1 mol X, khối lượng CO
2
thu được không vượt quá 22,0 gam. Tìm công
thức cấu tạo của X.
2. Khí SO
2
được sinh ra do sự đốt cháy các nhiên liệu hóa thạch (than, dầu, khí
đốt,...) là nguyên nhân quan trọng nhất gây ô nhiễm không khí. Tiêu chuẩn quốc tế
quy định nếu trong không khí nồng độ SO
2
vượt quá 30.10
-6
mol/m
3
thì coi như
không khí bị ô nhiễm SO
2
. Khi tiến hành phân tích 50 lít không khí ở một thành phố
thấy có chứa 0,08 mg SO
2
. Hãy cho biết thành phố đó có bị ô nhiễm SO
2
hay không?
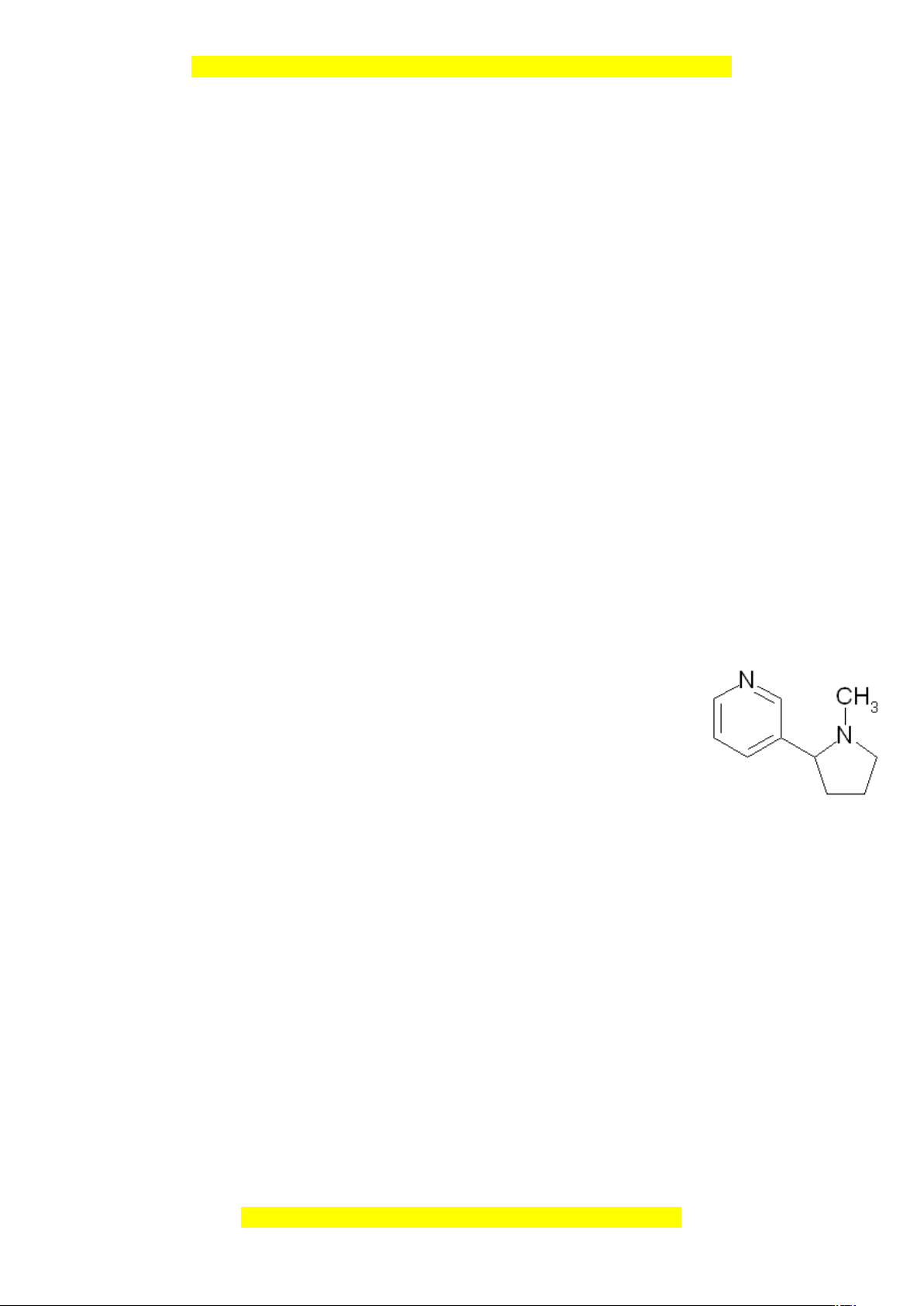
3. Nicotin là một chất tìm thấy trong các cây họ Cà (Solanaceae), chủ
yếu trong cây thuốc lá (0,6 đến 3% trọng lượng cây thuốc lá khô).
Nó là một chất độc thần kinh rất mạnh, có thể khiến giấc ngủ bị rối
loạn, nhức đầu, chóng mặt, có nguy cơ hạn chế dòng máu chảy lên
não. Hình bên cho thấy công thức cấu tạo thu gọn của nicotin.
- Tính thành phần phần trăm về khối lượng của nitơ trong nicotin, biết nitơ có hóa trị
III trong nicotin.
Câu 5. (1,0 điểm)
Dẫn 1 luồng hơi nước qua than nóng đỏ thì thu được hỗn hợp khí X gồm CO
2
, CO,
H
2
, tỉ khối hơi của X so với CH
4
là 0,975. Toàn bộ hỗn hợp khí X trên khử vừa đủ
27,6 gam hỗn hợp Y gồm CuO, Fe
3
O
4
nung nóng thu được rắn Z chỉ có 2 kim loại,
cho toàn bộ Z vào dung dịch HCl dư thấy có 3,36 lít H
2
bay ra (đktc).
Xác định phần trăm thể tích của CO trong hỗn hợp X. Giả thiết các phản ứng xảy ra
hoàn toàn
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
-------------------------- HẾT--------------------------
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85