CHƯƠNG 8: ANCOL – PHENOL BÀI 22: ANCOL Mục tiêu Kiến thức
+ Nêu được định nghĩa, phân loại ancol và công thức chung, đặc điểm cấu tạo phân tử, đồng
phân, danh pháp (gốc – chức và thay thế).
+ Nêu được tính chất vật lí: Nhiệt độ sôi, độ tan trong nước; Liên kết hiđro.
+ Nêu được tính chất hoá học: Phản ứng của nhóm OH (thế H, thế OH), phản ứng tách nước tạo
thành anken hoặc ete, phản ứng oxi hoá ancol bậc I, bậc II thành anđehit, xeton; Phản ứng cháy.
+ Trình bày được phương pháp điều chế ancol từ anken, điều chế etanol từ tinh bột, điều chế
glixerol và ứng dụng của etanol.
+ Chỉ ra được công thức phân tử, cấu tạo, tính chất riêng của glixerol (phản ứng với Cu(OH)2). Kĩ năng
+ Viết được công thức cấu tạo các đồng phân và đọc được tên khi biết công thức cấu tạo của các ancol (có 4C – 5C).
+ Dự đoán, mô tả hiện tượng phản ứng, giải thích và viết các phương trình hoá học.
+ Phân biệt được ancol đơn chức với glixerol bằng phương pháp hoá học.
+ Xác định được công thức phân tử, công thức cấu tạo của ancol.
I. LÍ THUYẾT TRỌNG TÂM
1. Cấu tạo, đồng đẳng, đồng phân, danh pháp
a. Đặc điểm cấu tạo
“Nhóm OH” gắn ở C no và mỗi C no chỉ được gắn 1 nhóm OH. Công thức phân tử chung của một số dãy đồng đẳng ancol:
Ancol no, đơn chức: CnH2n+1OH
Ancol không no, một nối đôi, đơn chức: CnH2n-1OH
Ancol no, đa chức: CnH2n+2Ox hay CnH2n+2-x(OH)x Ví dụ:
Ancol: CH3OH, C2H5OH, C3H7OH… thuộc cùng một dãy ancol no, đơn, hở, còn gọi là ankanol.
Ancol anlylic: CH2=CHCH2OH, thuộc dãy ancol không no, đơn chức, mạch hở.
C2H4(OH)2, C3H5(OH)3… thuộc dãy ancol no, đa chức, mạch hở (poliol). b. Đồng phân
Đồng phân mạch C, vị trí nhóm OH. Trang 1
Ngoài ra, cùng công thức phân tử còn có đồng phân khác chức: ete.
Ví dụ: C3H7OH có một dạng mạch C không nhánh, hở, nhưng có hai đồng phân vị trí OH và có một đồng phân dạng ete. c. Danh pháp
Tên thông thường: Ancol + tên gốc hiđrocacnol + ic.
Tên theo IUPAC: Tên IUPAC của hiđrocacbon + số chỉ vị trí OH + ol (1)/ điol (2)/ triol (3)…
(ưu tiên đánh số thứ tự cacbon mạch chính sao cho các chỉ số nhóm OH là nhỏ nhất). Ví dụ: n-C3H7OH:
Tên: Ancol n-proylic/propan-1-ol. C2H4(OH)2:
Tên: Etylenglicol/etan-1,2-điol. CH2=CHCH2OH:
Tên: Ancol anlylic/propen-1-ol.
2. Tính chất vật lí và liên kết hiđro
Các phân tử có nhóm OH (nước, ancol, axit axetic…) có liên kết liên phân tử: – O – H…O – H làm tăng
nhiệt độ sôi và độ tan trong nước hơn so với chất không có nhóm OH. Ví dụ:
C2H5Cl: rất ít tan trong nước, sôi ở 12oC.
C2H5OH: tan tốt trong nước, sôi ở 78,2oC.
Dựa vào bảng hằng số vật lí của một số ancol (trang 181 SGK):
Khối lượng phân tử tăng thì nhiệt độ sôi tăng, độ tan giảm.
Chất có càng nhiều nhóm OH thì liên kết H càng nhiều, nhiệt độ sôi càng cao.
Ví dụ: Bảng nhiệt độ sôi (ts) một số ancol như sau: Ancol
Khối lượng phân tử ts (oC) CH3OH 32 64,5 C3H7OH 60 82,4 C2H4(OH)2 62 197,6
Công thức tính độ rượu: Độ rượu =
Ví dụ: Cồn 96o nghĩa là Trang 2
Trong 100 ml cồn này thì có 96 ml C2H5OH.
3. Tính chất hoá học
Phản ứng thế H của nhóm OH (phản ứng với kim loại kiềm, phản ứng tạo phức với đồng(II) hiđroxit của glixerol).
Ví dụ: Glixerol – một ancol no, đa chức mạch hở: phản ứng được với Na, hoà tan Cu(OH)2.
Phản ứng thế nhóm OH ancol (phản ứng với HX tạo dẫn xuất halogen, phản ứng giữa hai phân tử ancol tạo ete).
Phản ứng este hoá với axit cacboxylic R – COOH.
Phản ứng tách nước tạo thành anken.
Phản ứng oxi hoá không hoàn toàn: + Ancol bậc I Anđehit, axit. + Ancol bậc II Xeton. + Ancol bậc III Không phản ứng.
Phản ứng oxi hoá hoàn toàn (Phản ứng cháy).
Ví dụ: Etanol có phản ứng với các chất: Na, K, HCl, HBr, CH3COOH, CuO, lên men giấm, tách nước ở
trên 170oC tạo etilen, dưới 170oC tạo đietyl ete. Khi cháy:
Chú ý: Ancol no, mạch hở khi cháy: 4. Điều chế
Phương pháp điều chế etanol: thuỷ phân dẫn xuất halogen, hiđrat hoá etilen, lên men rượu glucozơ. Trang 3
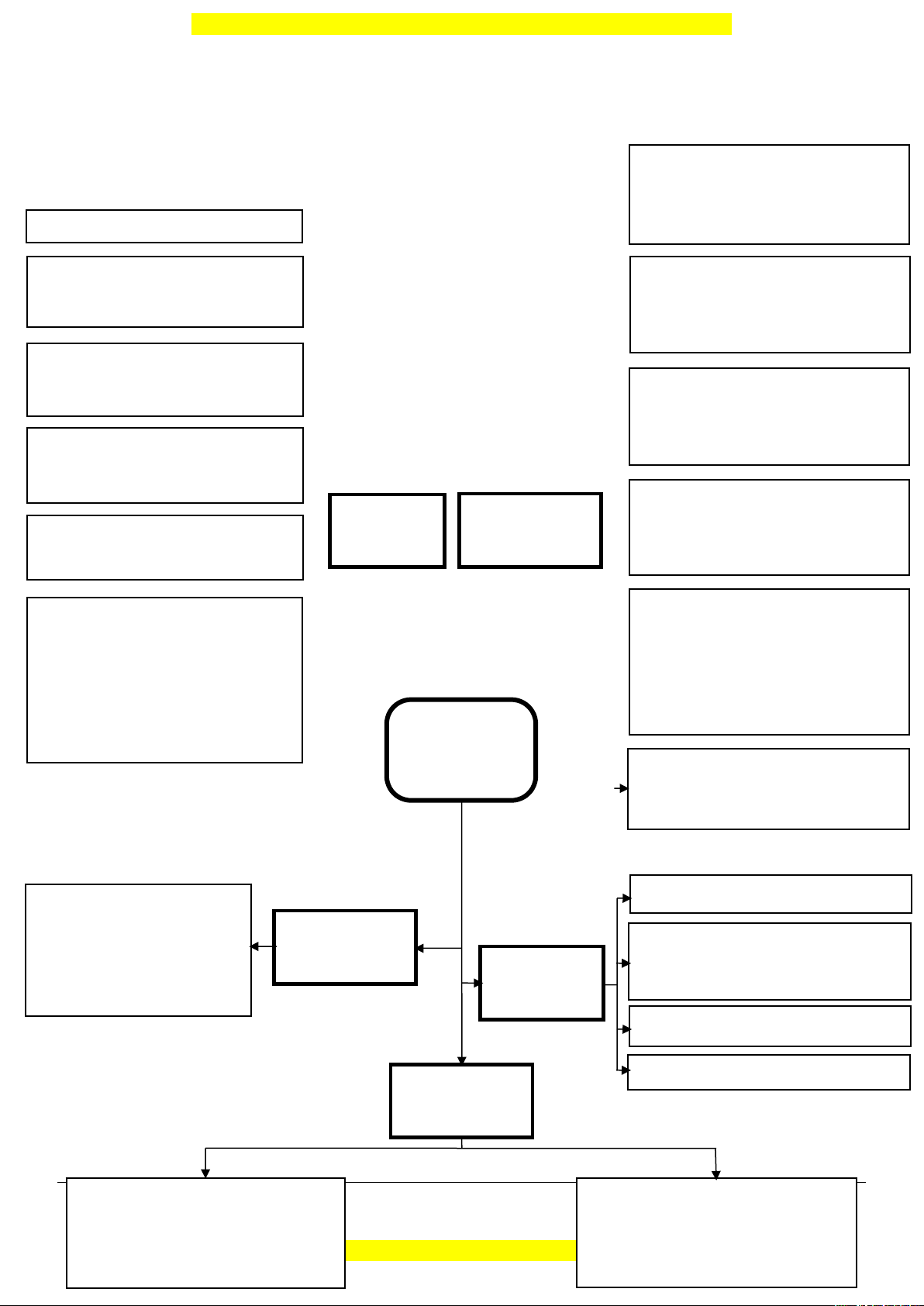
SƠ ĐỒ HỆ THỐNG HOÁ
Thế H ở OH bởi kim loại kiềm: Số nhóm OH =
Phân tử có nhóm OH gắn ở C no Công thức chung:
Ancol có từ 2 nhóm OH liền kề: C H (OH)
hoà tan Cu(OH) tạo dung dịch n 2n+2-2k-a a 2 xanh lam Ancol no, đơn chức:
Phản ứng este hoá: thay thế H C H OH n 2n+1
trong nhóm OH bởi gốc axyl Ancol no, đa chức: C H O hay RCO trong axit hữu cơ RCOOH n 2n+2 x C H (OH) n 2n+2-x x
Tách HOH: Từ một phân tử, quy TÍNH CHẤT CẤU TẠO
Đồng phân mạch C, vị trí nhóm
tắc Zaixep, tạo liên kết bội; tách HOÁ HỌC OH. nước từ 2 phân tử ete
Tên thông thường: Ancol – tên
Oxi hoá ancol bậc 1 tạo thành gốc hiđrocacbol + ic. anđehit;
Tên theo IUPAC: Tên IUPAC của
Oxi hoá ancol bậc 2 tạo xeton;
hiđrocacbon + số chỉ vị trí OH + Phản ứng lên men giấm
ol (1)/ điol (2)/ triol (3)… ANCOL Ancol no, hở khi cháy:
Nhiệt độ sôi, độ tan trong Hiđrat hoá anken TÍNH CHẤT nước cao hơn hiđrocacbon
Thuỷ phân dẫn xuất halogen bởi VẬT LÍ
do có liên kết H giữa các kiềm ĐIỀU CHẾ nhóm OH Hiđro hoá anđehit, xeton
Lên men rượu: được C2H5OH ỨNG DỤNG
C2H5OH: Làm dung môi, sản xuất Glixerol, C3H5(OH)3: dùng T ra t ng rong 4
nước hoa, làm nhiên liệu, sát
công nghiệp sản xuất sơn, mực
trùng y tế… in…
Bộ chuyên đề đầy đủ môn Hóa học 11 năm 2023 - Chương 8: Ancol - Phenol
1.4 K
684 lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Tài liệu được cập nhật liên tục trong gói này từ nay đến hết tháng 6/2023. Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Tailieugiaovien.com.vn giới thiệu bộ chuyên đề môn Hóa học 11 năm 2023 - Chương 8: Ancol - Phenol bao gồm: Bài 22. Ancol; Bài 23. Phenol mới nhất năm 2022 - 2023 nhằm giúp Giáo viên có thêm tài liệu tham khảo chuyên đề luyện thi Hóa học lớp 11.
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(1367 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN Hóa Học
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Lớp 11
Xem thêmTài liệu bộ mới nhất

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
CHƯƠNG 8: ANCOL – PHENOL
BÀI 22: ANCOL
Mục tiêu
Kiến thức
+ Nêu được định nghĩa, phân loại ancol và công thức chung, đặc điểm cấu tạo phân tử, đồng
phân, danh pháp (gốc – chức và thay thế).
+ Nêu được tính chất vật lí: Nhiệt độ sôi, độ tan trong nước; Liên kết hiđro.
+ Nêu được tính chất hoá học: Phản ứng của nhóm OH (thế H, thế OH), phản ứng tách nước tạo
thành anken hoặc ete, phản ứng oxi hoá ancol bậc I, bậc II thành anđehit, xeton; Phản ứng
cháy.
+ Trình bày được phương pháp điều chế ancol từ anken, điều chế etanol từ tinh bột, điều chế
glixerol và ứng dụng của etanol.
+ Chỉ ra được công thức phân tử, cấu tạo, tính chất riêng của glixerol (phản ứng với Cu(OH)
2
).
Kĩ năng
+ Viết được công thức cấu tạo các đồng phân và đọc được tên khi biết công thức cấu tạo của các
ancol (có 4C – 5C).
+ Dự đoán, mô tả hiện tượng phản ứng, giải thích và viết các phương trình hoá học.
+ Phân biệt được ancol đơn chức với glixerol bằng phương pháp hoá học.
+ Xác định được công thức phân tử, công thức cấu tạo của ancol.
I. LÍ THUYẾT TRỌNG TÂM
1. Cấu tạo, đồng đẳng, đồng phân, danh pháp
a. Đặc điểm cấu tạo
“Nhóm OH” gắn ở C no và mỗi C no chỉ được gắn 1 nhóm OH. Công thức phân tử chung của một số dãy
đồng đẳng ancol:
Ancol no, đơn chức: C
n
H
2n+1
OH
Ancol không no, một nối đôi, đơn chức: C
n
H
2n-1
OH
Ancol no, đa chức: C
n
H
2n+2
O
x
hay C
n
H
2n+2-x
(OH)
x
Ví dụ:
Ancol: CH
3
OH, C
2
H
5
OH, C
3
H
7
OH… thuộc cùng một dãy ancol no, đơn, hở, còn gọi là ankanol.
Ancol anlylic: CH
2
=CHCH
2
OH, thuộc dãy ancol không no, đơn chức, mạch hở.
C
2
H
4
(OH)
2
, C
3
H
5
(OH)
3
… thuộc dãy ancol no, đa chức, mạch hở (poliol).
b. Đồng phân
Đồng phân mạch C, vị trí nhóm OH.
Trang 1
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Ngoài ra, cùng công thức phân tử còn có đồng phân khác chức: ete.
Ví dụ: C
3
H
7
OH có một dạng mạch C không nhánh, hở, nhưng có hai đồng phân vị trí OH và có một đồng
phân dạng ete.
c. Danh pháp
Tên thông thường: Ancol + tên gốc hiđrocacnol + ic.
Tên theo IUPAC: Tên IUPAC của hiđrocacbon + số chỉ vị trí OH + ol (1)/ điol (2)/ triol (3)…
(ưu tiên đánh số thứ tự cacbon mạch chính sao cho các chỉ số nhóm OH là nhỏ nhất).
Ví dụ:
n-C
3
H
7
OH:
Tên: Ancol n-proylic/propan-1-ol.
C
2
H
4
(OH)
2
:
Tên: Etylenglicol/etan-1,2-điol.
CH
2
=CHCH
2
OH:
Tên: Ancol anlylic/propen-1-ol.
2. Tính chất vật lí và liên kết hiđro
Các phân tử có nhóm OH (nước, ancol, axit axetic…) có liên kết liên phân tử: – O – H…O – H làm tăng
nhiệt độ sôi và độ tan trong nước hơn so với chất không có nhóm OH.
Ví dụ:
C
2
H
5
Cl: rất ít tan trong nước, sôi ở 12
o
C.
C
2
H
5
OH: tan tốt trong nước, sôi ở 78,2
o
C.
Dựa vào bảng hằng số vật lí của một số ancol (trang 181 SGK):
Khối lượng phân tử tăng thì nhiệt độ sôi tăng, độ tan giảm.
Chất có càng nhiều nhóm OH thì liên kết H càng nhiều, nhiệt độ sôi càng cao.
Ví dụ: Bảng nhiệt độ sôi (t
s
) một số ancol như sau:
Ancol Khối lượng phân tử t
s
(
o
C)
CH
3
OH 32 64,5
C
3
H
7
OH 60 82,4
C
2
H
4
(OH)
2
62 197,6
Công thức tính độ rượu:
Độ rượu =
Ví dụ: Cồn 96
o
nghĩa là
Trang 2
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Trong 100 ml cồn này thì có 96 ml C
2
H
5
OH.
3. Tính chất hoá học
Phản ứng thế H của nhóm OH (phản ứng với kim loại kiềm, phản ứng tạo phức với đồng(II)
hiđroxit của glixerol).
Ví dụ: Glixerol – một ancol no, đa chức mạch hở: phản ứng được với Na, hoà tan Cu(OH)
2
.
Phản ứng thế nhóm OH ancol (phản ứng với HX tạo dẫn xuất halogen, phản ứng giữa hai phân tử
ancol tạo ete).
Phản ứng este hoá với axit cacboxylic R – COOH.
Phản ứng tách nước tạo thành anken.
Phản ứng oxi hoá không hoàn toàn:
+ Ancol bậc I Anđehit, axit.
+ Ancol bậc II Xeton.
+ Ancol bậc III Không phản ứng.
Phản ứng oxi hoá hoàn toàn (Phản ứng cháy).
Ví dụ: Etanol có phản ứng với các chất: Na, K, HCl, HBr, CH
3
COOH, CuO, lên men giấm, tách nước ở
trên 170
o
C tạo etilen, dưới 170
o
C tạo đietyl ete.
Khi cháy:
Chú ý: Ancol no, mạch hở khi cháy:
4. Điều chế
Phương pháp điều chế etanol: thuỷ phân dẫn xuất halogen, hiđrat hoá etilen, lên men rượu glucozơ.
Trang 3
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
ANCOL
CẤU TẠO
Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
SƠ ĐỒ HỆ THỐNG HOÁ
Trang 4
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
TÍNH CHẤT
VẬT LÍ
ĐIỀU CHẾ
ỨNG DỤNG
Phân tử có nhóm OH gắn ở C no
Công thức chung:
C
n
H
2n+2-2k-a
(OH)
a
Ancol no, đơn chức:
C
n
H
2n+1
OH
Ancol no, đa chức: C
n
H
2n+2
O
x
hay
C
n
H
2n+2-x
(OH)
x
Đồng phân mạch C, vị trí nhóm
OH.
Tên thông thường: Ancol – tên
gốc hiđrocacbol + ic.
Tên theo IUPAC: Tên IUPAC của
hiđrocacbon + số chỉ vị trí OH +
ol (1)/ điol (2)/ triol (3)…
Ancol no, hở khi cháy:
Thế H ở OH bởi kim loại kiềm:
Số nhóm OH =
Ancol có từ 2 nhóm OH liền kề:
hoà tan Cu(OH)
2
tạo dung dịch
xanh lam
Phản ứng este hoá: thay thế H
trong nhóm OH bởi gốc axyl
RCO trong axit hữu cơ RCOOH
Tách HOH: Từ một phân tử, quy
tắc Zaixep, tạo liên kết bội; tách
nước từ 2 phân tử ete
Oxi hoá ancol bậc 1 tạo thành
anđehit;
Oxi hoá ancol bậc 2 tạo xeton;
Phản ứng lên men giấm
TÍNH CHẤT
HOÁ HỌC
Nhiệt độ sôi, độ tan trong
nước cao hơn hiđrocacbon
do có liên kết H giữa các
nhóm OH
Hiđrat hoá anken
Thuỷ phân dẫn xuất halogen bởi
kiềm
Hiđro hoá anđehit, xeton
Lên men rượu: được C
2
H
5
OH
C
2
H
5
OH: Làm dung môi, sản xuất
nước hoa, làm nhiên liệu, sát
trùng y tế…
Glixerol, C
3
H
5
(OH)
3
: dùng trong
công nghiệp sản xuất sơn, mực
in…
Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
II. CÁC DẠNG BÀI TẬP
Dạng 1: Cấu tạo, đồng phân, danh pháp, tính chất vật lí, ứng dụng
Kiểu hỏi 1: Ancol có tồn tại hay không? Công thức dãy đồng đẳng ancol
Phương pháp giải
Ancol là hợp chất chứa nhóm OH gắn ở nguyên tử C no.
Chú ý: OH gắn ở cacbon không no sẽ không bền, không tồn tại chuyển thành chất khác.
Mỗi C no chỉ chứa tối đa 1 nhóm OH. Nếu có trên 1 nhóm thì tách nước tạo anđehit hoặc axit.
Ví dụ: Ancol nào sau đây không tồn tại?
A. Xiclohexanol C
6
H
11
OH.
B. CH
2
= CHOH.
C. C
2
H
4
(OH)
2
.
D. (CH
3
)
3
C – OH.
Hướng dẫn giải
A, C, D đúng.
B sai vì OH gắn vào C không no nên không tồn tại, chuyển thành chất khác.
Chọn B.
Ví dụ mẫu
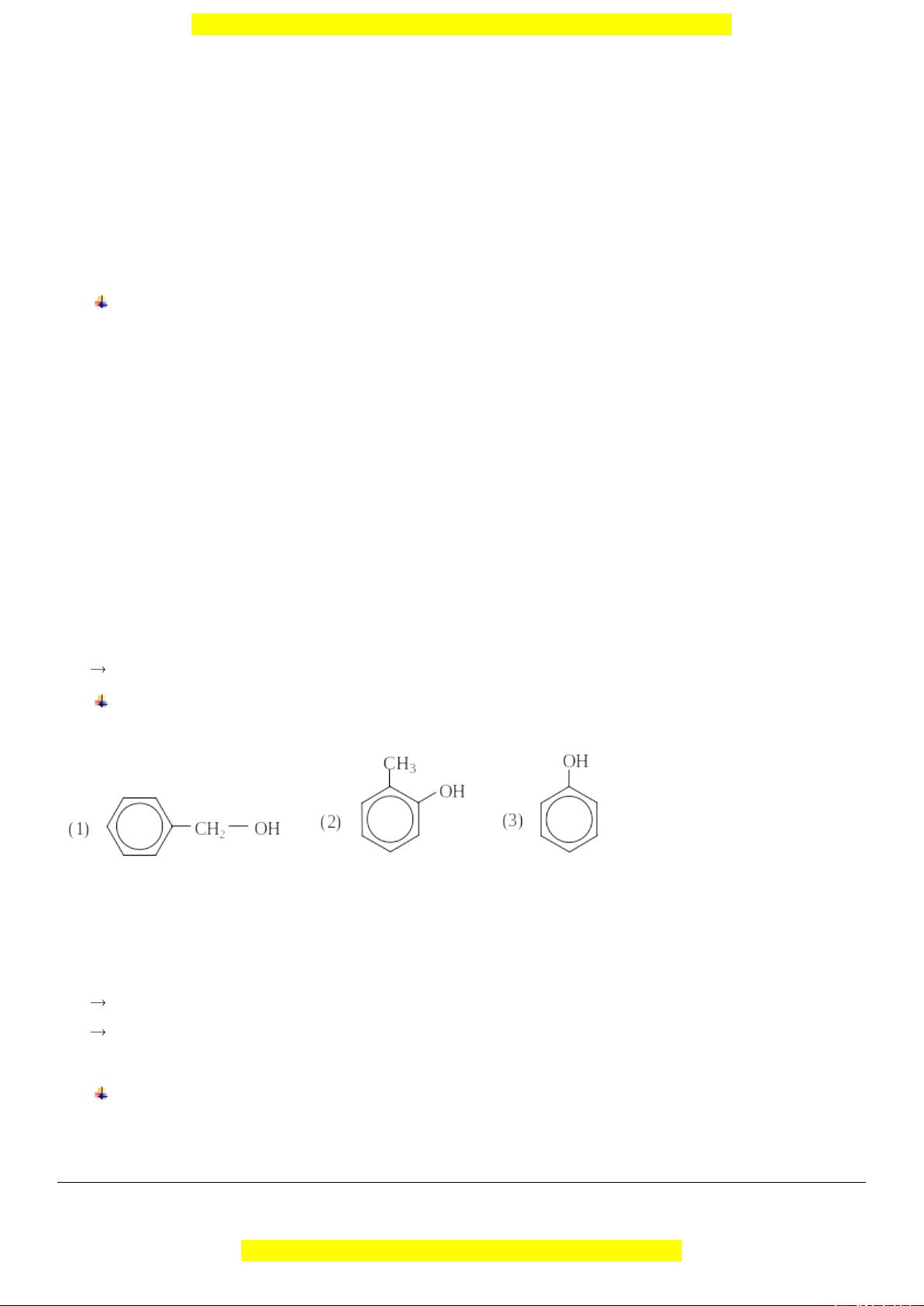
Ví dụ 1: Cho các chất có công thức cấu tạo:
Chất thuộc loại ancol là
A. (1) và (2). B. chỉ có (1). C. (1) và (3). D. cả (1), (2) và (3).
Hướng dẫn giải
Ancol là hợp chất chứa nhóm OH gắn ở nguyên tử C no.
Chỉ có (1) là ancol.
Chọn B.
Kiểu hỏi 2: Đếm số đồng phân ancol no mạch hở
Phương pháp giải
Viết các dạng mạch C; sau đó gắn OH vào những vị trí C khác nhau, chú ý tính đối xứng của mạch.
Chú ý: Cách viết đồng phân ete: Cũng mạch C như trên, ta đặt nguyên tử O vào giữa hai C.
Trang 5
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85