Chủ đề 2: TÍNH CHẤT, ỨNG DỤNG, ĐIỀU CHẾ ESTER
A. Kiến thức cần nắm vững 1) TÍNH CHẤT VẬT LÍ
- Các ester không tạo được liên kết hydrogen với nhau nên nhiệt độ sôi của ester thấp hơn so với
alcohol và carboxylic acid có cùng số nguyên tử .
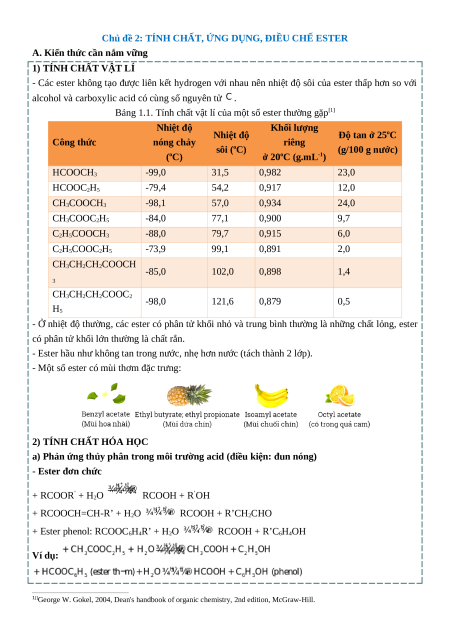
Bảng 1.1. Tính chất vật lí của một số ester thường gặp[1] Nhiệt độ Khối lượng Nhiệt độ Độ tan ở 25oC Công thức nóng chảy riêng sôi (oC) (g/100 g nước) (oC) ở 20oC (g.mL-1) HCOOCH3 -99,0 31,5 0,982 23,0 HCOOC2H5 -79,4 54,2 0,917 12,0 CH3COOCH3 -98,1 57,0 0,934 24,0 CH3COOC2H5 -84,0 77,1 0,900 9,7 C2H5COOCH3 -88,0 79,7 0,915 6,0 C2H5COOC2H5 -73,9 99,1 0,891 2,0 CH3CH2CH2COOCH -85,0 102,0 0,898 1,4 3 CH3CH2CH2COOC2 -98,0 121,6 0,879 0,5 H5
- Ở nhiệt độ thường, các ester có phân tử khối nhỏ và trung bình thường là những chất lỏng, ester
có phân tử khối lớn thường là chất rắn.
- Ester hầu như không tan trong nước, nhẹ hơn nước (tách thành 2 lớp).
- Một số ester có mùi thơm đặc trưng: 2) TÍNH CHẤT HÓA HỌC
a) Phản ứng thủy phân trong môi trường acid (điều kiện: đun nóng) - Ester đơn chức + RCOOR’ + H2O RCOOH + R’OH + RCOOCH=CH-R’ + H2O RCOOH + R’CH2CHO
+ Ester phenol: RCOOC6H4R’ + H2O RCOOH + R’C6H4OH Ví dụ:
1[]George W. Gokel, 2004, Dean's handbook of organic chemistry, 2nd edition, McGraw-Hill. - Ester 2 chức + (RCOO)2R’ + 2H2O 2RCOOH + R’(OH)2 + R(COOR’)2 + 2H2O R(COOH)2 + 2R’OH Ví dụ:
b) Phản ứng thủy phân trong môi trường kiềm (điều kiện: đun nóng) - Ester đơn chức + RCOOR’ + NaOH RCOONa + R’OH + RCOOCH=CH-R’ + NaOH RCOONa + R’CH2CHO
+ Ester phenol: RCOOC6H4R’ + 2NaOH RCOONa + R’C6H4ONa + H2O Ví dụ: - Ester 2 chức + (RCOO)2R’ + 2NaOH
2RCOONa + R’(OH)2; + R(COOR’)2 + 2NaOH R(COONa)2 + 2R’OH
+ Ít gặp: R1COOR2COOR’ + 2NaOH R1COONa + HOR2COONa + R’OH Ví dụ:
+ CH3COO-CH2CH2-OOC-C2H5 + 2NaOH CH3COONa + C2H5COONa + HO-CH2CHOH + CH3-OOC-COOC2H5 + 2NaOH NaOOC-COONa + CH3OH + C2H5OH + HCOOCH2COOCH3 + 2NaOH HCOONa + HOCH2COONa + CH3OH
c) Phản ứng không đặc trưng
+ Ester của formic acid có phản ứng với thuốc thử Tollens: HCOOR’ 2Ag
+ Ester không no, mạch hở, có phản ứng với H2 (Ni, to), và phản ứng làm mất màu dung dịch Br2.
Ví dụ: CH2 = CHCOOCH3 + 2H2 (dư) CH3-CH2COOCH3. 4) Điều chế
- Ester thường được điều chế bằng phản ứng ester hóa giữa carboxylic acid và alcohol, xúc tác
thường là acid H2SO4 đặc, đun nóng: RCOOH + R’OH RCOOR’ + H2O - Ví dụ: CH3COOC2H5 + H2O CH3COOH + C2H5OH
- Phản ứng cần đun nóng, dùng
nhiệt kế để đảm bảo nhiệt độ trong khoảng .
- Vai trò của H₂SO₄ đặc: xúc tác;
hút nước (làm tăng hiệu suất phản ứng điều chế ester).
- Đá bọt: giúp dung dịch sôi đều, chống trào.
- Dung dịch NaCl: giúp dung dịch
tách lớp nhanh và rõ rệt hơn. 5) Ứng dụng
Ester có nhiều ứng dụng trong công nghiệp. Làm dung môi Làm Nguyên liệu tổng hợp nhiều polymer sử dụng trong công nghiệp Làm chất tạo hương trong công nghiệp thực phẩm và mỹ phẩm
B. Câu hỏi và bài tập
Câu 1: Hoàn thành các phương trình hóa học sau: 1
C6H5COOCH3 (ester thơm) + H2O 2
CH2=CHCOOC6H5 (ester thơm) + H2O 3 CH3OOCCH2CH3 + H2O 4
C6H5COOCH2CH3 (ester thơm) + NaOH 5 CH2=CHOOCCH3 + NaOH 6
C6H5CH2OOCCH3 (ester thơm) + NaOH 7 CH3CH2COOCH=CH2 + NaOH 8 CH3COOCH2CH=CH2 + NaOH 9 CH3COOCH2CH2OOCC2H5 + NaOH 10 HCOOC3H6OOCCH2CH3 + NaOH 11 CH3OOCCH2COOC2H5 + NaOH 12 CH2=CHOOC-COOCH3+ NaOH 13
C6H5OOCC2H4COOCH3 (ester thơm) + NaOH 14 CH3COOCH2COOC2H5+ NaOH 15 HCOOC3H6OOCCH2CH3 + H2O 16 CH3OOCCH2COOC2H5 + H2O 17
C6H5OOCCH2CH2COOCH3 (ester thơm) + H2O 18 HCOOC6H5 (ester thơm)+ NaOH 19 CH3-OOC-COOCH3 + NaOH 20 CH3-COO-CH2-COO-C2H5+ NaOH 21 HCOO-CH2-CH2-OOC-CH3 + NaOH 22 CH3COO-C3H6-OOCH + NaOH 23
C6H5OOC-COO-CH3 (ester thơm) + NaOH 24
HCOO-C6H4-OOC-CH3 (ester thơm) + NaOH 25 CH2=CH-COOC2H5 + Br2
Câu 2: Propyl ethanoate là ester có mùi đặc trưng của quả lê, còn methyl butanoate là ester có
mùi đặc trưng của quả táo.
a) Viết công thức cấu tạo của propyl ethanoate và methylbutanoate.
b) Viết phương trình hoá học của phản ứng thuỷ phân propyl ethanoate và methyl
butanoate trong môi trường acid và môi trường base.
Câu 3: Hoàn thành sơ đồ phản ứng sau:
Câu 4: Cho salicylic acid (hay 2-hydroxybenzoic acid) phản ứng với methyl alcohol, có mặt
sulfuric acid làm xúc tác, thu được methyl salicylate (C8H8O3) dùng làm chất giảm đau
(có trong miếng dán giảm đau khi vận động hoặc chơi thể thao). Viết phương trình hoá
học của phản ứng trên.
Câu 5: Hoàn thành bảng sau: STT PHÁT BIỂU Đ/S ĐỀ XUẤT SỬA 1
Benzyl acetate có mùi thơm của hoa nhài, công thức cấu tạo là
Chuyên đề dạy thêm Chủ đề 2: Tính chất - ứng dụng - điều chế ester Hóa học 12 (sách mới)
1 K
506 lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Tailieugiaovien.com.vn giới thiệu Chuyên đề dạy thêm Hóa học lớp 12 dành cho cả 3 sách mới nhằm giúp Giáo viên có thêm tài liệu tham khảo tài liệu môn Hóa học 12.
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(1012 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)