Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t ế (có l i ờ gi i ả ) SỞ GIÁO D C Ụ VÀ ĐÀO KỲ THI CH N Ọ H C Ọ SINH GI I Ỏ TẠO CẤP T NH Ỉ L P Ớ 12 THPT NĂM H C Ọ 2022- BÌNH PHƯ C Ớ 2023 MÔN HÓA H C Ọ Đ Ề CHÍNH TH C Ứ Câu 1 (2 đi m ể ): 1.1. Cho r ng ằ Sb có 2 đ n
ồ g vị 121Sb và 123Sb, kh i ố lư n ợ g nguyên t ử trung bình c a ủ Sb là 121,75. Hãy tính ph n ầ trăm v ề kh i ố lư n ợ g c a ủ đ n
ồ g vị 121Sb trong Sb2O3 ? Cho nguyên
tử khối trung bình của O = 16.
1.2. Cân bằng các ph n ả ng ứ sau theo phư ng ơ pháp thăng b ng ằ electron:
a) Al + HNO3 Al(NO3)3 + N2O + NO + H2O Trong đó t ỉ l ệ mol khí N2O : NO = 1 : a. 0 b) FeS t 2 + H2SO4 (đ) Fe2(SO4)3 + SO2 + H2O Câu 2 (2 đi m ể ): 2.1. Vi t ế phư ng ơ
trình phản ứng cho các thí nghi m ệ sau: - Thí nghi m ệ 1: Cho hỗn h p
ợ gồm Cu và Fe3O4 (tỉ lệ mol 1:1) vào dung d c ị h H2SO4 loãng d . ư - Thí nghi m ệ 2: Cho Ba vào dung d c ị h NH4HCO3. Khi phản ng ứ k t ế thúc, thí nghi m ệ nào thu đư c ợ ch t ấ r n, ắ gi i ả thích? 2.2. Dung dịch X ch a ứ đ ng ồ th i ờ hai mu i
ố MgCl2 0,004M và FeCl3 0,001M. Cho dung dịch NaOH vào X. K t ế t a ủ nào t o ạ ra trư c
ớ ? Tìm giá trị pH thích h p ợ để tách 11 39 1 trong 2 ion: Mg2+ ho c ặ Fe3+ ra kh i ỏ dung dịch? Cho T = 10 T = 10 Mg(OH)2 ; Fe(OH)3 . Bi t ế rằng, n u ế nồng đ ộ ion b ng ằ 10-6M thì coi nh ư đã h t. ế Câu 3 (2 đi m ể ): 3.1. Xét cân b ng ằ hóa h c
ọ : 2SO2 (k) + O2 (k)
2SO3 (k); ∆H < 0. Cân b ng ằ hóa h c ọ trên sẽ chuy n ể dịch theo chi u ề nào trong các trư ng ờ h p ợ dư i ớ đây? a) Tăng nhi t ệ đ ộ c a ủ h . ệ b) Giảm áp su t ấ c a ủ h . ệ
Em hãy giải thích ngắn g n. ọ M i ọ thắc m c
ắ vui lòng xin liên h h
ệ otline: 084 283 45 85
Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t ế (có l i ờ gi i ả ) 3.2. Trong m t ộ bình kín có cân b ng ằ hóa h c ọ sau: 2NO2 (k) N2O4 (k). Tỉ khối h i ơ của hỗn h p ợ khí trong bình so v i ớ H2 ở nhi t ệ độ T1 bằng 27,6 và ở nhi t ệ độ T2 bằng 34,5. Bi t
ế T1> T2. Phản ứng thuận thu hay t a ỏ nhi t ệ ? Câu 4: ( 2,0 đi m ể ) 4.1. Có 5 ng ố nghi m, ệ m i ỗ ng ố nghi m ệ ch a ứ m t ộ trong các dung d c ị h sau: Na2SO4,
Ba(HCO3)2, Ba(OH)2, KHCO3, NaHSO4. Ngư i ờ ta đánh số ng u ẫ nhiên t ng ừ ng ố
nghiệm là (1), (2), (3), (4), (5) và ti n ế hành thí nghi m ệ cho k t ế qu ả nh ư sau: - Cho dung d c ị h (1) vào dung d c ị h (2) thấy v a ừ t o ạ k t ế t a ủ tr ng, ắ v a ừ có khí thoát ra.
- Cho dung dịch (2) vào các dung d c ị h (3) và (4) đ u ề có k t ế t a ủ .
- Cho dung dịch (3) vào dung d c ị h (5) có k t ế t a ủ . Xác đ nh ị các dung d c
ị h (1), (2), (3), (4), (5) ? 4.2. Cho 2,16 gam b t ộ Mg tác d ng ụ v a ừ đủ v i ớ 500 ml dung d c ị h HNO3 xM thu đư c ợ dung d c
ị h Y và 0,448 lít (đktc) m t ộ ch t
ấ khí không màu hóa nâu trong không
khí. Tính x và khối lư ng
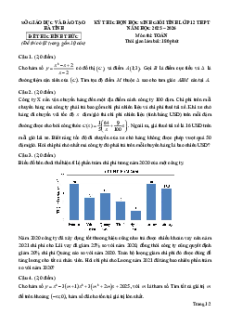
ợ muối tạo thành trong Y? Câu 5 (2 đi m ể ): Hòa tan m gam h n ỗ h p ợ CuSO4 và KCl vào nư c ớ thu đư c ợ dung d c ị h X. Đi n ệ phân dung d c ị h X v i ớ cư ng ờ độ dòng đi n ệ không đ i ổ (đi n ệ c c ự tr , ơ màng ngăn xốp). Th ể tích khí V (lít, đo
ở đktc) thoát ra theo th i ờ gian (t) đư c ợ bi u ể di n ễ theo đồ thị bên dư i. ớ N u ế d ng ừ đi n ệ phân ở th i ờ đi m ể 250 giây thì thu đư c ợ dung d c ị h Y. Nhúng thanh nhôm (d ) ư vào Y, sau khi ph n ả ng ứ hoàn toàn thu đư c ợ dung d c ị h Z. a) Lập lu n ậ xác đ nh
ị khí nào thoát ra ở các giai đo n ạ đi n ệ phân tư ng ơ ng ứ v i ớ các đo n ạ OA, AB và BC? b) Khối lư ng ợ dung d c ị h Z thay đ i ổ nh ư th ế nào so v i ớ dung d c ị h Y? M i ọ thắc m c
ắ vui lòng xin liên h h
ệ otline: 084 283 45 85
Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t ế (có l i ờ gi i ả ) Câu 6 (2 đi m ể ): 6.1. Vi t ế các đ ng ồ phân c u ấ t o ạ (b n) ề m c ạ h h ở c a ủ h p ợ ch t ấ có công th c ứ phân tử C3H6O? 6.2. Sắp x p
ế lực bazơ giảm dần của các ch t ấ có vòng benzen sau:
m-CH3C6H4NH2, p-CH3C6H4NH2, o-CH3C6H4NH2, p-O2NC6H4NH2, p-ClC6H4NH2. Giải thích? Câu 7 (2 đi m ể ): Hỗn h p ợ X ch a ứ b n ố hidrocacbon đ u ề m c ạ h hở và có công th c ứ
dạng CnH4 (n < 4). Đốt cháy hoàn toàn 5,96 gam X trong oxi thu đư c ợ 0,43 mol CO2. Tr n ộ 5,96 gam X v i
ớ 0,24 gam H2, sau đó nung m t ộ th i
ờ gian (xúc tác Ni) thu đư c ợ 62 hỗn h p ợ khí Y có tỉ kh i ố so v i ớ He bằng 9 . Dẫn Y l n ầ lư t ợ qua bình 1 đ ng ự dung
dịch AgNO3/NH3 dư thu đư c ợ m gam k t ế t a ủ , bình 2 ch a ứ dung d c ị h brom d , ư th y ấ lư ng ợ
brom phản ứng là 0,065 mol. a. Xác đ nh ị công th c ứ c u ấ t o ạ c a ủ bốn hidrocacbon trong X? b. Tính giá trị c a ủ m? Câu 8 (2 đi m ể ): 8.1. H p ợ ch t ấ h u ữ cơ X có công th c
ứ phân tử là C2H9N3O6, tác d ng ụ đư c ợ v i ớ HCl
và KOH. Cho 51,3 gam X phản ứng v i ớ dung d c ị h ch a ứ 48 gam NaOH. Sau khi ph n ả
ứng xảy ra hoàn toàn, cô c n ạ cẩn th n ậ dung d c ị h thu đư c ợ m gam chất rắn khan. Tính giá trị c a ủ m? 8.2. Vi t ế phư ng ơ trình hóa h c ọ cho các trư ng ờ h p ợ sau, ghi rõ đi u ề ki n ệ (n u ế có):
a. Thủy phân saccarozo trong dung d c ị h H2SO4 loãng. b. Trùng ng ng ư axit ađipic v i ớ hexametylenđiamin. c. Trùng h p ợ metyl metacrylat. d. Cho Gly-Ala tác d ng ụ v i ớ dung d c ị h HCl d , ư t0. Câu 9 (2 điểm): 9.1. Cho các phư ng ơ trình hóa h c ọ sau (v i ớ h ệ s ố t ỉl ệ đã cho): 0 (1) A + 2NaOH t
B + C + CH3CHO. 0 (2) B + 2AgNO t 3 +3NH3 + H2O C2H4NO4Na + 2Ag↓ + 2NH4NO3. 0 (3) C + HC1 t C3H6O3 + NaCl. Bi t
ế A có mạch cacbon không phân nhánh. Xác đ nh ị công th c ứ c u ấ t o ạ thu g n ọ của A, B, C. M i ọ thắc m c
ắ vui lòng xin liên h h
ệ otline: 084 283 45 85
Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t ế (có l i ờ gi i ả ) 9.2. Hỗn h p ợ E g m ồ X và Y đ u ề là các h p ợ ch t ấ h u ữ cơ no, m c ạ h h , ở chỉ ch a ứ nhóm ch c ứ este, trong đó X (đ n ơ ch c ứ ) và Y (hai ch c ứ ); MX < MY. Th y ủ phân hoàn toàn 10,56 gam h n ỗ h p ợ E trong dung d c ị h NaOH (v a ừ đ ) ủ , cô c n ạ dung d c ị h sau phản ứng thu đư c ợ hỗn h p ợ Z g m
ồ hai ancol và 12,12 gam h n ỗ h p ợ ch t ấ r n ắ T g m ồ 3 ch t ấ h u ữ c . ơ Đ t
ố cháy hoàn toàn T thu đư c
ợ 0,07 mol Na2CO3, 0,21 mol CO2 và
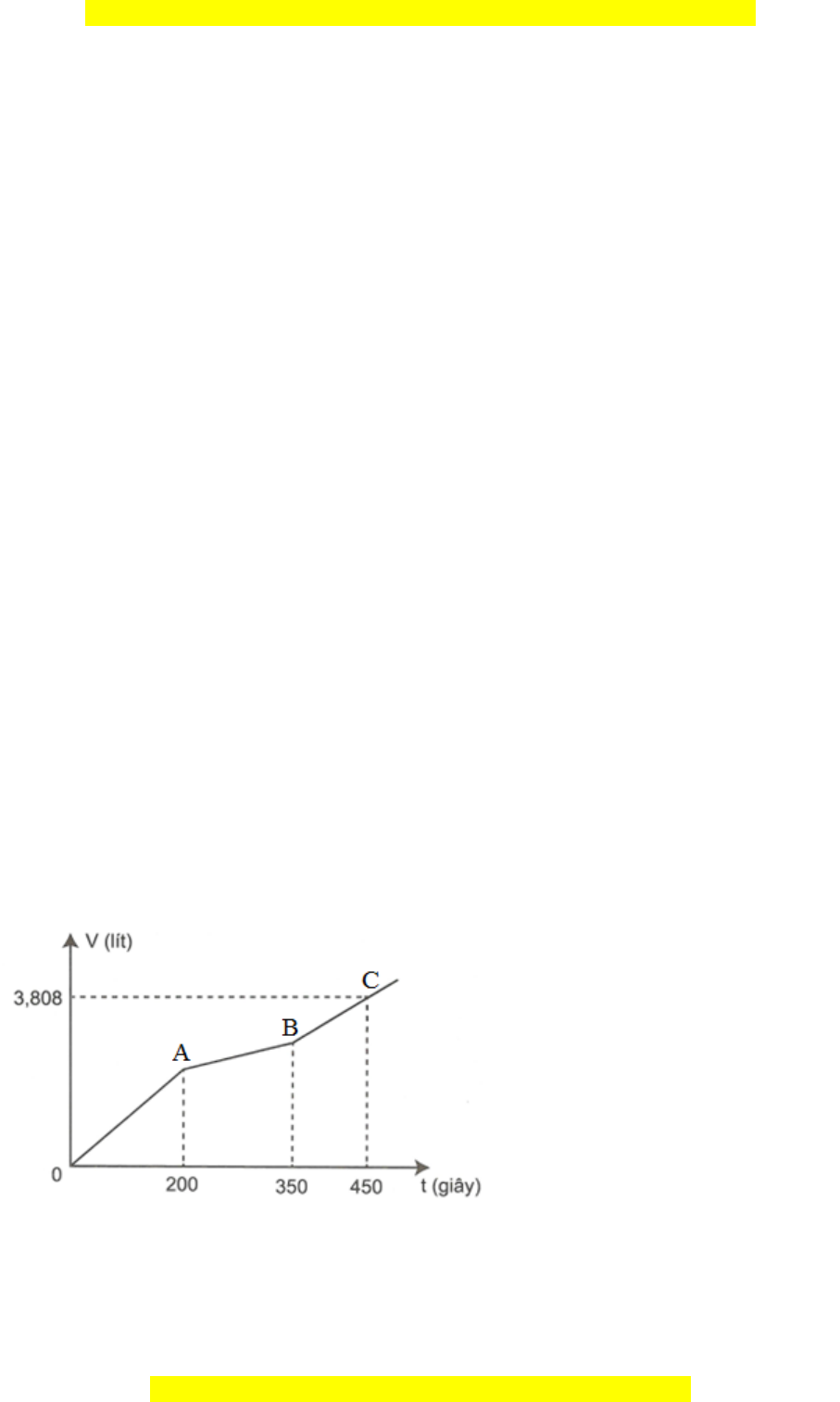
0,21 mol H2O. Tính phần trăm kh i ố lư ng ợ c a ủ Y trong E? Câu 10 (2 đi m ể ): 10.1. Khi n n ồ g đ ộ axit trong d c ị h v ịd ạ dày tăng có th ể gây ra viêm loét d ạ dày, tá tràng. Để gi m ả b t ớ n n ồ g độ axit trong d c ị h vị dạ dày ngư i ờ ta thư n ờ g dùng “thu c ố đau dạ dày” trong thành ph n ầ có mu i ố X. Xác đ nh ị công th c ứ hóa h c ọ c a ủ mu i ố X? Vi t ế phư ng ơ trình hóa h c ọ c a ủ muối X v i ớ axit trong d c ị h v ịd ạ dày? 10.2. Cho hình v ẽ mô t ả thí nghi m: ệ Nêu và gi i ả thích các hi n ệ tư ng ợ x y ả ra trong thí nghi m ệ ?
Lưu ý: Thí sinh làm bài theo cách khác, n u ế đúng v n ẫ đ t ạ đi m ể t i ố đa. . . . . . H T Ế . . . . . M i ọ thắc m c
ắ vui lòng xin liên h h
ệ otline: 084 283 45 85
Đề HSG Hóa 12 Bình Phước năm 2023 có đáp án
1.7 K
855 lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Tài liệu được cập nhật liên tục trong gói này từ nay đến hết tháng 3/2024. Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Tailieugiaovien.com.vn giới thiệu Đề HSG Hóa 12 Bình Phước năm 2023 có đáp án.
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(1709 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN Hóa Học
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Lớp 12
Xem thêmTài liệu bộ mới nhất

Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có l i gi i)ả ử ệ ể ế ờ ả
SỞ GIÁO D C VÀ ĐÀOỤ
T OẠ
BÌNH PH CƯỚ
KỲ THI CH N H C SINH GI IỌ Ọ Ỏ
C P T NH L P 12 THPT NĂM H C 2022-Ấ Ỉ Ớ Ọ
2023
MÔN HÓA H CỌ
Đ CHÍNH TH CỀ Ứ
Câu 1 (2 đi m):ể
1.1. Cho r ng ằ Sb có 2 đ ng v ồ ị
121
Sb và
123
Sb, kh i l ng nguyên t trung bình c a Sb làố ượ ử ủ
121,75. Hãy tính ph n trăm v kh i l ng c aầ ề ố ượ ủ đ ng vồ ị
121
Sb trong Sb
2
O
3
? Cho nguyên
t kh i trung bình c a O = 16. ử ố ủ
1.2. Cân b ng ằ các ph n ng sau theo ph ng pháp thăng b ng electron:ả ứ ươ ằ
a) Al + HNO
3
Al(NO
3
)
3
+ N
2
O + NO + H
2
O
Trong đó t l mol khí Nỉ ệ
2
O : NO = 1 : a.
b) FeS
2
+ H
2
SO
4 (đ)
0
t
Fe
2
(SO
4
)
3
+ SO
2
+ H
2
O
Câu 2 (2 đi m):ể
2.1. Vi t ph ng trình ph n ng cế ươ ả ứ ho các thí nghi m ệ sau:
- Thí nghi m 1: ệ Cho hỗn h p gợ ồm Cu và Fe
3
O
4
(t l mol 1:1) vào dung d chỉ ệ ị
H
2
SO
4
loãng d .ư
- Thí nghi m 2: ệ Cho Ba vào dung d ch NHị
4
HCO
3
.
Khi ph n ng k t ả ứ ế thúc, thí nghi m nào thu đ c ch t r n, gi i ệ ượ ấ ắ ả thích?
2.2. Dung d ch ị X ch a đ ng th i hai mu i MgClứ ồ ờ ố
2
0,004M và FeCl
3
0,001M. Cho
dung d chị NaOH vào X. K t t a nào t o ra tr c ? ế ủ ạ ướ Tìm giá trị pH thích h p đ táchợ ể
1 trong 2 ion: Mg
2+
ho c Feặ
3+
ra kh i dung ỏ d ch?ị Cho
2
11
Mg(OH)
T = 10
;
3
39
Fe(OH)
T = 10
.
Bi t ế r ng,ằ n u n ng đ ion b ng 10ế ồ ộ ằ
-6
M thì coi nh đã h t.ư ế
Câu 3 (2 đi m):ể
3.1. Xét cân b ng hóa h c: 2SOằ ọ
2
(k)
+ O
2
(k)
2SO
3
(k)
; ∆H < 0. Cân b ng hóa h cằ ọ
trên s chuy n d ch theo chi u nàoẽ ể ị ề trong các tr ng h p d i đây?ườ ợ ướ
a) Tăng nhi t đ c a h .ệ ộ ủ ệ
b) Gi m áp su t c a h .ả ấ ủ ệ
Em hãy gi i ả thích ng n g n.ắ ọ
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ
Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có l i gi i)ả ử ệ ể ế ờ ả
3.2. Trong m t bình kín có cân b ng hóa h c sau: 2NOộ ằ ọ
2
(k)
N
2
O
4
(k)
. T kh i h iỉ ố ơ
c a h n h p ủ ỗ ợ khí trong bình so v i Hớ
2
nhi t đ Tở ệ ộ
1
b ng 27,6 và nhi t đ Tằ ở ệ ộ
2
b ngằ
34,5. Bi t Tế
1
> T
2
. Ph n ng thu n thu hay t a nhi t?ả ứ ậ ỏ ệ
Câu 4: ( 2,0 đi m)ể
4.1. Có 5 ng nghi m, m i ng nghi m ch a ố ệ ỗ ố ệ ứ m tộ trong các dung d ch sau: Naị
2
SO
4
,
Ba(HCO
3
)
2
, Ba(OH)
2
, KHCO
3
, NaHSO
4
. Ng i ta đánh s ng u nhiên t ng ngườ ố ẫ ừ ố
nghi m là ệ (1), (2), (3), (4), (5) và ti n hành thí nghi m cho k t qu nh sau:ế ệ ế ả ư
- Cho dung d ch ị (1) vào dung d ch ị (2) th y v a t o k t t a tr ng, v a có khí thoátấ ừ ạ ế ủ ắ ừ
ra.
- Cho dung d ch ị (2) vào các dung d ch ị (3) và (4) đ u có k t t a.ề ế ủ
- Cho dung d ch ị (3) vào dung d ch ị (5) có k t t a. ế ủ
Xác đ nh các dung d ch ị ị (1), (2), (3), (4), (5) ?
4.2. Cho 2,16 gam b t Mg tác d ng v a đ v i 500ộ ụ ừ ủ ớ ml dung d ch HNOị
3
xM thu
đ c dung d ch Y và 0,448 lít (đktc) m t ch t khí không màu hóa nâu trong khôngượ ị ộ ấ
khí. Tính x và kh i l ng mu i t o thành trong Y?ố ượ ố ạ
Câu 5 (2 đi m):ể
Hòa tan m gam h n h p CuSOỗ ợ
4
và KCl vào n c thu đ c dung d ch X. Đi nướ ượ ị ệ
phân dung d ch X v i c ng đ dòng đi n không đ i (đi n c c tr , màng ngănị ớ ườ ộ ệ ổ ệ ự ơ
x p). Th tích khí V (lít, đo đktc) thoát ra theo th i gian (t) đ c bi u di n theo đố ể ở ờ ượ ể ễ ồ
th bên d i. N u d ng đi n phân th i đi m 250 giây thì thu đ c dung d ch Y.ị ướ ế ừ ệ ở ờ ể ượ ị
Nhúng thanh nhôm (d ) vào Y, sau khi ph n ng hoàn toàn thu đ c dung d ch Z. ư ả ứ ượ ị
a) L p lu n xác đ nh khí nào thoát ra các giai đo n đi n phân t ng ngậ ậ ị ở ạ ệ ươ ứ
v i các đo n OA, AB và BC?ớ ạ
b) Kh i l ng dung d ch Z thay đ i nh th nào so v i dung d ch Y?ố ượ ị ổ ư ế ớ ị
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ

Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có l i gi i)ả ử ệ ể ế ờ ả
Câu 6 (2 đi m):ể
6.1. Vi t các đ ng phân c u t o (b n) m ch h c a h p ch t cóế ồ ấ ạ ề ạ ở ủ ợ ấ công th c phân tứ ử
C
3
H
6
O?
6.2. S p x pắ ế l c bazự ơ gi m d nả ầ c a các ch t có vòng benzen sau: ủ ấ
m-CH
3
C
6
H
4
NH
2
, p-CH
3
C
6
H
4
NH
2
, o-CH
3
C
6
H
4
NH
2
, p-O
2
NC
6
H
4
NH
2
, p-ClC
6
H
4
NH
2
.
Gi i thích?ả
Câu 7 (2 đi m)ể : H n h p X ch a b n hidrocacbon đ u m ch h và có công th cỗ ợ ứ ố ề ạ ở ứ
d ng Cạ
n
H
4
(n < 4). Đ t cháy ố hoàn toàn 5,96 gam X trong oxi thu đ c 0,ượ 43 mol CO
2
.
Tr n ộ 5,96 gam X v i 0,24 ớ gam H
2
, sau đó nung m t th i gian (xúc tác Ni) thu đ cộ ờ ượ
h n h p khí Y có t kh i so v i He ỗ ợ ỉ ố ớ b ngằ
62
9
. D n Y l n l t qua bình 1 đ ng dungẫ ầ ượ ự
d ch AgNOị
3
/NH
3
d thu đ c m gam k t t a, bình 2 ch a dung d ch brom d , th yư ượ ế ủ ứ ị ư ấ
l ng brom ph n ng là 0,065 mol.ượ ả ứ
a. Xác đ nh công th c c u t o c a ị ứ ấ ạ ủ b n hidrocacbonố trong X?
b. Tính giá tr c a m?ị ủ
Câu 8 (2 đi m):ể
8.1. H p ch t h u c ợ ấ ữ ơ X có công th c phân t là ứ ử C
2
H
9
N
3
O
6
, tác d ngụ đ cượ v i HClớ
và KOH. Cho 51,3 gam X ph n ngả ứ v i dung d ch ch a 48 gam NaOH. Sau khi ph nớ ị ứ ả
ng x y ra hoàn toàn, cô c nứ ả ạ c n th nẩ ậ dung d ch thu đ c m gamị ượ ch tấ r nắ khan.
Tính giá tr c a ị ủ m?
8.2. Vi t ph ng trình hóa h c cho các ế ươ ọ tr ng h pườ ợ sau, ghi rõ đi u ki n (n u có)ề ệ ế :
a. Th y phân saccarozo trong dung d ch Hủ ị
2
SO
4
loãng.
b. Trùng ng ng axit ađipic v i hexametylenđiamin.ư ớ
c. Trùng h p metyl metacrylat.ợ
d. Cho Gly-Ala tác d ng v i dung d ch HCl ụ ớ ị d , tư
0
.
Câu 9 (2 đi m)ể :
9.1. Cho các ph ng trình hóa h c sau (v i h s t l đã cho):ươ ọ ớ ệ ố ỉ ệ
(1) A + 2NaOH
0
t
B + C + CH
3
CHO.
(2) B + 2AgNO
3
+3NH
3
+ H
2
O
0
t
C
2
H
4
NO
4
Na + 2Ag↓ + 2NH
4
NO
3
.
(3) C + HC1
0
t
C
3
H
6
O
3
+ NaCl.
Bi t ế A có m ch cacbon không phân nhánh. ạ Xác đ nh công th c c u t o thu g nị ứ ấ ạ ọ
c a ủ A, B, C.
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ
Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có l i gi i)ả ử ệ ể ế ờ ả
9.2. H n h p E g m X và Y đ u là các h p ch t h u c no, m ch h , ch ch aỗ ợ ồ ề ợ ấ ữ ơ ạ ở ỉ ứ
nhóm ch c este, trong đó X (đ n ch c) và Y (hai ch c); Mứ ơ ứ ứ
X
< M
Y
. Th y phân hoànủ
toàn 10,56 gam h n h p E trong dung d ch NaOH (v a đ ), cô c n dung d ch sauỗ ợ ị ừ ủ ạ ị
ph n ng thu đ c h n h p Z g m hai ancol và 12,12 gam h n h p ch t r n T g mả ứ ượ ỗ ợ ồ ỗ ợ ấ ắ ồ
3 ch t h u c . Đ t cháy hoàn toàn T thu đ c 0,07 mol Naấ ữ ơ ố ượ
2
CO
3
, 0,21 mol CO
2
và
0,21 mol H
2
O. Tính ph n trăm kh i l ng c a Y trong E?ầ ố ượ ủ
Câu 10 (2 đi m):ể
10.1. Khi n ng đ axit trong d ch v d dày tăng có th gây ra viêm loét d dày, tá tràng.ồ ộ ị ị ạ ể ạ
Đ gi m b t n ng đ axit trong d ch v d dày ng i ta th ng dùng “thu c đau dể ả ớ ồ ộ ị ị ạ ườ ườ ố ạ
dày” trong thành ph n có mu i X.ầ ố Xác đ nh cị ông th c hóa h c c a mu i X? Vi tứ ọ ủ ố ế
ph ng trình hóa h c c a mu i X v i axit trong d ch v d ươ ọ ủ ố ớ ị ị ạ dày?
10.2. Cho hình v mô t thí nghi m:ẽ ả ệ
Nêu và gi i thích các hi n t ng x y ra trong thí nghi m?ả ệ ượ ả ệ
L u ý:ư Thí sinh làm bài theo cách khác, n u đúng v n đ t đi m t i đa. ế ẫ ạ ể ố
. . . . . H T . . . . .Ế
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ

Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có l i gi i)ả ử ệ ể ế ờ ả
S GIÁO D C VÀ ĐÀOỞ Ụ
T OẠ
BÌNH PH CƯỚ
KỲ THI CH N H C SINH GI IỌ Ọ Ỏ
C P T NH L P 12 THPT NĂM H C 2022-Ấ Ỉ Ớ Ọ
2023
ĐÁP ÁN VÀ H NG D N CH M MÔN HÓA H CƯỚ Ẫ Ấ Ọ
Đ CHÍNH TH CỀ Ứ
Câu 1 (2 đi m):ể
1.1. Cho r ng ằ Sb có 2 đ ng v ồ ị
121
Sb và
123
Sb, kh i l ng nguyên t trung bình c a Sb làố ượ ử ủ
121,75. Hãy tính ph n trăm v kh i l ng c aầ ề ố ượ ủ đ ng vồ ị
121
Sb trong Sb
2
O
3
? Cho nguyên
t kh i trung bình c a O = 16. ử ố ủ
1.2. Cân b ng ằ các ph n ng sau theo ph ng pháp thăng b ng electron:ả ứ ươ ằ
a) Al + HNO
3
Al(NO
3
)
3
+ N
2
O + NO + H
2
O
Trong đó t l mol khí Nỉ ệ
2
O : NO = 1 : a.
b) FeS
2
+ H
2
SO
4 (đ)
0
t
Fe
2
(SO
4
)
3
+ SO
2
+ H
2
O
Câu 1 N i dungộ Đi mể
1.1 G i x, y l n l t là % đ ng v ọ ầ ượ ồ ị
121
Sb và
123
Sb
Ta có: x + y = 100 và 121x + 123y = 121,75*100
x = 62,5%; y = 37,5%
Kh i l ng mol phân t c a Sbố ượ ử ủ
2
O
3
là 291,5 g/mol
%
121
Sb =
121.2 . 0,625.100
291,5
= 51,89%
0,5
0,5
1.2 a)
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ