Sở GD - ĐT …
ĐỀ KIỂM TRA GIỮA HỌC KÌ I TRƯỜNG THPT … Năm học: …. Môn: Hóa học 11 Mã đề thi: 002
Bộ: Chân trời sáng tạo
Thời gian làm bài: 60 phút;
(28 câu trắc nghiệm – 3 câu tự luận)
(Học sinh không được sử dụng tài liệu)
Họ, tên học sinh:.....................................................................
Lớp: ............................. Đề bài:
Phần I: Trắc nghiệm (7 điểm)
* Mức độ nhận biết
Câu 1: Tại nhiệt độ không đổi, ở trạng thái cân bằng thì
A. nồng độ của các chất trong hỗn hợp phản ứng không thay đổi.
B. nồng độ của các chất trong hỗn hợp phản ứng vẫn liên tục thay đổi.
C. phản ứng hoá học không xảy ra.
D. tốc độ phản ứng hoá học xảy ra chậm dần.
Câu 2: Yếu tố nào sau đây luôn luôn không làm dịch chuyển cân bằng của hệ phản ứng? A. Nhiệt độ B. Áp suất C. Nồng độ D. Chất xúc tác
Câu 3: Sự điện li là
A. quá trình phân huỷ các chất thành chất mới khi hoà tan vào nước.
B. quá trình kết hợp giữa các ion thành phân tử trong dung dịch.
C. quá trình phản ứng giữa các ion tạo ra chất kết tủa.
D. quá trình phân li thành ion của các chất tan khi tan vào nước.
Câu 4: Trường hợp nào sau đây không dẫn điện được?
A. Dung dịch NaCl.
B. NaOH nóng chảy.
C. Dung dịch HCl. D. NaCl rắn khan.
Câu 5: Chất nào sau đây không phải là chất điện li? A. C2H4. B. KCl. C. HCl. D. KOH.
Câu 6: Giá trị pH của một dung dịch được tính theo biểu thức nào sau đây? A. pH = −log[H+]. B. pH = log[H+]. C. pH = −log[OH−]. D. pH = log[OH−]
Câu 7: “Đất phèn” là một khái niệm dân gian để chỉ loại đất chứa nhiều ion
sulfate, có pH < 7. Môi trường của đất phèn là
A. môi trường base.
B. môi trường trung tính.
C. môi trường acid.
D. môi trường trung hoà.
Câu 8: Theo thuyết của Bronsted – Lowry thì acid là chất A. cho proton.
B. tan trong nước phân li ra H+. C. nhận proton.
D. tan trong nước phân li ra OH−.
Câu 9: Trong tự nhiên, nguyên tố nitrogen (N) tồn tại ở dạng
A. đơn chất và hợp chất. B. đơn chất.
C. hợp chất hữu cơ.
D. hợp chất vô cơ.
Câu 10: Số oxi hoá của nitrogen trong hợp chất NH4Cl là A. – 3. B. +3. C. – 4. D. +4.
Câu 11: Dạng hình học của phân tử ammonia là
A. hình tam giác đều.
B. hình tứ diện đều. C. đường thẳng.
D. hình chóp tam giác.
Câu 12: Cho vài giọt quỳ tím vào dung dịch NH3 thì dung dịch chuyển thành A. màu hồng. B. màu vàng. C. màu đỏ. D. màu xanh.
Câu 13: Để tạo độ xốp cho một số loại bánh, có thể dùng muối nào sau đây làm bột nở? A. (NH4)2SO4. B. NH4HCO3. C. CaCO3. D. NH4NO2.
Câu 14: Muối nào sau đây tan tốt trong nước? A. BaCO3. B. CaSO4. C. NH4Cl. D. AgCl.
Câu 15: Vai trò của NH3 trong phản ứng oxi hoá – khử là A. tính khử. B. tính oxi hóa. C. tính base. D. tính acid.
Câu 16: Nhóm các kim loại đều phản ứng được với HNO3 là A. Al, Cu, Au. B. Mg, Zn, Cu. C. Mg, Au, Fe. D. Ag, Pt, Au.
* Mức độ thông hiểu
Câu 17: Xét các cân bằng sau:
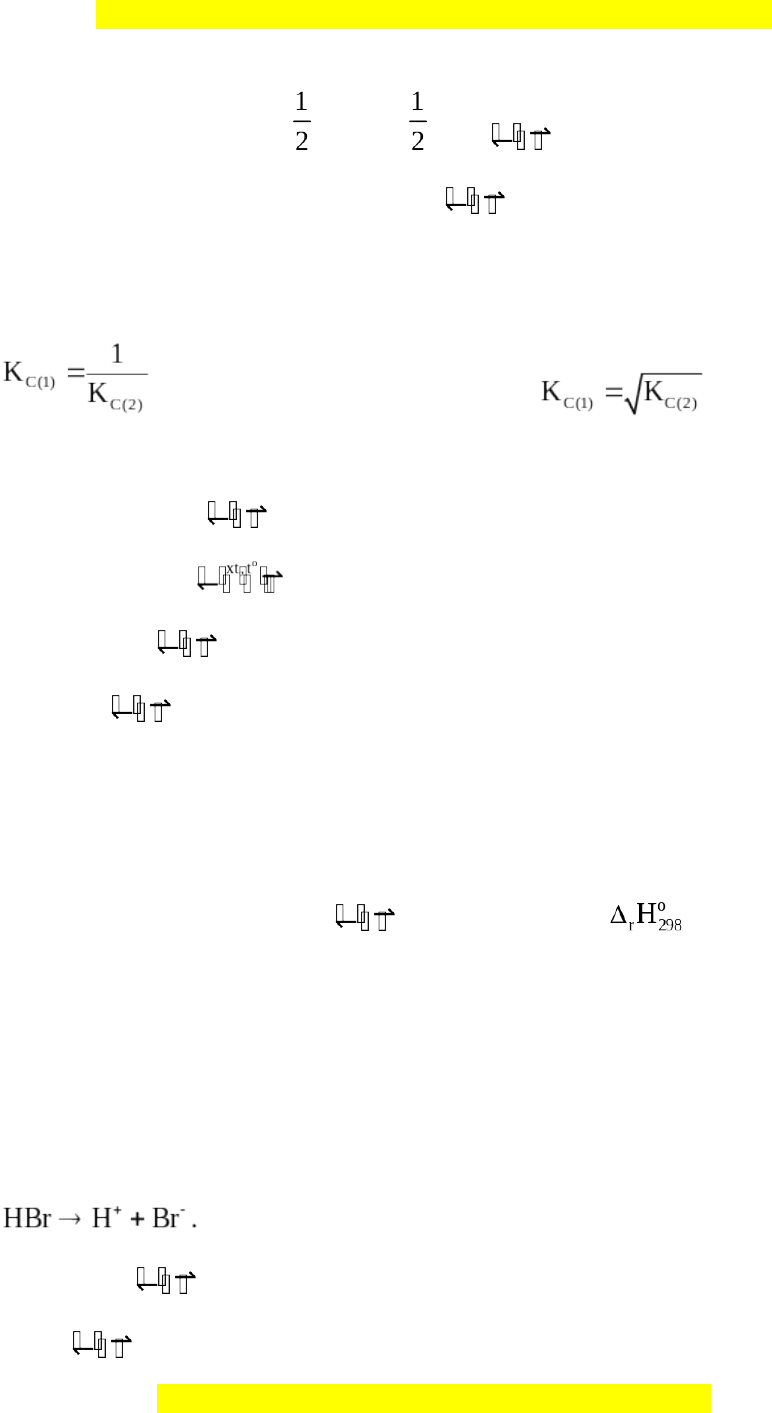
(1) H2(g) + I2(g) HI(g) KC(1) (2) H2(g) + I2(g) 2HI(g) KC(2)
Mối quan hệ giữa KC(1) và KC(2) là A. KC(1) = KC(2). B. KC(1) = (KC(2))2. C. D.
Câu 18: Cho các cân bằng hoá học: (1) CO (g) + H2O (g) CO2 (g) + H2 (g) (2) 2SO2(g) + O2(g) 2SO3(g) (3) H2(g) + I2(g) 2HI(g) (4) 2NO2(g) N2O4(g)
Khi thay đổi áp suất những cân bằng hóa học bị chuyển dịch là A. (1), (2). B. (2), (3). C. (3), (4). D. (2), (4).
Câu 19: Cho cân bằng (trong bình kín) sau: CO (g) + H2O (g) CO2 (g) + H2 (g); < 0.
Trong các yếu tố: (1) tăng nhiệt độ; (2) thêm một lượng hơi nước; (3) thêm một
lượng H2; (4) tăng áp suất chung của hệ; (5) dùng chất xúc tác.
Có bao nhiêu yếu tố làm thay đổi cân bằng của hệ? A. 2. B. 3. C. 4. D. 5.
Câu 20: Phương trình điện li nào dưới đây viết không đúng? A. B. CH3COOH CH3COO− + H+ C. KOH K+ + OH−
Đề thi giữa kì 1 Hóa Học 11 Chân trời sáng tạo (đề 2)
1.1 K
538 lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Tailieugiaovien.com.vn giới thiệu bộ 3 đề giữa kì 1 gồm đầy đủ ma trận và lời giải chi tiết môn Hóa học 11 Chân trời sáng tạo mới nhất năm 2023 - 2024 nhằm giúp Giáo viên có thêm tài liệu tham khảo ra đề thi Hóa học lớp 11.
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(1076 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN Hóa Học
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Lớp 11
Xem thêmTài liệu bộ mới nhất

Đây là bản xem thử, vui lòng mua tài liệu để xem chi ết (có lời giải)
Sở GD - ĐT …
TRƯỜNG THPT …
Mã đề thi: 002
ĐỀ KIỂM TRA GIỮA HỌC KÌ I
Năm học: ….
Môn: Hóa học 11
Bộ: Chân trời sáng tạo
Thời gian làm bài: 60 phút;
(28 câu trắc nghiệm – 3 câu tự luận)
(Học sinh không được sử dụng tài liệu)
Họ, tên học sinh:.....................................................................
Lớp: .............................
Đề bài:
Phần I: Trắc nghiệm (7 điểm)
* Mức độ nhận biết
Câu 1: Tại nhiệt độ không đổi, ở trạng thái cân bằng thì
A. nồng độ của các chất trong hỗn hợp phản ứng không thay đổi.
B. nồng độ của các chất trong hỗn hợp phản ứng vẫn liên tục thay đổi.
C. phản ứng hoá học không xảy ra.
D. tốc độ phản ứng hoá học xảy ra chậm dần.
Câu 2: Yếu tố nào sau đây luôn luôn không làm dịch chuyển cân bằng của hệ
phản ứng?
A. Nhiệt độ B. Áp suất C. Nồng độ D. Chất xúc
tác
Câu 3: Sự điện li là
A. quá trình phân huỷ các chất thành chất mới khi hoà tan vào nước.
B. quá trình kết hợp giữa các ion thành phân tử trong dung dịch.
C. quá trình phản ứng giữa các ion tạo ra chất kết tủa.
D. quá trình phân li thành ion của các chất tan khi tan vào nước.
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi ết (có lời giải)
Câu 4: Trường hợp nào sau đây không dẫn điện được?
A. Dung dịch NaCl.
B. NaOH nóng chảy.
C. Dung dịch HCl.
D. NaCl rắn khan.
Câu 5: Chất nào sau đây không phải là chất điện li?
A. C
2
H
4
. B. KCl.
C. HCl. D. KOH.
Câu 6: Giá trị pH của một dung dịch được tính theo biểu thức nào sau đây?
A. pH = −log[H
+
]. B. pH = log[H
+
].
C. pH = −log[OH
−
]. D. pH = log[OH
−
]
Câu 7: “Đất phèn” là một khái niệm dân gian để chỉ loại đất chứa nhiều ion
sulfate, có pH < 7. Môi trường của đất phèn là
A. môi trường base.
B. môi trường trung tính.
C. môi trường acid.
D. môi trường trung hoà.
Câu 8: Theo thuyết của Bronsted – Lowry thì acid là chất
A. cho proton.
B. tan trong nước phân li ra H
+
.
C. nhận proton.
D. tan trong nước phân li ra OH
−
.
Câu 9: Trong tự nhiên, nguyên tố nitrogen (N) tồn tại ở dạng
A. đơn chất và hợp chất.
B. đơn chất.
C. hợp chất hữu cơ.
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi ết (có lời giải)
D. hợp chất vô cơ.
Câu 10: Số oxi hoá của nitrogen trong hợp chất NH
4
Cl là
A. – 3. B. +3. C. – 4. D. +4.
Câu 11: Dạng hình học của phân tử ammonia là
A. hình tam giác đều.
B. hình tứ diện đều.
C. đường thẳng.
D. hình chóp tam giác.
Câu 12: Cho vài giọt quỳ tím vào dung dịch NH
3
thì dung dịch chuyển thành
A. màu hồng. B. màu vàng.
C. màu đỏ. D. màu xanh.
Câu 13: Để tạo độ xốp cho một số loại bánh, có thể dùng muối nào sau đây làm
bột nở?
A. (NH
4
)
2
SO
4
. B. NH
4
HCO
3
. C. CaCO
3
. D. NH
4
NO
2
.
Câu 14: Muối nào sau đây tan tốt trong nước?
A. BaCO
3
. B. CaSO
4
. C. NH
4
Cl. D. AgCl.
Câu 15: Vai trò của NH
3
trong phản ứng oxi hoá – khử là
A. tính khử. B. tính oxi hóa.
C. tính base. D. tính acid.
Câu 16: Nhóm các kim loại đều phản ứng được với HNO
3
là
A. Al, Cu, Au.
B. Mg, Zn, Cu.
C. Mg, Au, Fe.
D. Ag, Pt, Au.
* Mức độ thông hiểu
Câu 17: Xét các cân bằng sau:
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
Đây là bản xem thử, vui lòng mua tài liệu để xem chi ết (có lời giải)
(1) H
2
(g) + I
2
(g) HI(g) K
C(1)
(2) H
2
(g) + I
2
(g) 2HI(g) K
C(2)
Mối quan hệ giữa K
C(1)
và K
C(2)
là
A. K
C(1)
= K
C(2)
. B. K
C(1)
= (K
C(2)
)
2
.
C. D.
Câu 18: Cho các cân bằng hoá học:
(1) CO
(g) + H
2
O (g)
CO
2
(g)
+ H
2
(g)
(2) 2SO
2
(g) + O
2
(g) 2SO
3
(g)
(3) H
2
(g) + I
2
(g) 2HI(g)
(4) 2NO
2
(g) N
2
O
4
(g)
Khi thay đổi áp suất những cân bằng hóa học bị chuyển dịch là
A. (1), (2). B. (2), (3). C. (3), (4). D. (2), (4).
Câu 19: Cho cân bằng (trong bình kín) sau:
CO
(g) + H
2
O (g)
CO
2
(g)
+ H
2
(g); < 0.
Trong các yếu tố: (1) tăng nhiệt độ; (2) thêm một lượng hơi nước; (3) thêm một
lượng H
2
; (4) tăng áp suất chung của hệ; (5) dùng chất xúc tác.
Có bao nhiêu yếu tố làm thay đổi cân bằng của hệ?
A. 2. B. 3. C. 4. D. 5.
Câu 20: Phương trình điện li nào dưới đây viết không đúng?
A.
B. CH
3
COOH CH
3
COO
−
+ H
+
C. KOH K
+
+ OH
−
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi ết (có lời giải)
D.
Câu 21: Trong dung dịch acetic acid (bỏ qua sự phân li của H
2
O) có những phần tử
nào?
A. H
+
, CH
3
COO
-
.
B. H
+
, CH
3
COO
-
, H
2
O.
C. CH
3
COOH, H
+
, CH
3
COO
-
, H
2
O.
D. CH
3
COOH, CH
3
COO
-
, H
+
.
Câu 22: Cho phương trình: NH
3
+ H
2
O + OH
−
Trong phản ứng thuận, theo thuyết Bronsted – Lowry chất nào là acid?
A. NH
3
. B. H
2
O. C. . D. OH
−
.
Câu 23: Phương trình hóa học nào sau đây sai?
A.
B.
C.
D.
Câu 24: Ở nhiệt độ cao, khí nitrogen phản ứng với khí hydrogen và khí oxygen
theo hai phương trình hoá học sau:
N
2
+ O
2
2NO (1)
N
2
+ 3H
2
2NH
3
(2)
Trong các phản ứng (1) và (2), vai trò của N
2
lần lượt là
A. chất oxi hoá; chất khử.
B. chất khử; chất khử.
C. chất oxi hoá; chất oxi hoá.
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85























