SỞ GIÁO DỤC VÀ ĐÀO TẠO KỲ THI CHỌN HỌC SINH GIỎI CÁC MÔN VĂN HÓA CẤP TỈNH …..
NĂM HỌC: 2023 - 2024
MÔN THI: HÓA HỌC – KHỐI 11
ĐỀ THI CHÍNH THỨC NGÀY THI:
(Đề thi có 3 phần, 12 trang)
Thời gian làm 90 phút (không kể thời gian phát đề)
Họ và tên: ................................................................
Số báo danh:....... Mã đề 101
Cho biết nguyên tử khối: H=1; C=12; N=14; O=16; Cl=35,5; Na=23; K=39; Mg=24; Ba=137;
P=31; S=32; Ca=40; Fe=56; Cu=64; Br=80, Mn=55 ; F=19; I=127; Al=27
Thể tích khí ở đkc (25oC, 1 bar) được tính theo công thức: V = n 24,79
PHẦN 1. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 50. Mỗi
câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Cho phản ứng: HC≡CH + H HgSO ⎯⎯⎯⎯⎯ → 2O 4 o H SO , 80 C 2 4
Sản phẩm của phản ứng trên là A. CH2=CH−OH. B. CH2=CH2. C. CH − − 3 CH=O. D. CH3 O−CH3.
Câu 2. Trong phòng thí nghiệm, người ta có thể điều chế khí NH3 bằng cách
A. cho muối ammonium chloride đặc tác dụng với kiềm đặc và đun nóng.
B. cho muối ammonium chloride loãng tác dụng với acid HCl loãng và đun nóng.
C. cho N2 tác dụng với H2 (450℃, bột iron).
D. nhiệt phân muối (NH4)2CO3.
Câu 3. Trộn 100 ml dung dịch (gồm Ba(OH)2 0,1 M và NaOH 0,1 M) với 400 ml dung dịch (gồm
H2SO4 0,0375 M và HCl 0,0125 M), thu được dung dịch X. Giá trị pH của dung dịch X là A. 7. B. 2. C. 1. D. 6.
Câu 4. Cho dãy các chất: CH4, C2H2, C2H4, C2H5OH, CH2=CH−CH2OH, C6H5OH (phenol), C6H6
(benzene). Số chất trong dãy phản ứng được với nước bromine là A. 7. B. 6. C. 4. D. 5.
Câu 5. Phản ứng hóa học của các hợp chất hữu cơ có đặc điểm là
A. thường xảy ra rất chậm, nhưng hoàn toàn, không theo một hướng xác định.
B. thường xảy ra rất nhanh, không hoàn toàn, không theo một hướng nhất định.
C. thường xảy ra chậm, không hoàn toàn, không theo một hướng nhất định.
D. thường xảy ra rất nhanh và cho một sản phẩm duy nhất.
Câu 6. Phản ứng nào sau đây có phương trình ion rút gọn là H+ + OH− → H2O?
A. Ba(OH)2 + H2SO4 → BaSO4 + 2H2O.
B. Cu(OH)2 + 2HCl → CuCl2 + 2H2O.
C. Ba(OH)2 + 2HCl → BaCl2 + 2H2O.
D. NaHCO3 + NaOH → Na2CO3 + H2O. 1
Câu 7. Trong phòng thí nghiệm, khi X được điều chế và thu vào bình tam giác theo hình vẽ bên. Khí
X được tạo ra từ phản ứng hóa học nào sau đây? o A. NH t ⎯⎯→ 4Cl + NaOH NH3(g) + NaCl + H2O o B. 2Fe + 6H t ⎯⎯→ 2SO4(đặc)
Fe2(SO4)3 + 3SO2(g) + 6H2O
C. CaCO3 + 2HCl → CaCl2 + CO2(g) + H2O
D. 3Cu + 8HNO3(loãng) → 3Cu(NO3)2 + 2NO(g) + 4H2O
Câu 8. Một nhóm học sinh thực hiện thí nghiệm cho kim loại Cu tác dụng với dung dịch HNO3 đặc.
Hiện tượng quan sát nào sau đây là đúng?
A. Khí màu nâu đỏ thoát ra, dung dịch không màu.
B. Khí không màu thoát ra, dung dịch chuyển sang màu xanh.
C. Khí màu nâu đỏ thoát ra, dung dịch chuyển sang màu xanh.
D. Khí không màu thoát ra, dung dịch không màu.
Câu 9. Sản phẩm của phản ứng nhiệt phân hoàn toàn AgNO3 là A. Ag, NO2, O2.
B. Ag2O, NO2, O2. C. Ag, NO, O2.
D. Ag2O, NO, O2.
Câu 10. Chất nào sau đây thuộc loại chất điện li mạnh? A. C2H5OH. B. H2O. C. NaCl. D. CH3COOH.
Câu 11. Một mẫu khí gas X chứa hỗn hợp propane và butane. Đốt cháy hoàn toàn 12 gam mẫu khí
gas X tỏa ra nhiệt lượng 594 kJ. Biết rằng, khi đốt cháy hoàn toàn, 1 mol propane tỏa ra lượng nhiệt
là 2220 kJ và 1 mol butane tỏa ra lượng nhiệt là 2850 kJ. Tỉ lệ số mol của propane và butane trong X là A. 1 : 2. B. 1 : 1. C. 2 : 3. D. 3 : 2.
Câu 12. Hỗn hợp X gồm H2 và C2H4 có tỉ khối so với H2 là 7,5. Dẫn X qua Ni nung nóng, thu được
hỗn hợp Y có tỉ khối so với H2 là 12,5. Hiệu suất của phản ứng hydrogen hoá là A. 80%. B. 60%. C. 50%. D. 70%.
Câu 13. Cho các chất sau đây: (I) CH − − − 3 CH(OH)−CH3; (II) CH3 CH2 OH; (III) CH − − − − − − 3 CH2 CH2 OH; (IV) CH3 CH2 CH2 O−CH3; (V) CH − − − − − 3 CH2 CH2 CH2 OH; (VI) CH3 O.
Các chất đồng đẳng của nhau là
A. (I), (II), (III), (IV).
B. (I), III và (IV).
C. (II), (III), (V) và (VI).
D. (I), (II) và (VI).
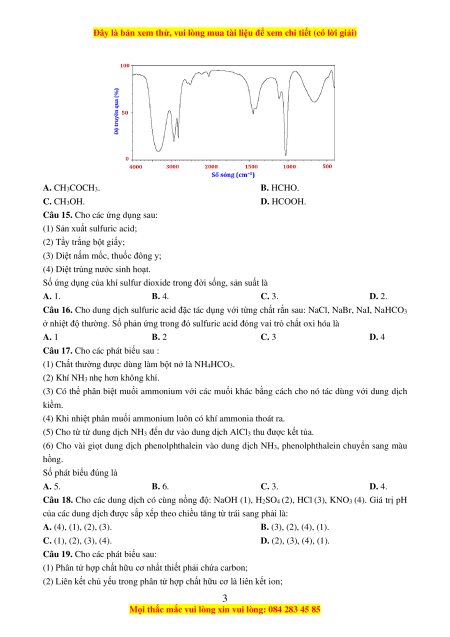
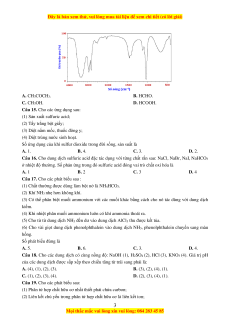
Câu 14. Cho phổ hồng ngoại (IR) của chất hữu cơ như hình dưới tương ứng chất nào sau đây: 2
A. CH3COCH3. B. HCHO. C. CH3OH. D. HCOOH.
Câu 15. Cho các ứng dụng sau:
(1) Sản xuất sulfuric acid;
(2) Tẩy trắng bột giấy;
(3) Diệt nấm mốc, thuốc đông y;
(4) Diệt trùng nước sinh hoạt.
Số ứng dụng của khí sulfur dioxide trong đời sống, sản suất là A. 1. B. 4. C. 3. D. 2.
Câu 16. Cho dung dịch sulfuric acid đặc tác dụng với từng chất rắn sau: NaCl, NaBr, NaI, NaHCO3
ở nhiệt độ thường. Số phản ứng trong đó sulfuric acid đóng vai trò chất oxi hóa là A. 1 B. 2 C. 3 D. 4
Câu 17. Cho các phát biểu sau :
(1) Chất thường được dùng làm bột nở là NH4HCO3.
(2) Khí NH3 nhẹ hơn không khí.
(3) Có thể phân biệt muối ammonium với các muối khác bằng cách cho nó tác dùng với dung dịch kiềm.
(4) Khi nhiệt phân muối ammonium luôn có khí ammonia thoát ra.
(5) Cho từ từ dung dịch NH3 đến dư vào dung dịch AlCl3 thu được kết tủa.
(6) Cho vài giọt dung dịch phenolphthalein vào dung dịch NH3, phenolphthalein chuyển sang màu hồng. Số phát biểu đúng là A. 5. B. 6. C. 3. D. 4.
Câu 18. Cho các dung dịch có cùng nồng độ: NaOH (1), H2SO4 (2), HCl (3), KNO3 (4). Giá trị pH
của các dung dịch được sắp xếp theo chiều tăng từ trái sang phải là:
A. (4), (1), (2), (3).
B. (3), (2), (4), (1).
C. (1), (2), (3), (4).
D. (2), (3), (4), (1).
Câu 19. Cho các phát biểu sau:
(1) Phân tử hợp chất hữu cơ nhất thiết phải chứa carbon;
(2) Liên kết chủ yếu trong phân tử hợp chất hữu cơ là liên kết ion; 3
(3) Hợp chất hữu cơ thường khó nóng chảy và khó bay hơi;
(4) Hợp chất hữu cơ thường không tan hoặc ít tan trong nước;
(5) Phản ứng của các hợp chất hữu cơ thường chậm, không hoàn toàn, không theo một hướng nhất định;
(6) Các hợp chất hữu cơ thường khó cháy và khó bị phân huỷ dưới tác dụng của nhiệt.
Số phát biểu đúng là A. 4. B. 3. C. 6. D. 5.
Câu 20. Trong một bình kín có cân bằng hóa học sau: 2NO2(g) ⇌ N2O4(g). Tỉ khối hơi của hỗn hợp
khí trong bình so với H2 ở nhiệt độ T1 bằng 27,6 và ở nhiệt độ T2 bằng 34,5. Biết T1 > T2. Phát biểu
nào sau đây về cân bằng trên là đúng?
A. Khi giảm nhiệt độ, áp suất chung của hệ cân bằng tăng.
B. Phản ứng thuận là phản ứng tỏa nhiệt.
C. Khi tăng nhiệt độ, áp suất chung của hệ cân bằng giảm.
D. Phản ứng nghịch là phản ứng tỏa nhiệt.
Câu 21. Hãy sắp xếp các cách tiến thành tách và tinh chế hợp chất hữu cơ theo đúng thứ tự của
phương pháp chiết lỏng – rắn?
(a) Làm bay hơi dung môi của dịch chiết để thu được chất cần tách.
(b) Lọc bỏ phần chất rắn không tan, thu được dịch chiết chứa chất cần tách.
(c) Hoà tan chất hữu cơ bằng cách ngâm hoặc đun hỗn hợp chất rắn với dung môi thích hợp.
A. (b), (c), (a).
B. (a), (c), (b).
C. (c), (a), (b).
D. (c), (b), (a).
Câu 22. Tiến hành thí nghiệm trộn từng cặp dung dịch sau: (a) NH3 và AlCl3; (b) (NH4)2SO4 và
Ba(OH)2; (c) NH4Cl và AgNO3; (d) NH3 và HCl.
Sau khi phản ứng kết thúc, số thí nghiệm thu được kết tủa là A. 3. B. 2. C. 4. D. 1.
Câu 23. Để điều chế 5 lít dung dịch HNO3 21% (D = 1,2 g/mL) bằng phương pháp oxi hóa NH3 với
hiệu suất toàn quá trình là 80%, thể tích khí NH3 (đkc) tối thiểu cần dùng là A. 743,70 lít. B. 495,80 lít. C. 371,85 lít. D. 619,75 lít.
Câu 24. Có bao nhiêu đặc điểm sau đây về muối sulfate là đúng?
(a) Nhiều muối sulfate tan tốt trong nước nhưng một số muối như CaSO4, BaSO4 rất ít tan trong nước.
(b) Magnesium sulfate được dùng làm chất hút mồ hôi tay cho các vận động viên, …
(c) Calcium sulfate là thành phần chính của các loại thạch cao.
(d) Barium sulfate là chất rắn màu trắng, hầu như không tan trong nước, Chất này được dùng làm
thuốc cản quang trong kỹ thuật chụp X - quang. A. 2. B. 4. C. 3. D. 1
Câu 25. Trong bình kín có hệ cân bằng hóa học sau: CO
2(g) + H2(g) ⇌ CO(g) + H2O(g); o H > 0. r 298 4
Bộ 20 đề thi HSG Hóa 11 năm 2023-2024 có đáp án
6.7 K
3.3 K lượt tải
300.000 ₫
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Bộ tài liệu bao gồm: 20 tài liệu lẻ (mua theo bộ tiết kiệm đến 50%)
- Tailieugiaovien.com.vn giới thiệu Bộ 20 đề thi Học sinh giỏi Hóa 11 năm 2023 - 2024 chương trình sách mới và tặng kèm 12 đề HSG Hóa 11 năm 2022-2023 nhằm giúp Giáo viên có thêm tài liệu tham khảo Hóa học 11.
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(6669 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)