PHÒNG GIÁO DỤC VÀ ĐÀO TẠO
ĐỀ KIỂM TRA GIỮA HỌC KÌ I TRƯỜNG THCS ……
Môn: Khoa học tự nhiên 8 Đề số 2
(Theo chương trình dạy nối tiếp)
Thời gian: 60 phút (không kể thời gian giao đề)
(Đề gồm 16 câu trắc nghiệm và 4 câu tự luận) Đề bài
Phần I. Trắc nghiệm (4 điểm)
Hãy khoanh tròn chữ cái đứng trước câu trả lời mà em cho là đúng nhất. Mỗi câu
trả lời đúng được 0,25 điểm.
Câu 1: Thiết bị nào sau đây là thiết bị sử dụng điện? A. Pin. B. Cầu chì. C. Diode phát quang. D. Công tắc.
Câu 2: Những việc nào sau đây không được làm khi sử dụng hóa chất?
A. Sau khi lấy hóa chất xong cần phải đậy kín các lọ đựng hóa chất.
B. Cần thông báo ngay cho giáo viên nếu gặp sự cố cháy, nổ, đổ hóa chất, vỡ dụng cụ thí nghiệm, …
C. Sử dụng tay tiếp xúc trực tiếp với hóa chất.
D. Đọc kĩ nhãn mác, không sử dụng hóa chất nếu không có nhãn mác, hoặc nhãn mác bị mờ.
Câu 3: Nến được làm bằng parafin, khi đốt nến, xảy ra các quá trình sau: 1. Parafin nóng chảy
2. Parafin lỏng chuyển thành hơi
3. Hơi parafin cháy biến đổi thành khí CO2 và hơi nước
Quá trình nào có sự biến đổi hoá học? A. 1. B. 2. C. 3. D. Cả 1, 2, 3.
Câu 4: Iron để trong không khí một thời gian sẽ bị gỉ do tác dụng với khí oxygen
trong không khí tạo ra oxide (gỉ sắt). Trong phản ứng trên, chất tham gia phản ứng là?
A. Không khí.
B. Iron và không khí. C. Oxide.
D. Iron và khí oxygen.
Câu 5: Cho các quá trình biến đổi hóa học sau:
(1) Đốt cháy củi, than đá, than cốc.
(2) Phân hủy đá vôi ở nhiệt độ cao (900-1000oC) thành vôi sống.
Phát biểu nào sau đây đúng?
A. (1) là phản ứng tỏa nhiệt; (2) là phản ứng thu nhiệt.
B. (1) là phản ứng thu nhiệt; (2) là phản ứng tỏa nhiệt.
C. Cả (1) và (2) đều là phản ứng tỏa nhiệt.
D. Cả (1) và (2) đều là phản ứng thu nhiệt.
Câu 6: Dung dịch chưa bão hòa là dung dịch _______
A. không thể hòa tan thêm chất tan.
B. có thể hòa tan thêm chất tan.
C. không thể hòa tan thêm nước.
D. có thể hòa tan thêm dung dịch.
Câu 7: Khi tăng nhiệt độ thì độ tan của chất rắn trong nước nhìn chung _______ A. biến đổi ít. B. tăng. C. giảm. D. không đổi.
Câu 8: Cho sơ đồ phản ứng: CO2 + Ca(OH)2 CaCO3 + ?
Cần điền chất nào sau đây để hoàn thành phương trình hoá học của phản ứng trên? A. CaO. B. H2O. C. CO. D. CH4.
Câu 9: Than cháy trong bình khí oxygen nhanh hơn cháy trong không khí. Yếu tố đã
làm tăng tốc độ của phản ứng này là A. tăng nhiệt độ. B. tăng nồng độ.
C. tăng diện tích bề mặt tiếp xúc.
D. dùng chất xúc tác.
Câu 10: Tốc độ phản ứng là đại lương đặc trưng cho
A. thời gian phản ứng.
B. khối lượng chất đã tham gia phản ứng.
C. sự nhanh chậm của phản ứng hóa học.
D. thể tích chất đã tham gia phản ứng.
Câu 11: Chất nào sau đây không phải là acid? A. NaCl. B. HNO3. C. HCl. D. H2SO4.
Câu 12: Trong giấm ăn có chứa acid X với nồng độ 2 – 5%. Chất X là A. CH3CHO. B. CH3COOH. C. HCl. D. H2SO4.
Câu 13: Calcium hydroxide được sử dụng rộng rãi trong nhiều ngành công nghiệp.
Công thức của calcium hydroxide? A. CaO. B. Ca(OH)2. C. CaSO4. D. CaCO3.
Câu 14: Trong số quá trình và sự việc dưới đây, đâu là biến đổi hiện tượng vật lí:
1. Hoà tan muối ăn vào nước ta được dung dịch muối ăn
2. Cồn để trong lọ không kín bị bay hơi
3. Nước bị đóng băng hai cực Trái đất
4. Cho vôi sống CaO hoà tan vào nước được vôi tôi A. 1, 2, 3. B. 1, 2, 4. C. 2, 3, 4. D. 1, 3, 4.
Câu 15: Khí nào nặng hơn không khí trong các khí sau A. N2. B. SO2. C. NH3. D. H2.
Câu 16: Trong số các base sau đây, base nào là base tan trong nước? A. Fe(OH)2 B. KOH C. Cu(OH)2 D. Fe(OH)3
Phần II. Tự luận (6 điểm)
Bài 1: (1 điểm) Nêu cách lấy hoá chất an toàn trong phòng thí nghiệm? Bài 2: (2 điểm)
a) Hoà tan hoàn toàn 32 gam copper(II) sulfate (CuSO4) trong nước thu được 200 ml
dung dịch. Tính nồng độ mol của dung dịch này.
b) Cần bao nhiêu g BaCl2 và bao nhiêu gam nước để pha 200 g dung dịch BaCl2 10%.
Bài 3: (1 điểm) Cho 0,50 mol khí hydrogen tác dụng với 0,45 mol hơi iodine thu
được 0,60 mol khí hydrogen iodide. Tính hiệu suất phản ứng.
Bài 4: (2 điểm) Nhỏ từ từ dung dịch HCl loãng vào ống nghiệm (1) chứa lá nhôm
(aluminium) và ống nghiệm (2) chứa lá đồng (copper). Hãy mô tả hiện tượng xảy ra
trong các ống nghiệm trên và viết phương trình hoá học xảy ra (nếu có).
Hướng dẫn giải đề số 2
Phần I. Trắc nghiệm 1. C 2. C 3. C 4. D 5. A 6. B 7. B 8. B 9. B 10. C 11. A 12. B 13. B 14. A 15. B 16. B Phần II. Tự luận Bài 1:
Cách lấy hoá chất an toàn: Không dùng tay trực tiếp lấy hoá chất. Khi lấy hoá chất
rắn ở dạng hạt nhỏ hay bột ra khỏi lọ phải dùng thìa kim loại hoặc thìa thuỷ tinh để
xúc. Lấy hoá chất ở dạng hạt to, dây, thanh có thể dùng panh để gắp. Không được đặt
lại thìa, panh vào lọ đựng hoá chất sau khi đã sử dụng. Lấy hoá chất lỏng từ chai
miệng nhỏ thường phải rót qua phễu hoặc qua cốc, ống đong có mỏ, lấy lượng nhỏ
dung dịch thường dùng ống hút nhỏ giọt; rót hoá chất lỏng từ lọ cần hướng nhãn hoá
chất lên phía trên tránh để các giọt hoá chất dính vào làm hỏng nhãn. Bài 2:
a) Số mol CuSO4 có trong dung dịch là: Đổi 200ml = 0,2 (lít)
Nồng độ mol của dung dịch CuSO4 là: (mol /l) hoặc viết là 1M.
b) Khối lượng BaCl2 trong 200 gam dung dịch:
Đề thi giữa kì 1 KHTN 8 Kết nối tri thức (nối tiếp) - Đề 2
1.4 K
716 lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Đề thi được cập nhật liên tục trong gói này từ nay đến hết tháng 3/2024. Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Tailieugiaovien.com.vn giới thiệu bộ 4 đề thi giữa kì 1 môn Khoa học tự nhiên 8 Kết nối tri thức bao gồm: bộ nối tiếp và bộ song song mới nhất năm 2023 nhằm giúp Giáo viên có thêm tài liệu tham khảo ra đề thi Khoa học tự nhiên lớp 8.
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(1432 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN KHTN
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Lớp 8
Xem thêmTài liệu bộ mới nhất

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
PHÒNG GIÁO DỤC VÀ ĐÀO TẠO
TRƯỜNG THCS ……
Đề số 2
ĐỀ KIỂM TRA GIỮA HỌC KÌ I
Môn: Khoa học tự nhiên 8
(Theo chương trình dạy nối tiếp)
Thời gian: 60 phút (không kể thời gian giao đề)
(Đề gồm 16 câu trắc nghiệm và 4 câu tự luận)
Đề bài
Phần I. Trắc nghiệm (4 điểm)
Hãy khoanh tròn chữ cái đứng trước câu trả lời mà em cho là đúng nhất. Mỗi câu
trả lời đúng được 0,25 điểm.
Câu 1: Thiết bị nào sau đây là thiết bị sử dụng điện?
A. Pin. B. Cầu chì.
C. Diode phát quang. D. Công tắc.
Câu 2: Những việc nào sau đây không được làm khi sử dụng hóa chất?
A. Sau khi lấy hóa chất xong cần phải đậy kín các lọ đựng hóa chất.
B. Cần thông báo ngay cho giáo viên nếu gặp sự cố cháy, nổ, đổ hóa chất, vỡ dụng cụ
thí nghiệm, …
C. Sử dụng tay tiếp xúc trực tiếp với hóa chất.
D. Đọc kĩ nhãn mác, không sử dụng hóa chất nếu không có nhãn mác, hoặc nhãn mác
bị mờ.
Câu 3: Nến được làm bằng parafin, khi đốt nến, xảy ra các quá trình sau:
1. Parafin nóng chảy
2. Parafin lỏng chuyển thành hơi
3. Hơi parafin cháy biến đổi thành khí CO
2
và hơi nước
Quá trình nào có sự biến đổi hoá học?
A. 1. B. 2. C. 3. D. Cả 1, 2, 3.
Câu 4: Iron để trong không khí một thời gian sẽ bị gỉ do tác dụng với khí oxygen
trong không khí tạo ra oxide (gỉ sắt). Trong phản ứng trên, chất tham gia phản ứng
là?
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
A. Không khí. B. Iron và không khí.
C. Oxide. D. Iron và khí oxygen.
Câu 5: Cho các quá trình biến đổi hóa học sau:
(1) Đốt cháy củi, than đá, than cốc.
(2) Phân hủy đá vôi ở nhiệt độ cao (900-1000
o
C) thành vôi sống.
Phát biểu nào sau đây đúng?
A. (1) là phản ứng tỏa nhiệt; (2) là phản ứng thu nhiệt.
B. (1) là phản ứng thu nhiệt; (2) là phản ứng tỏa nhiệt.
C. Cả (1) và (2) đều là phản ứng tỏa nhiệt.
D. Cả (1) và (2) đều là phản ứng thu nhiệt.
Câu 6: Dung dịch chưa bão hòa là dung dịch _______
A. không thể hòa tan thêm chất tan.
B. có thể hòa tan thêm chất tan.
C. không thể hòa tan thêm nước.
D. có thể hòa tan thêm dung dịch.
Câu 7: Khi tăng nhiệt độ thì độ tan của chất rắn trong nước nhìn chung _______
A. biến đổi ít. B. tăng. C. giảm. D. không đổi.
Câu 8: Cho sơ đồ phản ứng:
CO
2
+ Ca(OH)
2
CaCO
3
+ ?
Cần điền chất nào sau đây để hoàn thành phương trình hoá học của phản ứng trên?
A. CaO. B. H
2
O. C. CO. D. CH
4
.
Câu 9: Than cháy trong bình khí oxygen nhanh hơn cháy trong không khí. Yếu tố đã
làm tăng tốc độ của phản ứng này là
A. tăng nhiệt độ.
B. tăng nồng độ.
C. tăng diện tích bề mặt tiếp xúc.
D. dùng chất xúc tác.
Câu 10: Tốc độ phản ứng là đại lương đặc trưng cho
A. thời gian phản ứng.
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
B. khối lượng chất đã tham gia phản ứng.
C. sự nhanh chậm của phản ứng hóa học.
D. thể tích chất đã tham gia phản ứng.
Câu 11: Chất nào sau đây không phải là acid?
A. NaCl. B. HNO
3
. C. HCl. D. H
2
SO
4
.
Câu 12: Trong giấm ăn có chứa acid X với nồng độ 2 – 5%. Chất X là
A. CH
3
CHO. B. CH
3
COOH.
C. HCl. D. H
2
SO
4
.
Câu 13: Calcium hydroxide được sử dụng rộng rãi trong nhiều ngành công nghiệp.
Công thức của calcium hydroxide?
A. CaO. B. Ca(OH)
2
. C. CaSO
4
. D. CaCO
3
.
Câu 14: Trong số quá trình và sự việc dưới đây, đâu là biến đổi hiện tượng vật lí:
1. Hoà tan muối ăn vào nước ta được dung dịch muối ăn
2. Cồn để trong lọ không kín bị bay hơi
3. Nước bị đóng băng hai cực Trái đất
4. Cho vôi sống CaO hoà tan vào nước được vôi tôi
A. 1, 2, 3. B. 1, 2, 4. C. 2, 3, 4. D. 1, 3, 4.
Câu 15: Khí nào nặng hơn không khí trong các khí sau
A. N
2
. B. SO
2
. C. NH
3
. D. H
2
.
Câu 16: Trong số các base sau đây, base nào là base tan trong nước?
A. Fe(OH)
2
B. KOH
C. Cu(OH)
2
D. Fe(OH)
3
Phần II. Tự luận (6 điểm)
Bài 1: (1 điểm) Nêu cách lấy hoá chất an toàn trong phòng thí nghiệm?
Bài 2: (2 điểm)
a) Hoà tan hoàn toàn 32 gam copper(II) sulfate (CuSO
4
) trong nước thu được 200 ml
dung dịch. Tính nồng độ mol của dung dịch này.
b) Cần bao nhiêu g BaCl
2
và bao nhiêu gam nước để pha 200 g dung dịch BaCl
2
10%.
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Bài 3: (1 điểm) Cho 0,50 mol khí hydrogen tác dụng với 0,45 mol hơi iodine thu
được 0,60 mol khí hydrogen iodide. Tính hiệu suất phản ứng.
Bài 4: (2 điểm) Nhỏ từ từ dung dịch HCl loãng vào ống nghiệm (1) chứa lá nhôm
(aluminium) và ống nghiệm (2) chứa lá đồng (copper). Hãy mô tả hiện tượng xảy ra
trong các ống nghiệm trên và viết phương trình hoá học xảy ra (nếu có).
Hướng dẫn giải đề số 2
Phần I. Trắc nghiệm
1. C 2. C 3. C 4. D 5. A 6. B 7. B 8. B
9. B 10. C 11. A 12. B 13. B 14. A 15. B 16. B
Phần II. Tự luận
Bài 1:
Cách lấy hoá chất an toàn: Không dùng tay trực tiếp lấy hoá chất. Khi lấy hoá chất
rắn ở dạng hạt nhỏ hay bột ra khỏi lọ phải dùng thìa kim loại hoặc thìa thuỷ tinh để
xúc. Lấy hoá chất ở dạng hạt to, dây, thanh có thể dùng panh để gắp. Không được đặt
lại thìa, panh vào lọ đựng hoá chất sau khi đã sử dụng. Lấy hoá chất lỏng từ chai
miệng nhỏ thường phải rót qua phễu hoặc qua cốc, ống đong có mỏ, lấy lượng nhỏ
dung dịch thường dùng ống hút nhỏ giọt; rót hoá chất lỏng từ lọ cần hướng nhãn hoá
chất lên phía trên tránh để các giọt hoá chất dính vào làm hỏng nhãn.
Bài 2:
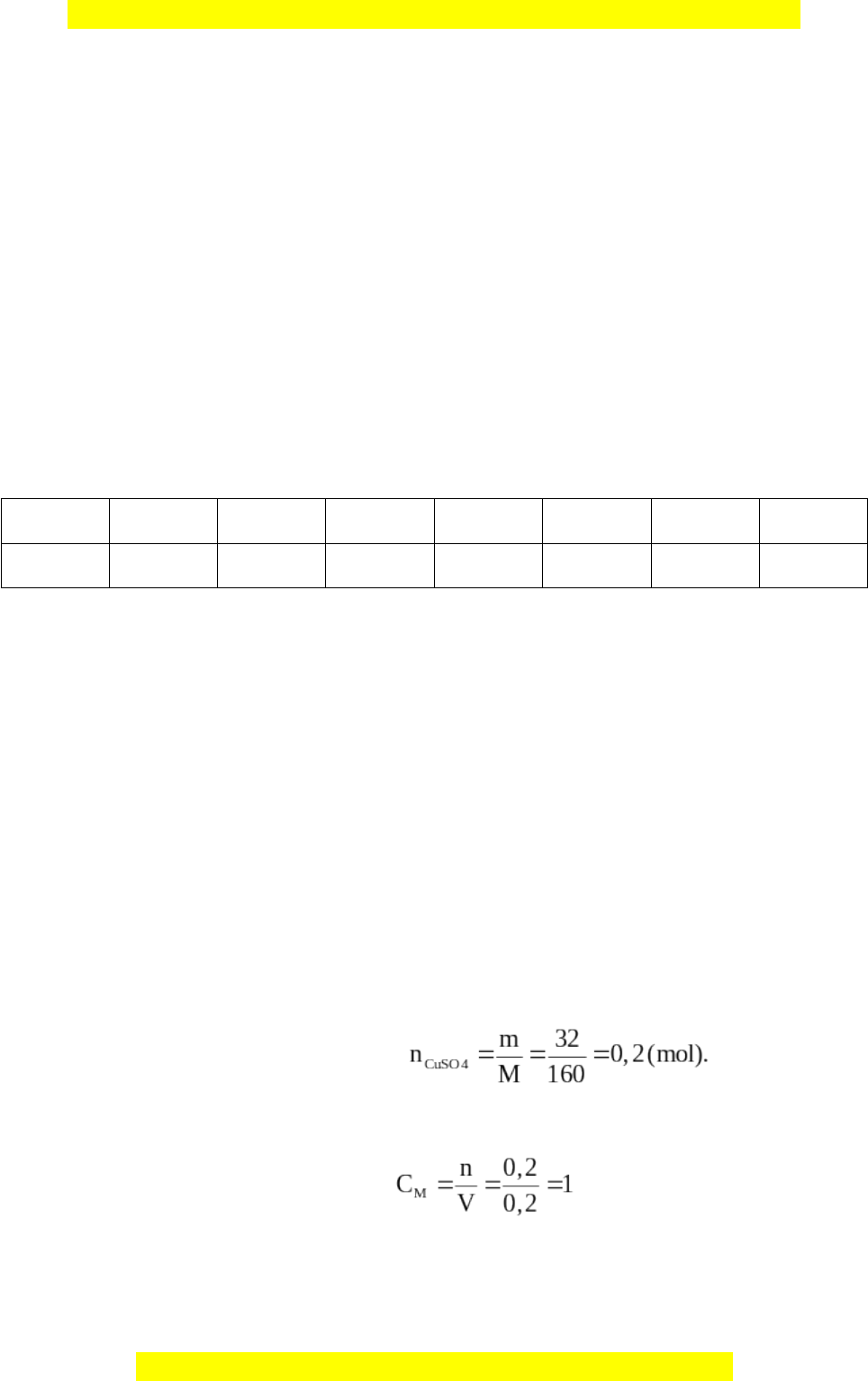
a) Số mol CuSO
4
có trong dung dịch là:
Đổi 200ml = 0,2 (lít)
Nồng độ mol của dung dịch CuSO
4
là: (mol /l) hoặc viết là 1M.
b) Khối lượng BaCl
2
trong 200 gam dung dịch:
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Khối lượng nước cần để pha chế là:
Bài 3:
Phương trình hoá học: H
2
+ I
2
→ 2HI
Tỉ lệ các chất: 1 : 1 : 2
Giả sử hiệu suất đạt 100% thì I
2
hết, H
2
dư, vậy lượng HI thu được theo lí thuyết tính
theo I
2
. Theo tỉ lệ mol của phản ứng, ta có:
n
HI lý thuyết
=
Hiệu suất của phản ứng là:
Bài 4:
Trong ống nghiệm (1) chứa lá nhôm có bọt khí thoát ra, lá nhôm bị tan dần do có
phản ứng:
2Al + 6HCl → 2AlCl
3
+ 3H
2
Trong ống nghiệm (2) chứa lá đồng không có hiện tượng gì xảy ra do đồng không
phản ứng với dung dịch HCl.
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85