(Đề thi có 0 trang)
ĐỀ THI THỬ THPTQG NĂM 2019
CHUẨN CẤU TRÚC CỦA BỘ GIÁO DỤC – ĐỀ 0 Môn thi: HÓA HỌC
Thời gian làm bài: 50 phút, không kể thời gian phát đề
Họ, tên thí sinh:.......................................................................
Số báo danh:............................................................................
Cho biết nguyên tử khối của các nguyên tố:
H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; S = 32; Cl = 35,5; K = 39; Ca = 40; Cr = 52;
Fe = 56; Cu = 64; Zn = 65; Ag = 108; Ba = 137.
Câu 1. Trong điều kiện thích hợp glucozơ lên men tạo thành khí CO2 và A. CH3CHO. B. HCOOH. C. CH3COOH. D. C2H5OH.
Câu 2. Chất X có công thức phân tử C4H6O2. Khi tác dụng với dung dịch NaOH sinh ra chất Y có công
thức phân tử C3H3O2Na. Chất X có tên gọi là A. metyl acrylat. B. metyl metacrylat. C. metyl axetat. D. etyl acrylat.
Câu 3. Hỗn hợp X gồm C2H5NH2 và NH2C2H4NH2, Cho 7,5 gam X tác dụng vừa đủ với dung dịch
thu được 17,3 gam muối. Phần trăm khối lượng của C2H5NH2 trong X là: A. 60. B. 90. C. 48. D. 72.
Câu 4. Ở điều kiện thường, kim loại nào sau đây không phản ứng với nước: A. Rb. B. Na. C. Fe. D. Ca.
Câu 5. Cho 0,6 gam một kim loại hóa trị II phản ứng hết với dung dịch H2SO4 loãng, dư, thu được 0,56
lít H2 (đktc). Kim loại đó là A. Ca. B. Zn. C. Mg. D. Sr.
Câu 6. Cho các phát biểu sau:
(1) Amino axit là các chất rắn màu trắng, kết tinh, tương đối dễ tan trong nước.
(2) Các amin có số cacbon nhỏ hơn hoặc bằng 3, đơn chức, mạch hở là chất khí mùi khai giống
(3) Sợi bông, tơ tằm và tơ olon thuộc loại polime thiên nhiên.
(4) Saccarozơ và mantozơ chỉ có cấu tạo mạch vòng. (5) Trùng ngưng axit
aminoenantoic thu được nilon – 6. Số phát biểu sai là A. 4 B. 3 C. 5 D. 2
Câu 7. Trong bốn polime cho dưới đây, polime nào cùng loại polime với tơ lapsan A. Tơ tằm B. Tơ nilon-6,6 C. Xenlulozơ trinitrat D. Cao su thiên nhiên
Câu 8. Hòa tan 5,4 gam bột Al vào 150 ml dung dịch X chứa Fe(NO3)3 1M và Cu(NO3)2 1M. Kết thúc
phản ứng thu được của m là A. 10,95. B. 13,20. C. 13,80. D. 15,20. Trang 1
Câu 9. Este X có công thức phân tử là C4H6O2 khi thủy phân trong môi trường axit thu được ancol có khả
năng làm mất màu nước brom. Công thức cấu tạo thu gọn của X là: A. CH3COO-CH=CH2 B. HCOO-CH=CH-CH3 C. HCOO-CH2CH=CH2 D. CH2=CH-COOCH3
Câu 10. Hợp chất ion G tạo nên từ các ion đơn nguyên tử M2+ và X2-. Tổng số hạt (nơtron, proton,
electron) trong phân tử G là 84, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 28 hạt.
Số hạt mang điện của ion X2- ít hơn số hạt mang điện của ion M2+ là 20 hạt. Vị trí của M trong bảng tuần hoàn là
A. ô 8, chu kì 2, nhóm VIA.
B. ô 26, chu kì 4, nhóm VIIIB.
C. ô 12, chu kì 3, nhóm IIA.
D. ô 20, chu kì 4, nhóm IIA.
Câu 11. Polime nào sau đây có cấu trúc mạng không gian? A. Cao su buna B. Aminozơ C. Glicogen D. Cao su lưu hóa
Câu 12. N – metyletanamin có công thức là: A. C2H5NHCH3 B. CH3NHCH3 C. CH3NH2 D. CH3NH2C2H5
Câu 13. Hòa tan 6 gam glyxin vào 200 ml dung dịch hỗn hợp chứa HCl 0,1M và H2SO4 0,15M thu được
dung dịch X. Cho 6,8 gam NaOH tan hết trong dung dịch X được dung dịch Y. Sau khi các phản ứng
hoàn toàn, cô cạn Y thu được m gam chất rắn khan. Giá trị của m là: A. 13,59 B. 14,08 C. 12,84 D. 15,04
Câu 14. Hợp chất X không no mạch hở có công thức phân tử C5H8O2, khi tham gia phản ứng xà phòng
hóa thu được một anđehit và một muối của axit hữu cơ. Có bao nhiêu công thức cấu tạo phù hợp với X
(không kể đồng phân hình học) A. 4 B. 5 C. 2 D. 3
Câu 15. Dãy gồm các chất được xếp theo chiều lực bazơ tăng dần từ trái qua phải là
A. C6H5NH2, NH3, CH3NH2.
B. CH3NH2, C6H5NH2, NH3.
C. NH3, CH3NH2, C6H5NH2.
D. CH3NH2, NH3, C6H5NH2.
Câu 16. Để phân biệt các dung dịch riêng biệt: NaCl, MgCl2, AlCl3, FeCl3 có thể dùng dung dịch A. HCl. B. Na2SO4. C. NaOH. D. HNO3.
Câu 17. Cho dung dịch AgNO3 tác dụng với dung dịch chứa chất X thấy tạo kết tủa T màu vàng. Cho kết
tủa T tác dụng với dung dịch HNO3 dư thấy kết tủa tan. Chất X là A. KCl. B. K3PO4. C. KI. D. KBr.
Câu 18. Cho các chất CH3COOH (1), HCOO-CH2CH3 (2), CH3CH2COOH (3), CH3COO-CH2CH3 (4),
CH3CH2CH2OH (5). Dãy các chất sắp xếp theo thứ tự nhiệt độ sôi giảm dần là
A. (3) > (1) > (5) > (4) > (2).
B. (3) > (5) > (1) > (4) > (2).
C. (1) > (3) > (4) > (5) > (2).
D. 3) > (1) > (4) > (5) > (2).
Câu 19. Dung dịch FeSO4 bị lẫn CuSO4. Phương pháp đơn giản để loại tạp chất là:
A. Cho dung dịch NH3 đến dư vào dung dịch, lọc lấy kết tủa Fe(OH)2 rồi hòa tan vào dung dịch H2SO4 loãng.
B. Cho một lá nhôm vào dung dịch.
C. Cho một lá đồng vào dung dịch.
D. Cho một lá sắt vào dung dịch. Trang 2
Câu 20. Polime thiên nhiên X được sinh ra trong quá trình quang hợp của cây xanh. Ở nhiệt độ thường, X
tạo với dung dịch iot hợp chất có màu xanh tím. Polime X là A. tinh bột. B. xenlulozơ. C. saccarozơ. D. glicogen.
Câu 21. Hòa tan hết 17,76 gam hỗn hợp X gồm FeCl2, Mg, Fe(NO3)2 và Al vào dung dịch chứa 0,408
mol HCl thu được dung dịch Y và 1,6128 lít khí NO (đo ở đktc). Cho từ từ AgNO 3 vào Y đến phản ứng
hoàn toàn thì thấy lượng AgNO3 phản ứng là 0,588 mol, kết thúc phản ứng thu được 82,248 gam kết
tủa; 0,448 lít khí NO2 sản phẩm khử duy nhất (đo ở đktc) và dung dịch Z chỉ chứa m gam muối. Giá trị m gần nhất với? A. 41 gam. B. 43 gam. C. 42 gam. D. 44 gam.
Câu 22. Hợp chất hữu cơ X có công thức phân tử C2H8O3N2. Cho X phản ứng với lượng dư dung dịch
NaOH và đun nóng, thu được dung dịch Y và 1 amin bậc 2. Công thức cấu tạo của X là: A. CH3CH2NH3NO3. B. (CH3)2NH3NO3. C. H2NCH2NH3HCO3. D. HCOONH3CH3.
Câu 23. Cho dãy các kim loại: Cu, Ni, Zn, Mg, Ba và Ag. Số kim loại trong dãy phản ứng với lượng dư
dung dịch FeCl3 dư tạo kết tủa là A. 5. B. 3. C. 1. D. 4.
Câu 24. Cho các đặc điểm sau về phản ứng este hóa: (1) hoàn toàn, (2) thuận nghịch, (3) tỏa nhiệt mạnh,
(4) nhanh, (5) chậm. Phản ứng este hóa nghiệm đúng các đặc điểm? A. (1), (4). B. (2), (5). C. (1), (3), (4). D. (1), (3).
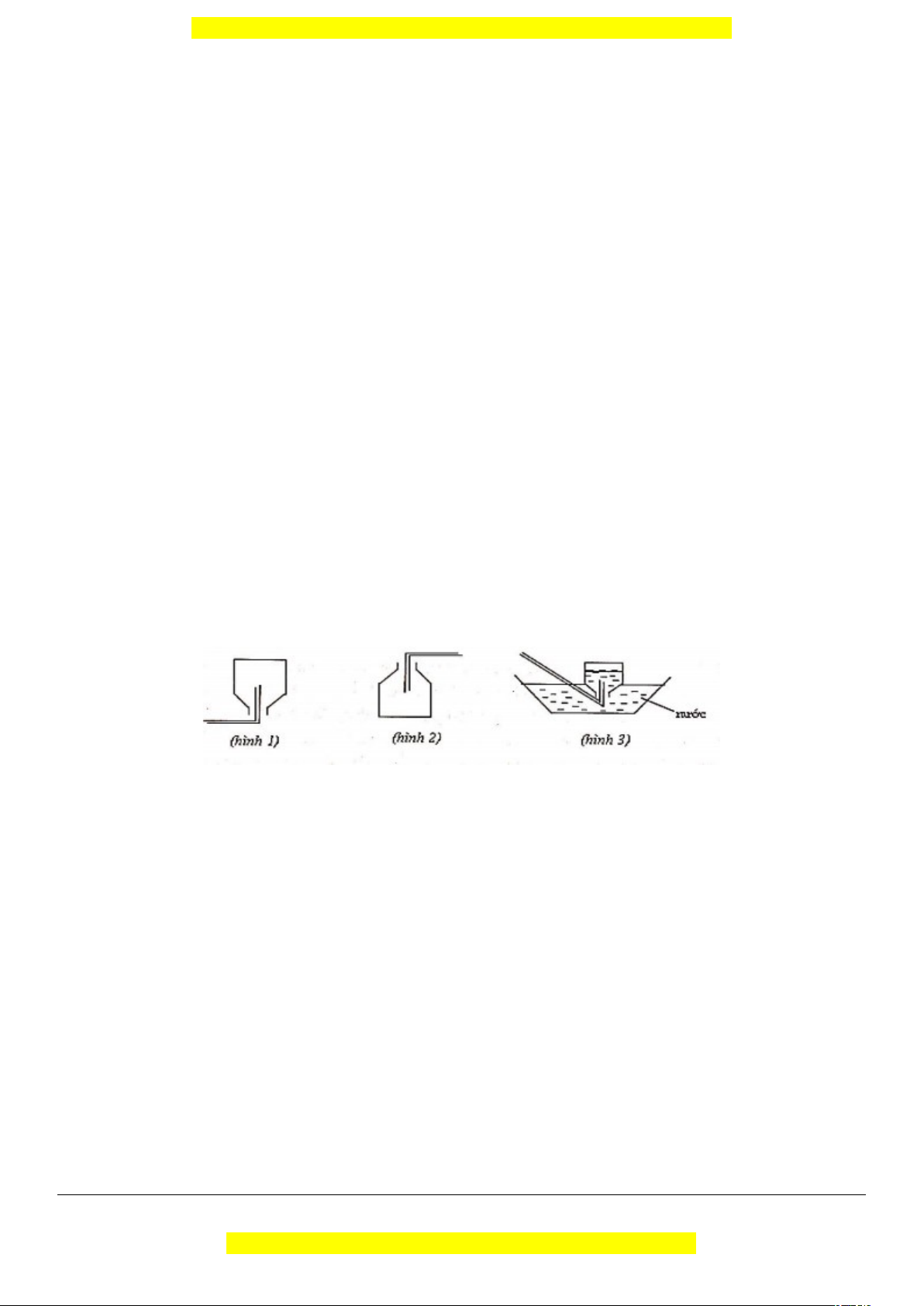
Câu 25. Các hình vẽ sau mô tả các cách thu khí thường được sử dụng khi điều chế và thu khí trong
phòng thí nghiệm. Hình 2 có thể dùng để thu được những khí nào trong các khí sau: H 2, C2H2, NH3, SO2, HCl, N2. A. H2, N2, NH3 B. H2, N2, C2H2 C.N2,H2 D. HCL, SO2
Câu 26. Tiến hành các thí nghiệm sau:
(a) Nhúng thanh Fe vào dung dịch CuSO4.
(b) Dẫn khí CO qua Fe2O3 nung nóng.
(c) Điện phân dung dịch NaCl bão hòa, có màng ngăn.
(d) Đốt bột Fe trong khí oxi.
(e) Cho kim loại Ag vào dung dịch HNO3 loãng. (f) Nung nóng Cu(NO3)2.
(g) Cho Fe2O3 vào dung dịch H2SO4 đặc, nóng. A. 2. B. 3. C. 4. D. 5.
Câu 27. Hỗn hợp khí X có thể tích 4,48 lít (đo ở đktc) gồm H2 và vinylaxetilen có tỉ lệ mol tương ứng là
3:1. Cho hỗn hợp X qua xúc tác Ni nung nóng thu được hỗn hợp khí Y có tỉ khối so với H 2 bằng 14,5.
Cho toàn bộ hỗn hợp Y ở trên từ từ qua dung dịch nước brom dư (phản ứng hoàn toàn) thì khối lượng brom đã phản ứng là A. 32,0 gam. B. 8,0 gam. C. 3,2 gam. D. 16,0 gam. Trang 3
Câu 28. Điện phân dung dịch chứa CuSO4 và NaCl với điện cực trơ, cường độ dòng điện không đổi 2A,
hiệu suất 100%. Kết quả thí nghiệm được ghi trong bảng sau:
Thời gian điện phân (giây) t 2t
Tổng số mol khí ở 2 điện cực a 2,125a Số mol Cu ở catot b
Nếu dừng điện phân ở thời điểm 5404 giây rồi nhúng thanh sắt dư vào dung dịch, sau khi phản ứng hoàn
toàn, khối lượng thanh sắt thay đổi như thế nào? A. Tăng 0,032 gam B. Giảm 0,256 gam C. Giảm 0,56 gam D. Giảm 0,304 gam
Câu 29. Cho một luồng khí O2 đi qua ống đựng 63,6 gam hỗn hợp kim loại Mg, Al và Fe nung nóng thu
được 92,4 gam chất rắn X. Hòa tan hoàn toàn lượng X trên bằng dung dịch HNO3 (dư). Sau khi các phản
ứng xảy ra hoàn toàn thu được dung dịch Y và 3,44 gam hỗn hợp khí Z. Biết có 4,25 mol HNO3 tham gia
phản ứng, cô cạn cẩn thận dung dịch Y thu được 319 gam muối. Phần trăm khối lượng của N có trong
319 gam hỗn hợp muối trên là: A. 18,082% B. 18,038% C. 18,125% D. 18,213%
Câu 30. X là este no, đơn chức, Y là este đơn chức, không no chứa một nối đôi C = C (X, Y đều mạch
hở). Đốt cháy 10,56 gam hỗn hợp E chứa X, Y cần dùng 10,08 lít O2 (đktc) thu được 6,48 gam nước. Mặt
khác, đun nóng 10,56 gam E với dung dịch NaOH vừa đủ thu được một ancol duy nhất và hỗn hợp muối
chứa a gam muối A và b gam muối B
Biết A, B là các muối của các axit cacboxylic. Tỷ lệ
gần nhất với giá trị nào sau đây? A. 0,9 B. 1,2 C. 1,0 D. 1,5
Câu 31. Thủy phân hoàn toàn a mol triglixerit X trong dung dịch NaOH vừa đủ, thu được glixerol và m
gam hỗn hợp muối. Đốt cháy hoàn toàn a mol X thu được 1,375 mol CO 2 và 1,275 mol H2O. Mặt khác,
a mol X tác dụng tối đa với 0,05 mol Br2 trong dung dịch. Giá trị của m là A. 20,15. B. 20,60. C. 23,35. D. 22,15.
Câu 32. Cho các phát biểu sau:
(a) Vinyl axetat không làm mất màu dung dịch brom.
(b) Anilin và phenol đều làm mất màu nước brom ở nhiệt độ thường.
(c) Trùng ngưng caprolactam thu được tơ capron.
(d) Cao su lưu hóa, amilopectin của tinh bột là những polime có cấu trúc mạng không gian.
(e) Peptit, tinh bột, xenlulozơ và tơ lapsan đều bị thủy phân trong môi trường axit hoặc bazơ, đun nóng.
(f) Glucozơ, axit glutamic, sobitol đều là các hợp chất hữu cơ tạp chức. Số nhận định đúng là A. 2. B. 3. C. 1. D. 4.
Câu 33. Hỗn hợp X gồm 0,15 mol axetilen, 0,1 mol vinylaxetilen, 0,1 mol etilen và 0,4 mol hiđro. Nung
hỗn hợp X với niken xúc tác, một thời gian được hỗn hợp khí Y có tỉ khối đối với hiđro bằng 12,7. Hỗn
hợp khí Y phản ứng vừa đủ với dung dịch chứa a mol Br2. Giá trị của a là A. 0,35 mol. B. 0,65 mol. C. 0,45 mol. D. 0,25 mol.
Câu 34. Cho sơ đồ chuyển hóa sau: Trang 4
X, Y, Z là các hợp chất của sắt. Cho m gam hỗn hợp E (X, Y, Z) tác dụng với dung dịch HCl dư thu được
10,752 lít NO (đktc, sản phẩm khử duy nhất) và dung dịch G chỉ chứa 2 chất tan. Cô cạn dung dịch G thu
được 253,5 gam muối khan. Phần trăm khối lượng X trong E là: A. 17,7% B. 18,8% C. 16,6% D. 19,9%
Câu 35. Thí nghiệm nào sau đây không tạo ra đơn chất?
A. Cho bột nhôm vào dung dịch NaOH.
B. Cho bột Cu vào dung dịch AgNO3.
C. Cho Na vào dung dịch FeCl2.
D. Cho dung dịch FeCl3 vào dung dịch AgNO3.
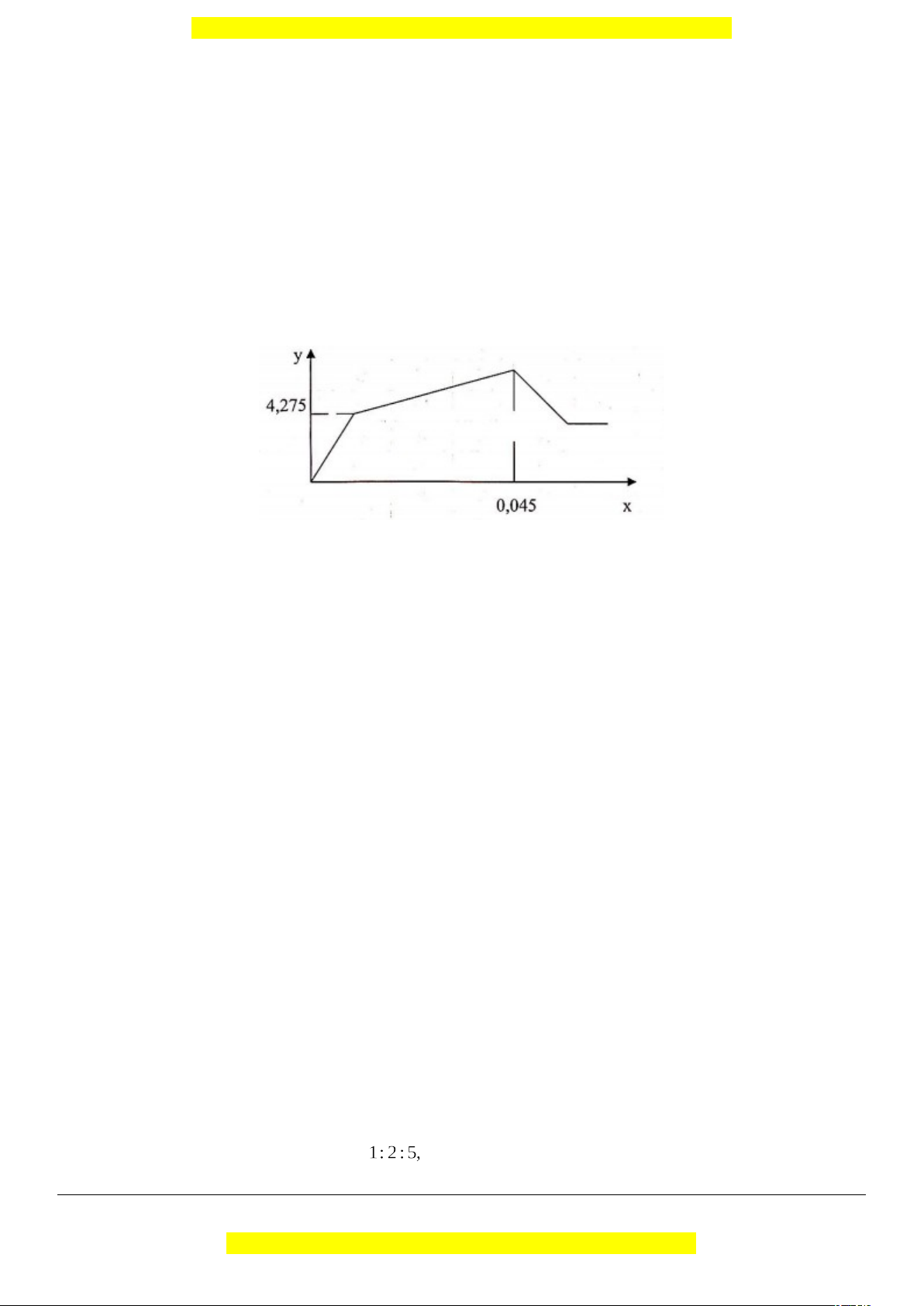
Câu 36. Nhỏ từ từ đến dư dung dịch Ba(OH)2 vào dung dịch chứa m gam hỗn hợp Al2(SO4)3 và Al(NO3)3.
Sự phụ thuộc của khối lượng kết tủa (y gam) vào số mol Ba(OH)2 (x mol) được biểu diễn bằng đồ thị bên. Giá trị của m là A. 5,97. B. 7,26. C. 7,68. D. 7,91.
Câu 37. Hỗn hợp E gồm chất X (CmH2m+4N2, là muối của axit cacboxylic hai chức) và chất Y
(CnH2n+3O2N, là muối của axit cacboxylic đơn chức). Đốt cháy hoàn toàn 0,2 mol E cần vừa đủ 0,58 mol
O2, thu được N2, CO2 và 0,84 mol H2O. Mặt khác, cho 0,2 mol E tác dụng hết với dung dịch NaOH, cô
cạn dung dịch sau phản ứng, thu được một chất khí làm xanh quỳ tím ẩm và a gam hỗn hợp hai muối khan. Giá trị của a là A. 18,56. B. 23,76. C. 24,88. D. 22,64.
Câu 38. Cho các cặp chất sau: (1) Khí Cl2 và khí O2.
(6) Dung dịch KMnO4 và khí SO2. (2) Khí H2S và khí SO2. (7) Hg và S.
(3) Khí H2S và dung dịch Pb(NO3)2.
(8) Khí CO2 và dung dịch NaClO.
(4) Khí Cl2 và dung dịch NaOH. (9) CuS và dung dịch HCl.
(5) Khí NH3 và dung dịch AlCl3.
(10) Dung dịch AgNO3 và dung dịch Fe(NO3)2.
Số cặp chất xảy ra phản ứng hóa học ở nhiệt độ thường là A. 8 B. 7 C. 9 D. 10
Câu 39. Hỗn hợp X gồm alanin; axit glutamic và hai amin thuộc dãy đồng đẳng của metyl amin. Đốt
cháy hoàn toàn 0,2 mol hỗn hợp X, thu được 1,58 mol hỗn hợp Y gồm CO2; H2) và N2. Dẫn Y qua bình
đựng H2SO4 đặc dư thấy khối lượng bình tăng 14,76 gam. Nếu cho 29,74 gam hỗn hợp X trên tác dụng
với dung dịch HCl loãng dư thu được m gam muối. Giá trị của m gần nhất là: A. 46. B. 48. C. 42. D. 40.
Câu 40. Peptit X và peptit Y đều mạch hở được cấu tạo từ các α-amino axit no có 1 nhóm –COOH; Z là
este thuần chức của glixerol và 2 axit thuộc cùng dãy đồng đẳng axit acrylic. Đốt cháy 0,16 mol hỗn hợp
E chứa X, Y, Z có tỉ lệ mol tương ứng
sản phẩm cháy gồm CO2, H2O và N2 được dẫn qua bình
đựng nước vôi trong dư thu được 196,0 gam kết tủa; đồng thời khối lượng bình tăng 112,52 gam. Khí Trang 5
Đề thi THPT Quốc Gia Hóa năm 2023 Megabook - Đề 27
0.9 K
465 lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Đề thi được cập nhật liên tục trong gói này từ nay đến hết tháng 6/2023. Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Bộ 39 đề thi TN THPT Quốc gia môn Hóa học có lời giải chi tiết được biên soạn theo chuẩn cấu trúc minh họa của Bộ Giáo dục và Đào tạo năm 2022-2023.
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(930 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN Hóa Học
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Lớp 12
Xem thêmTài liệu bộ mới nhất

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
(Đề thi có 0 trang) ĐỀ THI THỬ THPTQG NĂM 2019
CHUẨN CẤU TRÚC CỦA BỘ GIÁO DỤC – ĐỀ 0
Môn thi: HÓA HỌC
Thời gian làm bài: 50 phút, không kể thời gian phát đề
Họ, tên thí sinh:.......................................................................
Số báo danh:............................................................................
Cho biết nguyên tử khối của các nguyên tố:
H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; S = 32; Cl = 35,5; K = 39; Ca = 40;
Cr = 52;
Fe = 56; Cu = 64; Zn = 65; Ag = 108; Ba = 137.
Câu 1. Trong điều kiện thích hợp glucozơ lên men tạo thành khí CO
2
và
A. CH
3
CHO. B. HCOOH. C. CH
3
COOH. D. C
2
H
5
OH.
Câu 2. Chất X có công thức phân tử C
4
H
6
O
2
. Khi tác dụng với dung dịch NaOH sinh ra chất Y có công
thức phân tử C
3
H
3
O
2
Na. Chất X có tên gọi là
A. metyl acrylat. B. metyl metacrylat. C. metyl axetat. D. etyl acrylat.
Câu 3. Hỗn hợp X gồm C
2
H
5
NH
2
và NH
2
C
2
H
4
NH
2
, Cho 7,5 gam X tác dụng vừa đủ với dung dịch
thu được 17,3 gam muối. Phần trăm khối lượng của C
2
H
5
NH
2
trong X là:
A. 60. B. 90. C. 48. D. 72.
Câu 4. Ở điều kiện thường, kim loại nào sau đây không phản ứng với nước:
A. Rb. B. Na. C. Fe. D. Ca.
Câu 5. Cho 0,6 gam một kim loại hóa trị II phản ứng hết với dung dịch H
2
SO
4
loãng, dư, thu được 0,56
lít H
2
(đktc). Kim loại đó là
A. Ca. B. Zn. C. Mg. D. Sr.
Câu 6. Cho các phát biểu sau:
(1) Amino axit là các chất rắn màu trắng, kết tinh, tương đối dễ tan trong nước.
(2) Các amin có số cacbon nhỏ hơn hoặc bằng 3, đơn chức, mạch hở là chất khí mùi khai giống
(3) Sợi bông, tơ tằm và tơ olon thuộc loại polime thiên nhiên.
(4) Saccarozơ và mantozơ chỉ có cấu tạo mạch vòng.
(5) Trùng ngưng axit aminoenantoic thu được nilon – 6.
Số phát biểu sai là
A. 4 B. 3 C. 5 D. 2
Câu 7. Trong bốn polime cho dưới đây, polime nào cùng loại polime với tơ lapsan
A. Tơ tằm B. Tơ nilon-6,6 C. Xenlulozơ trinitrat D. Cao su thiên nhiên
Câu 8. Hòa tan 5,4 gam bột Al vào 150 ml dung dịch X chứa Fe(NO
3
)
3
1M và Cu(NO
3
)
2
1M. Kết thúc
phản ứng thu được của m là
A. 10,95. B. 13,20. C. 13,80. D. 15,20.
Trang 1
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Câu 9. Este X có công thức phân tử là C
4
H
6
O
2
khi thủy phân trong môi trường axit thu được ancol có khả
năng làm mất màu nước brom. Công thức cấu tạo thu gọn của X là:
A. CH
3
COO-CH=CH
2
B. HCOO-CH=CH-CH
3
C. HCOO-CH
2
CH=CH
2
D. CH
2
=CH-COOCH
3
Câu 10. Hợp chất ion G tạo nên từ các ion đơn nguyên tử M
2+
và X
2-
. Tổng số hạt (nơtron, proton,
electron) trong phân tử G là 84, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 28 hạt.
Số hạt mang điện của ion X
2-
ít hơn số hạt mang điện của ion M
2+
là 20 hạt. Vị trí của M trong bảng tuần
hoàn là
A. ô 8, chu kì 2, nhóm VIA. B. ô 26, chu kì 4, nhóm VIIIB.
C. ô 12, chu kì 3, nhóm IIA. D. ô 20, chu kì 4, nhóm IIA.
Câu 11. Polime nào sau đây có cấu trúc mạng không gian?
A. Cao su buna B. Aminozơ C. Glicogen D. Cao su lưu hóa
Câu 12. N – metyletanamin có công thức là:
A. C
2
H
5
NHCH
3
B. CH
3
NHCH
3
C. CH
3
NH
2
D. CH
3
NH
2
C
2
H
5
Câu 13. Hòa tan 6 gam glyxin vào 200 ml dung dịch hỗn hợp chứa HCl 0,1M và H
2
SO
4
0,15M thu được
dung dịch X. Cho 6,8 gam NaOH tan hết trong dung dịch X được dung dịch Y. Sau khi các phản ứng
hoàn toàn, cô cạn Y thu được m gam chất rắn khan. Giá trị của m là:
A. 13,59 B. 14,08 C. 12,84 D. 15,04
Câu 14. Hợp chất X không no mạch hở có công thức phân tử C
5
H
8
O
2
, khi tham gia phản ứng xà phòng
hóa thu được một anđehit và một muối của axit hữu cơ. Có bao nhiêu công thức cấu tạo phù hợp với X
(không kể đồng phân hình học)
A. 4 B. 5 C. 2 D. 3
Câu 15. Dãy gồm các chất được xếp theo chiều lực bazơ tăng dần từ trái qua phải là
A. C
6
H
5
NH
2
, NH
3
, CH
3
NH
2
. B. CH
3
NH
2
, C
6
H
5
NH
2
, NH
3
.
C. NH
3
, CH
3
NH
2
, C
6
H
5
NH
2
. D. CH
3
NH
2
, NH
3
, C
6
H
5
NH
2
.
Câu 16. Để phân biệt các dung dịch riêng biệt: NaCl, MgCl
2
, AlCl
3
, FeCl
3
có thể dùng dung dịch
A. HCl. B. Na
2
SO
4
. C. NaOH. D. HNO
3
.
Câu 17. Cho dung dịch AgNO
3
tác dụng với dung dịch chứa chất X thấy tạo kết tủa T màu vàng. Cho kết
tủa T tác dụng với dung dịch HNO
3
dư thấy kết tủa tan. Chất X là
A. KCl. B. K
3
PO
4
. C. KI. D. KBr.
Câu 18. Cho các chất CH
3
COOH (1), HCOO-CH
2
CH
3
(2), CH
3
CH
2
COOH (3), CH
3
COO-CH
2
CH
3
(4),
CH
3
CH
2
CH
2
OH (5). Dãy các chất sắp xếp theo thứ tự nhiệt độ sôi giảm dần là
A. (3) > (1) > (5) > (4) > (2). B. (3) > (5) > (1) > (4) > (2).
C. (1) > (3) > (4) > (5) > (2). D. 3) > (1) > (4) > (5) > (2).
Câu 19. Dung dịch FeSO
4
bị lẫn CuSO
4
. Phương pháp đơn giản để loại tạp chất là:
A. Cho dung dịch NH
3
đến dư vào dung dịch, lọc lấy kết tủa Fe(OH)
2
rồi hòa tan vào dung dịch H
2
SO
4
loãng.
B. Cho một lá nhôm vào dung dịch.
C. Cho một lá đồng vào dung dịch.
D. Cho một lá sắt vào dung dịch.
Trang 2
Mọi thắc mắc xin vui lòng xin liên hệ hotline: 084 283 45 85
Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Câu 20. Polime thiên nhiên X được sinh ra trong quá trình quang hợp của cây xanh. Ở nhiệt độ thường, X
tạo với dung dịch iot hợp chất có màu xanh tím. Polime X là
A. tinh bột. B. xenlulozơ. C. saccarozơ. D. glicogen.
Câu 21. Hòa tan hết 17,76 gam hỗn hợp X gồm FeCl
2
, Mg, Fe(NO
3
)
2
và Al vào dung dịch chứa 0,408
mol HCl thu được dung dịch Y và 1,6128 lít khí NO (đo ở đktc). Cho từ từ AgNO
3
vào Y đến phản ứng
hoàn toàn thì thấy lượng AgNO
3
phản ứng là 0,588 mol, kết thúc phản ứng thu được 82,248 gam kết
tủa; 0,448 lít khí NO
2
sản phẩm khử duy nhất (đo ở đktc) và dung dịch Z chỉ chứa m gam muối. Giá trị
m gần nhất với?
A. 41 gam. B. 43 gam. C. 42 gam. D. 44 gam.
Câu 22. Hợp chất hữu cơ X có công thức phân tử C
2
H
8
O
3
N
2
. Cho X phản ứng với lượng dư dung dịch
NaOH và đun nóng, thu được dung dịch Y và 1 amin bậc 2. Công thức cấu tạo của X là:
A. CH
3
CH
2
NH
3
NO
3
. B. (CH
3
)
2
NH
3
NO
3
. C. H
2
NCH
2
NH
3
HCO
3
. D. HCOONH
3
CH
3
.
Câu 23. Cho dãy các kim loại: Cu, Ni, Zn, Mg, Ba và Ag. Số kim loại trong dãy phản ứng với lượng dư
dung dịch FeCl
3
dư tạo kết tủa là
A. 5. B. 3. C. 1. D. 4.
Câu 24. Cho các đặc điểm sau về phản ứng este hóa: (1) hoàn toàn, (2) thuận nghịch, (3) tỏa nhiệt mạnh,
(4) nhanh, (5) chậm. Phản ứng este hóa nghiệm đúng các đặc điểm?
A. (1), (4). B. (2), (5). C. (1), (3), (4). D. (1), (3).
Câu 25. Các hình vẽ sau mô tả các cách thu khí thường được sử dụng khi điều chế và thu khí trong
phòng thí nghiệm. Hình 2 có thể dùng để thu được những khí nào trong các khí sau: H
2
, C
2
H
2
, NH
3
,
SO
2
, HCl, N
2
.
A. H
2
, N
2
, NH
3
B. H
2
, N
2
, C
2
H
2
C.N
2,
H
2
D. HCL, SO
2
Câu 26. Tiến hành các thí nghiệm sau:
(a) Nhúng thanh Fe vào dung dịch CuSO
4
.
(b) Dẫn khí CO qua Fe
2
O
3
nung nóng.
(c) Điện phân dung dịch NaCl bão hòa, có màng ngăn.
(d) Đốt bột Fe trong khí oxi.
(e) Cho kim loại Ag vào dung dịch HNO
3
loãng.
(f) Nung nóng Cu(NO
3
)
2
.
(g) Cho Fe
2
O
3
vào dung dịch H
2
SO
4
đặc, nóng.
A. 2. B. 3. C. 4. D. 5.
Câu 27. Hỗn hợp khí X có thể tích 4,48 lít (đo ở đktc) gồm H
2
và vinylaxetilen có tỉ lệ mol tương ứng là
3:1. Cho hỗn hợp X qua xúc tác Ni nung nóng thu được hỗn hợp khí Y có tỉ khối so với H
2
bằng 14,5.
Cho toàn bộ hỗn hợp Y ở trên từ từ qua dung dịch nước brom dư (phản ứng hoàn toàn) thì khối lượng
brom đã phản ứng là
A. 32,0 gam. B. 8,0 gam. C. 3,2 gam. D. 16,0 gam.
Trang 3
Mọi thắc mắc xin vui lòng xin liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Câu 28. Điện phân dung dịch chứa CuSO
4
và NaCl với điện cực trơ, cường độ dòng điện không đổi 2A,
hiệu suất 100%. Kết quả thí nghiệm được ghi trong bảng sau:
Thời gian điện phân (giây) t 2t
Tổng số mol khí ở 2 điện cực a 2,125a
Số mol Cu ở catot b
Nếu dừng điện phân ở thời điểm 5404 giây rồi nhúng thanh sắt dư vào dung dịch, sau khi phản ứng hoàn
toàn, khối lượng thanh sắt thay đổi như thế nào?
A. Tăng 0,032 gam B. Giảm 0,256 gam C. Giảm 0,56 gam D. Giảm 0,304 gam
Câu 29. Cho một luồng khí O
2
đi qua ống đựng 63,6 gam hỗn hợp kim loại Mg, Al và Fe nung nóng thu
được 92,4 gam chất rắn X. Hòa tan hoàn toàn lượng X trên bằng dung dịch HNO
3
(dư). Sau khi các phản
ứng xảy ra hoàn toàn thu được dung dịch Y và 3,44 gam hỗn hợp khí Z. Biết có 4,25 mol HNO
3
tham gia
phản ứng, cô cạn cẩn thận dung dịch Y thu được 319 gam muối. Phần trăm khối lượng của N có trong
319 gam hỗn hợp muối trên là:
A. 18,082% B. 18,038% C. 18,125% D. 18,213%
Câu 30. X là este no, đơn chức, Y là este đơn chức, không no chứa một nối đôi C = C (X, Y đều mạch
hở). Đốt cháy 10,56 gam hỗn hợp E chứa X, Y cần dùng 10,08 lít O
2
(đktc) thu được 6,48 gam nước. Mặt
khác, đun nóng 10,56 gam E với dung dịch NaOH vừa đủ thu được một ancol duy nhất và hỗn hợp muối
chứa a gam muối A và b gam muối B Biết A, B là các muối của các axit cacboxylic. Tỷ lệ
gần nhất với giá trị nào sau đây?
A. 0,9 B. 1,2 C. 1,0 D. 1,5
Câu 31. Thủy phân hoàn toàn a mol triglixerit X trong dung dịch NaOH vừa đủ, thu được glixerol và m
gam hỗn hợp muối. Đốt cháy hoàn toàn a mol X thu được 1,375 mol CO
2
và 1,275 mol H
2
O. Mặt khác,
a mol X tác dụng tối đa với 0,05 mol Br
2
trong dung dịch. Giá trị của m là
A. 20,15. B. 20,60. C. 23,35. D. 22,15.
Câu 32. Cho các phát biểu sau:
(a) Vinyl axetat không làm mất màu dung dịch brom.
(b) Anilin và phenol đều làm mất màu nước brom ở nhiệt độ thường.
(c) Trùng ngưng caprolactam thu được tơ capron.
(d) Cao su lưu hóa, amilopectin của tinh bột là những polime có cấu trúc mạng không gian.
(e) Peptit, tinh bột, xenlulozơ và tơ lapsan đều bị thủy phân trong môi trường axit hoặc bazơ, đun
nóng.
(f) Glucozơ, axit glutamic, sobitol đều là các hợp chất hữu cơ tạp chức. Số nhận định đúng là
A. 2. B. 3. C. 1. D. 4.
Câu 33. Hỗn hợp X gồm 0,15 mol axetilen, 0,1 mol vinylaxetilen, 0,1 mol etilen và 0,4 mol hiđro. Nung
hỗn hợp X với niken xúc tác, một thời gian được hỗn hợp khí Y có tỉ khối đối với hiđro bằng 12,7. Hỗn
hợp khí Y phản ứng vừa đủ với dung dịch chứa a mol Br
2
. Giá trị của a là
A. 0,35 mol. B. 0,65 mol. C. 0,45 mol. D. 0,25 mol.
Câu 34. Cho sơ đồ chuyển hóa sau:
Trang 4
Mọi thắc mắc xin vui lòng xin liên hệ hotline: 084 283 45 85
Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
X, Y, Z là các hợp chất của sắt. Cho m gam hỗn hợp E (X, Y, Z) tác dụng với dung dịch HCl dư thu được
10,752 lít NO (đktc, sản phẩm khử duy nhất) và dung dịch G chỉ chứa 2 chất tan. Cô cạn dung dịch G thu
được 253,5 gam muối khan. Phần trăm khối lượng X trong E là:
A. 17,7% B. 18,8% C. 16,6% D. 19,9%
Câu 35. Thí nghiệm nào sau đây không tạo ra đơn chất?
A. Cho bột nhôm vào dung dịch NaOH. B. Cho bột Cu vào dung dịch AgNO
3
.
C. Cho Na vào dung dịch FeCl
2
. D. Cho dung dịch FeCl
3
vào dung dịch AgNO
3
.
Câu 36. Nhỏ từ từ đến dư dung dịch Ba(OH)
2
vào dung dịch chứa m gam hỗn hợp Al
2
(SO
4
)
3
và Al(NO
3
)
3
.
Sự phụ thuộc của khối lượng kết tủa (y gam) vào số mol Ba(OH)
2
(x mol) được biểu diễn bằng đồ thị bên.
Giá trị của m là
A. 5,97. B. 7,26. C. 7,68. D. 7,91.
Câu 37. Hỗn hợp E gồm chất X (C
m
H
2m+4
N
2
, là muối của axit cacboxylic hai chức) và chất Y
(C
n
H
2n+3
O
2
N, là muối của axit cacboxylic đơn chức). Đốt cháy hoàn toàn 0,2 mol E cần vừa đủ 0,58 mol
O
2
, thu được N
2
, CO
2
và 0,84 mol H
2
O. Mặt khác, cho 0,2 mol E tác dụng hết với dung dịch NaOH, cô
cạn dung dịch sau phản ứng, thu được một chất khí làm xanh quỳ tím ẩm và a gam hỗn hợp hai muối
khan. Giá trị của a là
A. 18,56. B. 23,76. C. 24,88. D. 22,64.
Câu 38. Cho các cặp chất sau:
(1) Khí Cl
2
và khí O
2
. (6) Dung dịch KMnO
4
và khí SO
2
.
(2) Khí H
2
S và khí SO
2
. (7) Hg và S.
(3) Khí H
2
S và dung dịch Pb(NO
3
)
2
. (8) Khí CO
2
và dung dịch NaClO.
(4) Khí Cl
2
và dung dịch NaOH. (9) CuS và dung dịch HCl.
(5) Khí NH
3
và dung dịch AlCl
3
. (10) Dung dịch AgNO
3
và dung dịch Fe(NO
3
)
2
.
Số cặp chất xảy ra phản ứng hóa học ở nhiệt độ thường là
A. 8 B. 7 C. 9 D. 10
Câu 39. Hỗn hợp X gồm alanin; axit glutamic và hai amin thuộc dãy đồng đẳng của metyl amin. Đốt
cháy hoàn toàn 0,2 mol hỗn hợp X, thu được 1,58 mol hỗn hợp Y gồm CO
2
; H
2
) và N
2
. Dẫn Y qua bình
đựng H
2
SO
4
đặc dư thấy khối lượng bình tăng 14,76 gam. Nếu cho 29,74 gam hỗn hợp X trên tác dụng
với dung dịch HCl loãng dư thu được m gam muối. Giá trị của m gần nhất là:
A. 46. B. 48. C. 42. D. 40.
Câu 40. Peptit X và peptit Y đều mạch hở được cấu tạo từ các α-amino axit no có 1 nhóm –COOH; Z là
este thuần chức của glixerol và 2 axit thuộc cùng dãy đồng đẳng axit acrylic. Đốt cháy 0,16 mol hỗn hợp
E chứa X, Y, Z có tỉ lệ mol tương ứng sản phẩm cháy gồm CO
2
, H
2
O và N
2
được dẫn qua bình
đựng nước vôi trong dư thu được 196,0 gam kết tủa; đồng thời khối lượng bình tăng 112,52 gam. Khí
Trang 5
Mọi thắc mắc xin vui lòng xin liên hệ hotline: 084 283 45 85