Trường: ……………………………….. Họ và tên giáo viên:
Tổ: …………………………………… ……………………….
BÀI 6: GIỚI THIỆU VỂ LIÊN KẾT HOÁ HỌC
Thời gian thực hiện: 04 tiết I. MỤC TIÊU 1. Kiến thức
- Nêu được mô hình sắp xếp electron trong vỏ nguyên tử của một số nguyên tố khí
hiếm; sự hình thành liên kết cộng hoá trị theo nguyên tắc dùng chung electron để tạo
ra lớp electron ngoài cùng giống nguyên tử nguyên tố khí hiếm.
- Nêu được sự hình thành liên kết ion theo nguyên tắc cho và nhận electron để tạo ra
ion có lớp electron ngoài cùng giống nguyên tử nguyên tố khí hiếm.
- Chỉ ra được sự khác nhau về một số tính chất của chất ion và chất cộng hóa trị. 2. Năng lực 2.1. Năng lực chung
- Tự chủ và tự học: Chủ động, tích cực tìm hiểu về vỏ nguyên tử của một số nguyên
tố khí hiếm; sự hình thành liên kết cộng hoá trị theo nguyên tắc dùng chung electron
để tạo ra lớp vỏ electron của nguyên tó khí hiếm; sự hình thành liên kết ion theo
nguyên tắc cho và nhận electron để tạo ra lớp vỏ electron của nguyên tố khí hiếm; Tự
tìm hiểu sự khác nhau về một số tính chất của chất ion và chất cộng hoá trị.
- Giao tiếp và hợp tác: Sử dụng ngôn ngữ khoa học để diễn đạt về liên kết hoá học;
chất ion và chất cộng hoá trị. Hoạt động nhóm một cách hiệu quả theo đúng yêu cẩu
của GV, đảm bảo các thành viên trong nhóm đều được tham gia và trình bày báo cáo tốt.
- Giải quyết vấn để và sáng tạo: Thảo luận với các thành viên trong nhóm nhằm giải
quyết các vấn để trong bài học để hoàn thành nhiệm vụ học tập tốt nhất.
2.2. Năng lực khoa học tự nhiên
- Nhận thức khoa học tự nhiên: Nêu được đặc điểm vỏ nguyên tử của một số nguyên
tố khí hiếm; khái niệm vể liên kết cộng hoá trị, liên kết ion, electron góp chung, sự
cho - nhận electron; chất ion và chất cộng hoá trị.
- Tìm hiểu tự nhiên: Quan sát một số phân tử trong tự nhiên (hydrochloric acid,
calcium chloride, ethanol, ...) thông qua các hình ảnh mô phỏng cấu trúc phân tử.
- Vận dụng kiến thức, kĩ năng đã học: Nhận biết được một số nguyên tố khí hiếm;
loại liên kết có trong các phân tử; chất ion, chất cộng hoá trị và ứng dụng của nó trong đời sống. 3. Phẩm chất
- Tham gia tích cực hoạt động nhóm phù hợp với khả năng của bản thân;
- Cẩn thận, trung thực và thực hiện an toàn trong quá trình làm thực hành;
- Có niềm say mê, hứng thú với việc khám phá và học tập khoa học tự nhiên.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU 1. Giáo viên
- Tranh ảnh phóng to các hình ảnh trong SGK (nếu có) hoặc có thể thay thế bằng hình
chiếu lên màn chiếu (yêu cầu các hình ảnh phải đảm bảo rõ nét, dễ nhìn).
- Thiết kế các phiếu học tập. 2. Học sinh
- Ôn tập bài cũ và chuẩn bị bài mới.
III. TIẾN TRÌNH DẠY HỌC
1. Hoạt động 1: Mở đầu a) Mục tiêu
- Giúp học sinh xác định được vấn đề sự sắp xếp e lớp ngoài cùng của khí hiếm
khác với e lớp ngoài cùng của nguyên tử nguyên tố khác. b) Nội dung
- Học sinh căn cứ vào hình ảnh mẫu mô hình nguyên tử khí hiếm, so sánh với các
nguyên tố khác, nêu được (một phần) vấn đề cần giải quyết.
c) Sản phẩm
- Câu trả lời của học sinh (có thể đúng hoặc chưa đúng), GV không nhận xét tính
đúng – sai mà dựa vào đó đặt vấn đề vào bài học.
d) Tổ chức thực hiện
*Chuyển giao nhiệm vụ học tập
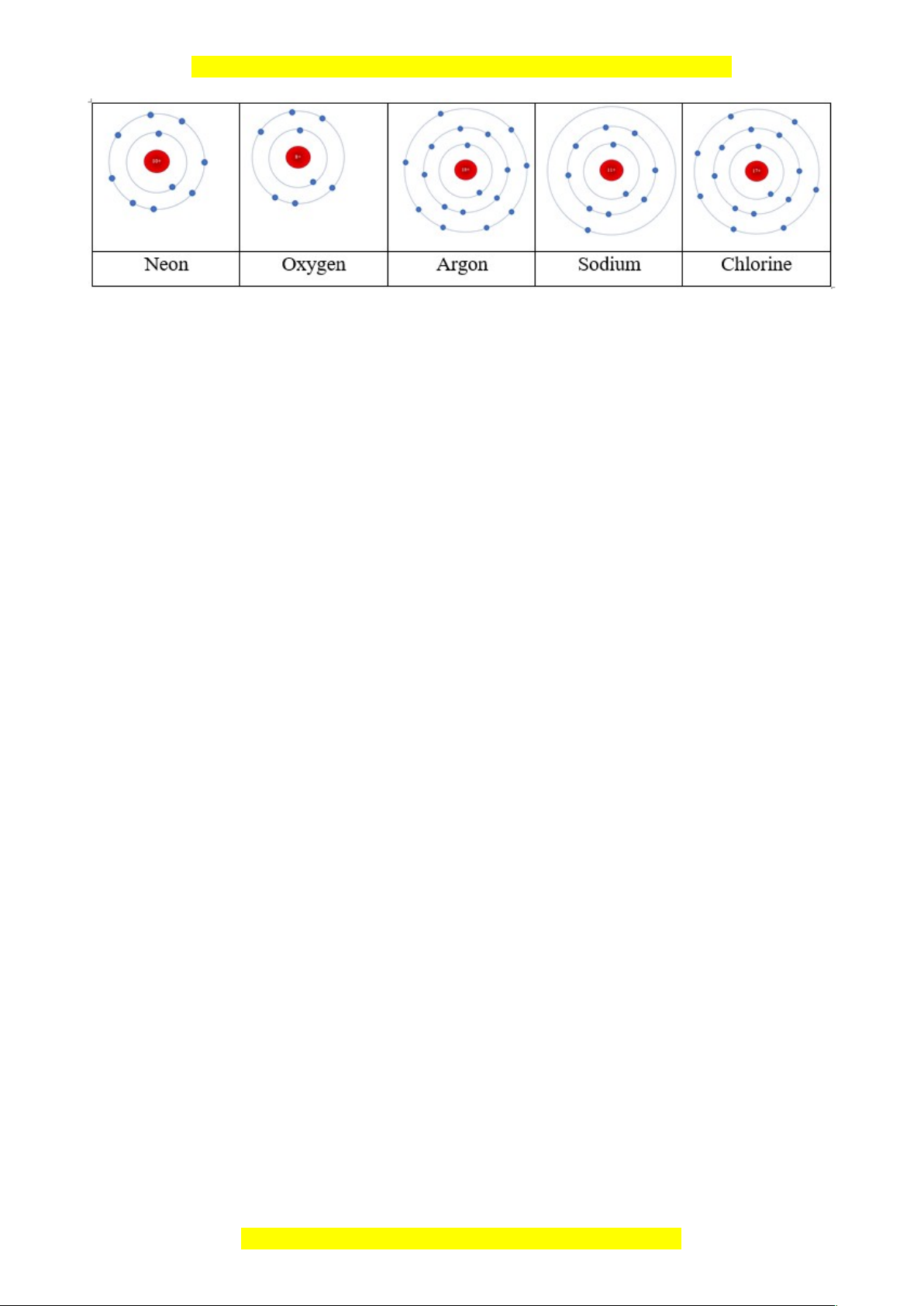
GV cho HS quan sát mô hình nguyên tử neon, argon, oxygen, sodium, chlorine:
Dự đoán nguyên nhân vì sao:
+ Neon, argon không liên kết với các chất khác được?
+ Oxygen có thể tự liên kết với nhau để tạo ra phân tử khí?
+ Sodium có thể liên kết với chlorine để tạo phân tử rắn?
*Thực hiện nhiệm vụ học tập
- HS hoạt động cá nhân nghiên cứu câu hỏi.
- HS chia sẻ thông tin theo cặp trong bàn.
*Báo cáo kết quả và thảo luận
- GV gọi ngẫu nhiên học sinh trình bày đáp án, mỗi HS trình bày 1 nội dung, những
HS trình bày sau không trùng nội dung với HS trình bày trước. GV liệt kê đáp án của HS trên bảng.
*Đánh giá kết quả thực hiện nhiệm vụ
- Học sinh nhận xét, bổ sung, đánh giá:
- Giáo viên nhận xét, đánh giá:
Giáo viên gieo vấn đề cần tìm hiểu trong bài học: Để trả lời câu hỏi trên đầy đủ và
chính xác nhất chúng ta vào bài học hôm nay.
Giáo viên nêu mục tiêu bài học:
2. Hoạt động 2: Hình thành kiến thức mới
2. 1: Tìm hiểu vỏ nguyên tử khí hiếm a) Mục tiêu
Nêu được mô hình sắp xếp electron trong vỏ nguyên tử của một số nguyên tố khí hiếm. b) Nội dung
- Học sinh quan sát hình 6.1 Hình mô phỏng vỏ nguyên tử một số nguyên tố khí
hiếm, trả lời được câu hỏi:
H1: Trừ helium, vỏ nguyên tử của các nguyên tố còn lại ở hình 6.1 có những điểm giống và khác nhau gì?
c) Sản phẩm
Vỏ nguyên tử của các nguyên tố khí hiếm đều có 8 electron ở lớp ngoài cùng, riêng
helium ở lớp ngoài cùng chỉ có 2 electron.
d) Tổ chức thực hiện
Hoạt động của giáo viên và học sinh Nội dung
* Chuyển giao nhiệm vụ học tập
I. Vỏ nguyên tử khí hiếm
- GV giao nhiệm vụ học tập cặp đôi, quan sát - Nhóm khí hiếm là nhóm các
hình 6.1 (phóng to trên màn hình).
nguyên tố hoạt động hóa học
Ghi lại kết quả vào bảng sau: kém. Tên khí hiếm
Số e lớp ngoài cùng
Nhóm khí hiếm gồm: helium He (He); neon (Ne); argon (Ar); Ne krypton (Kr); xenon (Xe), … Ar
- Vỏ nguyên tử của các nguyên Kr
tố khí hiếm đều có 8 electron ở Xe
lớp ngoài cùng, riêng helium ở
Trả lời câu hỏi: Trừ helium, vỏ nguyên tử của lớp ngoài cùng có 2 electron.
các nguyên tố còn lại ở hình 6.1 có những điểm Chú ý: giống và khác nhau gì?
Để có số electron ở lớp ngoài
*Thực hiện nhiệm vụ học tập
cùng giống nguyên tử của
HS thảo luận cặp đôi, thống nhất đáp án.
nguyên tố khí hiếm, các nguyên
*Báo cáo kết quả và thảo luận
tử của các nguyên tố có khuynh
GV gọi ngẫu nhiên một HS đại diện cho một hướng nhường hoặc nhận hoặc
nhóm trình bày, các nhóm khác bổ sung (nếu có). góp chung electron.
*Đánh giá kết quả thực hiện nhiệm vụ
+ Nguyên tử của các nguyên tố
- Học sinh nhận xét, bổ sung, đánh giá.
kim loại thường có khuynh
hướng nhường electron ở lớp
Giáo án Bài 6 Hóa học 7 Chân trời sáng tạo (2024): Giới thiệu về liên kết hóa học
0.9 K
460 lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Bộ giáo án Hóa học 7 Chân trời sáng tạo đã cập nhật đủ Cả năm.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Bộ giáo án Hóa học 7 Chân trời sáng tạo năm 2024 mới, chuẩn nhất được thiết kế theo phong cách hiện đại, đẹp mắt, trình bày chi tiết cho từng phần học và bám sát chương trình Sách giáo khoa Hóa học 7 Chân trời sáng tạo.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(919 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN KHTN
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Lớp 7
Xem thêmTài liệu bộ mới nhất

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
BÀI 6: GIỚI THIỆU VỂ LIÊN KẾT HOÁ HỌC
I. MỤC TIÊU
1. Kiến thức
!"#$%&'(')*)+,-."/%0,012
"3%$*1/4),&56)*) 78
*9')*)60,-,012"
!%$*1),&:)*) 78
;*9')*)60,-,012"
<= !%1>"/%02?.??/;4
2. Năng lực
2.1. Năng lực chung
.<. /@2$"7>+,-."/%0,
012"3%$*1/4),&56)*)
78*9'+ )*) .,;12"3%$*1)
,&:)*) 78*9'+)*).,012"3
$"7%1>"/%02?.??/4
A'!'B-5C#D1 75E 8>*13
??/48 /;""/FG) H,I
.AJ@ G"KG;" > !"$K,K
0
AGF,? 7%8G*:9;"L"G
F,? 7K 7"C:'0?
2.2. Năng lực khoa học tự nhiên
:M1 ! N 7"+,-."/%0,
012"31"7*1/4@*1@)*);'@%
:)*)3??/4
Mọi thắc mắc xin vui lòng liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
$"7O%"/%0'P- Q,5*5@
*"*5)@)*@R#F$G"#'+?H'P-
J:5C1M@1ST U:K !"/%0,012"3
*8*1;'P-3?@?/4M5C.;
%0
3. Phẩm chất
"28 /;"'6!'91GT.KGP3
<I:@F$*"3
<;>"%,"@MH91"':'1
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
1. Giáo viên
G';$GBAVQ;RN;7,KL$
*"Q,W$G'G G"KGXY@5E$R
1':'
2. Học sinh
- Z:'K[IK4K"9
III. TIẾN TRÌNH DẠY HỌC
1. Hoạt động 1: Mở đầu
a) Mục tiêu
AH'%( 4 !? >%%&'(')*9'6.12"
19)*9'6.,-,01
b) Nội dung
%TM$G"\"#$,-12"@%%9
,01@ !Q"/'WR? >WGF,
c) Sản phẩm
<PG*.%Q;7 HN HR@AJ1#:(Y2
H]%"5 ; N? >K
d) Tổ chức thực hiện
*Chuyển giao nhiệm vụ học tập
AJBF%"#$,-neon, argon, oxygen, sodium, chlorine:
Mọi thắc mắc xin vui lòng liên hệ hotline: 084 283 45 85
Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Dự đoán nguyên nhân vì sao:
^)@1#*19?1 !_
^`(,);7*19 78'P-12_
^B5";7*19*) 78'P-&_
*Thực hiện nhiệm vụ học tập
B8 /PMP+
- B%a#)N'K
*Báo cáo kết quả và thảo luận
AJ\%$K, '@"bB$K,c/5@D
B$K,%1#6/59B$K,9AJ*1 '.
BKG.
*Đánh giá kết quả thực hiện nhiệm vụ
- Học sinh nhận xét, bổ sung, đánh giá:
- Giáo viên nhận xét, đánh giá:
Giáo viên gieo vấn đề cần tìm hiểu trong bài học: d7G*P+ W, .
2(?HK#",
Giáo viên nêu mục tiêu bài học:
2. Hoạt động 2: Hình thành kiến thức mới
2. 1: Tìm hiểu vỏ nguyên tử khí hiếm
a) Mục tiêu
!"#$%&'(')*)+,-."/%0,012
".
b) Nội dung
Mọi thắc mắc xin vui lòng liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
%F%$ec$"#'++,-"/%0,012
"@G* !P+
cf)*"@+,-.,0g*8h$ec;D 7"
01$_
c) Sản phẩm
J+,-.,012" >;i)*)h*9'6@
)*"h*9'6=;j)*)
d) Tổ chức thực hiện
Hoạt động của giáo viên và học sinh Nội dung
* Chuyển giao nhiệm vụ học tập
AJ"C:'N' #@F%
$ecQ';"$R
A*81FGKG%
Tên khí hiếm Số e lớp ngoài cùng
)
)
k
V
l)
G*P+f)*"@+,-.
,0g*8h$ec;D 7"
01$_
*Thực hiện nhiệm vụ học tập
BG*:N' #@0? '
*Báo cáo kết quả và thảo luận
AJ\"/B 85"/
;"$K,@;"1K%Q;R
*Đánh giá kết quả thực hiện nhiệm vụ
- Học sinh nhận xét, bổ sung, đánh giá.
I. Vỏ nguyên tử khí hiếm
;" 12 " * ;"
, 0 8 / ;
1Y"
;" 12 " m" )*"
Q)R3 ) Q)R3 QkR3
1,'QVR3()Ql)R@
J+,-.,
012" >;i)*)h
*9'6@)*"h
*9'6;j)*)
Chú ý:
d7 ; %0 )*) h *9'
6 0 , - .
,012"@,
-.,0;1,
9 N : N
;')*)
^,-.,0
1" *8 ; 1,
9 )*) h *9'
Mọi thắc mắc xin vui lòng liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
- Giáo viên nhận xét, đánh giá.
AJ:(Y0/5Vỏ nguyên tử
khí hiếm đều có 8 electron ở lớp ngoài cùng,
riêng helium ở lớp ngoài cùng có 2 electron.
GV phân tích thêm: Với electron lớp ngoài
cùng là 8 thì nguyên tử đạt cấu hình bền, khó
hoặc không thể liên kết với nguyên tử nguyên tố
khác hoặc chính nó. Do đó khí hiếm còn có tên
khác là khí trơ. Các nguyên tử nguyên tố khác
liên kết với nhau thường đạt tới cấu hình bền.
6
^,-.,0
' 1" ; 1,
9 : " N ;'
)*) 7;*9')*)
6K>D
Hoạt động 2. 2: Tìm hiểu liên kết ion
a) Mục tiêu
!%$*1),&:)*) 78
;*9')*)60,-,012"
b) Nội dung
%F%$ej@en@e':'%0cf ;B"#G
!%$5o@P"*1
PHIẾU HỌC TẬP SỐ 1
Câu 1: O%$ej@)"U,"#G%8%5"@")%"
:(Y>%0)*)*9'6.,K%'PK0
)*).j,0%'PK0)*).,-12"_
Câu 2: O%$en@)"U,"#G%8*5)@(5):
(Y>%0)*)*9'6.,K%'PK0)*).
j,0%'PK0)*).,-12"_
Câu 3: O%$e@)"U,"#GF$8*1'P
-%5"*5)"/%0M5C.%5"*5) %0
c) Sản phẩm
<PG*.%
TRẢ LỜI PHIẾU HỌC TẬP SỐ 1
Mọi thắc mắc xin vui lòng liên hệ hotline: 084 283 45 85