SỞ GD&ĐT ĐẮK LẮK
ĐỀ KIỂM TRA HỌC KÌ I
TRƯỜNG THPT NGÔ GIA TỰ MÔN: Hóa – Lớp 11
Thời gian làm bài: 45 phút; không kể thời gian phát đề
Câu 1 (TH): Tổng hệ số cân bằng của các chất tham gia trong phản ứng sau là:
Mg + HNO3 → Mg(NO3)2 + N2O↑ + H2O A. 24. B. 38. C. 14. D. 10.
Câu 2 (TH): Phương trình điện li nào sau đây viết đúng? A. H 2- 2SO3 → 2H+ + SO3 B. Na2S → 2Na+ + S2- C. H 2- 2- 2CO3 → 2H+ + CO3 D. H2SO4 ⇌ 2H+ + SO4
Câu 3 (NB): Kết luận nào sau đây không đúng?
A. Sự điện li là sự phân li ra ion của các chất khi tan trong nước hoặc ở trạng thái nóng chảy
B. Dung dịch các chất điện li dẫn được điện
C. Chất khi tan trong nước hoặc ở trạng thái nóng chảy phân li thành ion gọi là chất điện li
D. Chất điện li mạnh là chất tan hoàn toàn trong nước
Câu 4 (NB): Axit HNO3 là một axit A. yếu. B. mạnh. C. rất yếu. D. trung bình.
Câu 5 (TH): Đối với dung dịch axit yếu CH3COOH 0,1M, nếu bỏ qua sự điện li của nước thì đánh giá
nào về nồng độ mol ion nào sau đây là đúng?
A. [H+] < [CH3COO-] B. [H+] < 0,1M C. [H+] = 0,1M D. [H+] > [CH3COO-]
Câu 6 (NB): Nước đá khô là khí nào sau đây ở trạng thái rắn: A. CO2 B. SO2 C. CO D. NO2
Câu 7 (NB): Hợp chất nào sau đây là hợp chất hữu cơ? A. CaCO3 B. CO C. CH4 D. CaC2
Câu 8 (NB): Chất nào sau đây khi tan trong nước, các phân tử hòa tan đều phân li thành ion? A. H2CO3 B. CH3COOH C. NaOH D. HF
Câu 9 (TH): Tiến hành các thí nghiệm sau ở điều kiện thường:
(a) Sục khí SO2 vào dung dịch H2S.
(b) Sục khí F2 vào nước.
(c) Cho KMnO4 vào dung dịch HCl đặc.
(d) Sục khí CO2 vào dung dịch NaOH.
(e) Cho Si vào dung dịch NaOH.
(g) Cho Na2SO3 vào dung dịch H2SO4.
(h) C + H2O(hơi) ở nhiệt độ cao. (i) Nung Cu(NO3)2. Trang 1
(k) Dẫn CO qua FeO nung nóng.
Số thí nghiệm có sinh ra đơn chất là A. 6 B. 5 C. 7 D. 8
Câu 10 (TH): Khí CO không khử được chất nào sau đây ở nhiệt độ cao: A. CaO B. CuO C. PbO D. ZnO
Câu 11 (VD): Khử hoàn toàn 14 gam hỗn hợp X gồm CuO và một oxit sắt bằng CO thu được 10,32 gam
hỗn hợp Y gồm 2 kim loại. Thể tích CO (đktc) đã dùng cho quá trình trên là: A. 10,304 lít. B. 1,0304 lít. C. 5,152 lít. D. 51,52 lít.
Câu 12 (TH): Muối được sử dụng làm bột nở cho bánh quy xốp là muối nào sau đây? A. NaHCO3. B. NH4HCO3. C. Na2CO3. D. (NH4)2CO3.
Câu 13 (TH): Cho các chất: nhôm cacbua (Al4C3), axetilen (C2H2), natri cacbonat (Na2CO3), đường
saccarozơ (C12H22O11), PVC ([C2H3Cl]n). Số chất không phải là hợp chất hữu cơ là A. 2 B. 1 C. 4 D. 3
Câu 14 (VD): Đốt cháy hoàn toàn 20 ml hợp chất hữu cơ M bằng vừa đủ 105 ml khí oxi, sản phẩm cháy
thu được gồm 80 ml khí CO2, 90 ml hơi H2O, 10 ml N2. Biết các thể tích đo ở cùng điều kiện nhiệt độ, áp
suất, nhiệt độ. Công thức phân tử của M là (cho nguyên tử khối của các nguyên tố C = 12; H=1; O = 16; N = 14) A. C4H10O2N2 B. C3H7O2N C. C4H7O2N D. C4H9O2N
Câu 15 (TH): Thành phần của dung dịch NH3 gồm: A. NH + 3, NH4 và OH-. B. NH3 và H2O. C. NH + + 4 , OH-, NH3 và H2O. D. NH4 và OH.
Câu 16 (VD): Dung dịch BaCl2 2M có nồng độ mol/l của anion là A. 4M B. 1M C. 2M D. 0,5M
Câu 17 (TH): Ở nhiệt độ thường, nitơ phản ứng được với: A. Li B. Cl2 C. Pb D. F2
Câu 18 (TH): Phát biểu nào dưới đây không đúng:
A. Dung dịch NH3 là 1 bazơ yếu.
B. Đốt cháy NH3 không có xúc tác thu được N2 và H2O.
C. NH3 là chất khí không màu, không mùi, tan nhiều trong nước.
D. Phản ứng tổng hợp NH3 là phản ứng thuận nghịch.
Câu 19 (VD): Hấp thụ hoàn toàn 3,36 lít khí CO2 (điều kiện tiêu chuẩn) vào dung dịch chứa 0,15 mol
NaOH và 0,1 mol Ba(OH)2 thu được m gam kết tủa. Giá trị của m là A. 9,850. B. 19,700. C. 29,550. D. 14,775.
Câu 20 (TH): Cacbon phản ứng với tất cả các chất nào sau đây?
A. Al, HNO3 đặc, KClO3 B. Na2O, NaOH, HCl Trang 2
C. NH4Cl, KOH, AgNO3
D. Ba(OH)2, Na2CO3, CaCO3
Câu 21 (TH): Cặp chất nào sau đây tác dụng với nhau đều tạo ra sản phẩm đều là chất khí? A. CO2 và NaOH B. C và HNO3 đặc C. CO và Fe2O3 D. C và CuO
Câu 22 (VD): Khối lượng NaNO2 cần dùng trong phòng thí nghiệm để thu được 6,72 lít N2 (đktc) là A. 19,2 gam B. 20,1 gam C. 27,0 gam D. 20,7 gam
Câu 23 (VD): Dẫn 2,24 lít khí NH3 (đktc) đi qua ống đựng 32 gam bột CuO nung nóng thu được chất rắn
X và khí Y. Thể tích khí Y sinh ra là: A. 3,36 B. 2,24 C. 1,12 D. 1,344
Câu 24 (VD): Cho từ từ khí CO đi qua ống đựng 3,2 gam CuO nung nóng. Khí thoát ra khỏi ống được
hấp thụ hoàn toàn vào nước vôi trong dư tạo thành 1 gam kết tủa. Chất rắn còn lại trong ống sứ cho vào
cốc đựng 500 ml dung dịch HNO3 0,16M thu được V1 lít khí NO và còn một phần kim loại chưa tan.
Thêm tiếp vào cốc 760 ml dung dịch HCl 2/3 M, sau khi phản ứng xong thu thêm V2 lít khí NO. Biết NO
là sản phẩm khử duy nhất của N+5, các phản ứng xảy ra hoàn toàn. V2 gần nhất với giá trị nào sau đây A. 0,037. B. 0,336. C. 0,112. D. 1,490.
Câu 25 (VDC): Cho m gam hỗn hợp X (gồm Mg, Al, Zn và Cu) tác dụng hết với dung dịch HNO3 thu
được dung dịch Y (không có muối amoni) và 11,2 lít (đktc) hỗn hợp khí Z (gồm N2, NO, N2O và NO2,
trong đó N2 và NO2 có phần trăm thể tích bằng nhau) có tỉ khối đối với heli bằng 8,9. Số mol HNO3 phản ứng là A. 3,0 mol. B. 2,8 mol. C. 3,2 mol. D. 3,4 mol.
Câu 26 (VD): Cho 200 ml dung dịch HNO3 vào 200 ml dung dịch hỗn hợp gồm NaOH 0,2M và KOH
0,3M được 400 ml dung dịch X có pH = a. Cô cạn dung dịch X được 7,66 gam chất rắn khan. Giá trị của a là A. 1 B. 2 C. 12 D. 13
Câu 27 (VD): Hợp chất hữu cơ X có công thức đơn giản nhất CH2O và có tỉ khối so với hiđro là 30.
Công thức phân tử của X là (cho nguyên tử khối của các nguyên tố C = 12; H=1; O = 16) A. CH2O B. C2H4O2 C. C2H4O D. C3H8O
Câu 28 (NB): Hợp chất hữu cơ là hợp chất của nguyên tố A. cacbon B. oxi C. silic D. nitơ
Câu 29 (TH): Chất nào sau đây là chất điện li mạnh? A. HNO2 B. H2CO3 C. CH3COOH D. HCl
Câu 30 (NB): Muối amoni là chất điện li thuộc loại: A. Mạnh. B. Trung bình. C. Tùy gốc axit. D. Yếu.
Câu 31 (TH): Cho từ từ dung dịch (NH4)2SO4 vào dung dịch Ba(OH)2. Hiện tượng xảy ra là:
A. Có khí mùi khai bay lên
B. Không có hiện tượng.
C. Có kết tủa trắng
D. Có khí mùi khai bay lên và có kết tủa trắng. Trang 3
Câu 32 (TH): Chất nào sau đây khi tan trong nước tạo thành dung dịch có khả năng dẫn được điện?
A. đường saccarozơ (C12H22O11) B. muối ăn (NaCl)
C. đường glucozơ (C6H12O6)
D. rượu etylic (C2H5OH) Đáp án 1-C 2-B 3-D 4-B 5-B 6-A 7-C 8-C 9-C 10-A 11-C 12-B 13-A 14-D 15-C 16-A 17-A 18-C 19-B 20-A 21-B 22-D 23-C 24-A 25-C 26-D 27-B 28-A 29-D 30-A 31-D 32-B LỜI GIẢI CHI TIẾT
Câu 1: Đáp án C Phương pháp giải:
Cân bằng phương trình bằng phương pháp thăng bằng eletron. Giải chi tiết:
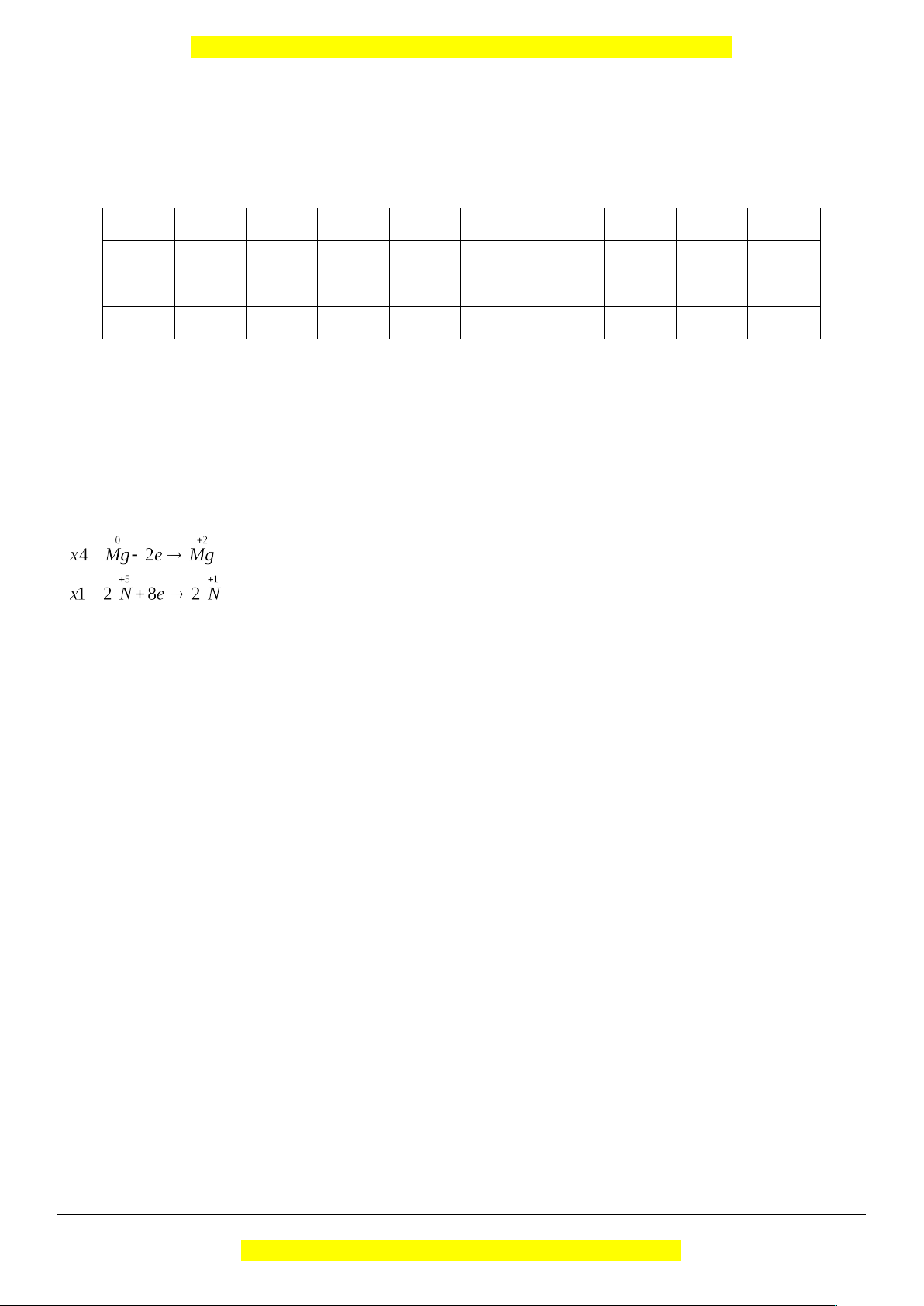
4Mg + 10HNO3 → 4Mg(NO3)2 + N2O↑ + 5H2O
Tổng hệ số các chất tham gia là: 4 + 10 = 14
Câu 2: Đáp án B Phương pháp giải:
Chất điện li mạnh phân li hoàn toàn ta sử dụng mũi tên một chiều
Chất điện li yếu phân li không hoàn toàn ta sử dụng mũi tên hai chiều Giải chi tiết:
A sai vì H2SO3 là chất điện li yếu, phải sử dụng mũi tên hai chiều
B đúng vì Na2S là chất điện li mạnh C sai. H2CO3 ⇄ H2O + CO2
D sai vì H2SO4 là 1 axit mạnh, phải sử dụng mũi tên một chiều
Câu 3: Đáp án D A, B, C đúng
D sai vì chất điện li mạnh là chất khi tan trong nước phân li hoàn toàn thành ion
Câu 4: Đáp án B
Câu 5: Đáp án B Phương pháp giải:
CH3COOH là một chất điện li yếu do đó khi hòa tan vào nước không phân li hoàn toàn thành ion. Trang 4
Đề thi học kì I Hóa lớp 11 trường THPT Ngô Gia Tự - Đăk Lăk
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Bộ 29 Đề thi học kì 1 Hóa học năm 2023 - 2024 chọn lọc từ các trường bản word có lời giải chi tiết:
+ Đề thi học kì 1 Hóa học năm 2023 trường THPT Trần Hưng Đạo - Hà Nội;
+Đề thi học kì 1 Hóa học năm 2023 trường THPT Tenlơman - TP. Hồ Chí Minh;
+Đề thi học kì 1 Hóa học năm 2023 trường THPT Bình Chánh - TP. Hồ Chí Minh;
+Đề thi học kì 1 Hóa học năm 2023 trường THPT Quang Trung;
+Đề thi học kì 1 Hóa học năm 2023 Sở GD_ĐT tỉnh Quảng Nam.
…..……………………
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(742 )Trọng Bình
Giúp ích cho tôi rất nhiều
Duy Trần
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN Hóa Học
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Lớp 11
Xem thêmTài liệu bộ mới nhất