SỞ GD&ĐT HÀ NỘI
ĐỀ KIỂM TRA HỌC KÌ I
TRƯỜNG THPT YÊN HÒA MÔN: Hóa – Lớp 11
Thời gian làm bài: 45 phút; không kể thời gian phát đề
PHẦN I. TRẮC NGHIỆM
Câu 1 (NB): Trong phòng thí nghiệm, nito tinh khiết được điều chế từ: A. không khí. B. NH3 và O2. C. NH4NO2. D. Zn và HNO3.
Câu 2 (TH): Nhiệt phân hoàn toàn Fe(NO3)3 trong không khí thu được các sản phẩm là: A. FeO, NO2, O2. B. Fe2O3, NO2, O2. C. Fe2O3, NO2. D. Fe, NO2, O2.
Câu 3 (TH): Cho 300 ml dung dịch NaOH 1M tác dụng với 200 ml dung dịch H3PO4 1M. Muối thu được sau phản ứng là A. NaH2PO4.
B. NaH2PO4 và Na2HPO4. C. Na2HPO4 và Na3PO4. D. Na3PO4.
Câu 4 (TH): Những ion sau đây cùng có mặt trong một dung dịch là: A. Mg2+, SO 2- 4 , Cl-, Ag+. B. H+, Cl-, Na+, Al3+.
C. S2-, Fe2+, Cu2+, Cl-.
D. OH-, Na+, Ba2+, Fe3+.
Câu 5 (NB): Phân bón hóa học: Đạm, Lân, Kali lần lượt được đánh giá theo chỉ số nào:
A. Hàm lượng % số mol: N, P2O5, K2O.
B. Hàm lượng % khối lượng: N, P, K.
C. Hàm lượng % khối lượng: N, P2O5, K2O. D. Hàm lượng % khối lượng: N2O5, P2O5, K2O.
Câu 6 (NB): Để tạo độ xốp cho một số loại bánh, có thể dùng muối nào sau đây làm bột nở? A. (NH4)2SO4. B. NH4NO2. C. CaCO3. D. NH4HCO3.
Câu 7 (TH): HNO3 chỉ thể hiện tính oxi hóa khi tác dụng với các chất thuộc dãy nào dưới đây?
A. Mg, H2S, C, Fe3O4, Fe(OH)2.
B. Na2SO3, P, CuO, CaCO3, Ag.
C. Al, FeCO3, HI, CaO, FeO.
D. Cu, C, Fe2O3, Fe(OH)2, SO2.
Câu 8 (NB): Thí nghiệm với dung dịch HNO3 thường sinh ra khí độc NO2. Để hạn chế khí NO2 thoát ra
từ ống nghiệm, người ta nút ống nghiệm bằng (a) bông khô (b) bông có tẩm nước
(c) bông có tẩm nước vôi trong (d) bông có tẩm giấm ăn
Trong 4 biện pháp trên, biện pháp có hiệu quả nhất là A. (b). B. (a). C. (d). D. (c).
Câu 9 (NB): Để khắc chữ lên thủy tinh người ta dựa vào phản ứng
A. SiO2 + 2Mg → 2MgO + Si.
B. SiO2 + 2NaOH → Na2SiO3 + H2O.
C. SiO2 + 4HF → SiF4 + 2H2O.
D. SiO2 + Na2CO3 → Na2SiO3 + CO2.
Câu 10 (VD): Một loại thủy tinh có thành phần gồm 70,559% SiO2, 10,98% CaO, 18,43% K2O. Công
thức của thủy tinh này là
A. K2O.2CaO.6SiO2. B. K2O.CaO.5SiO2. C. K2O.CaO.4SiO2. D. K2O.CaO.6SiO2. Trang 1
Câu 11 (NB): Phản ứng nào chứng tỏ axit silixic yếu hơn axit cacbonic
A. Na2SiO3 + CO2 + H2O → Na2CO3 + H2SiO3.
B. Na2SiO3 + 2HCl → 2NaCl + H2SiO3.
C. H2SiO3 + 2NaOH → Na2SiO3 + 2H2O.
D. SiO2 + 2NaOH → Na2SiO3 + H2O.
Câu 12 (VD): Hấp thụ toàn bộ 0,896 lít CO2 vào 3 lít dung dịch Ca(OH)2 0,01M thu được? A. 1 gam kết tủa. B. 2 gam kết tủa. C. 3 gam kết tủa. D. 4 gam kết tủa. II. PHẦN TỰ LUẬN
Câu 13 (TH): Hoàn thành sơ đồ phản ứng sau (ghi rõ điều kiện, xúc tác nếu có):
Câu 14 (TH): Nêu hiện tượng xảy ra, viết phương trình phản ứng khi:
a. Thổi từ từ đến dư khí CO2 vào dung dịch nước vôi trong.
b. Cho dung dịch HCl vào dung dịch Na2SiO3.
c. Cho dung dịch Ba(HCO3)2 vào dung dịch NaHSO4.
Câu 15 (VD): Hòa tan hoàn toàn 25,6 gam hỗn hợp A gồm Cu và Fe2O3 vào dung dịch HNO3 2M (dư
20% so với lượng cần phản ứng) thu được dung dịch B và 2,24 lít NO (đktc) là sản phẩm khử duy nhất.
a. Viết phương trình phản ứng hóa học xảy ra.
b. Tính phần trăm khối lượng Fe2O3 trong hỗn hợp A?
c. Tính thể tích dung dịch HNO3 ban đầu?
d. Lấy dung dịch B đem cô cạn rồi nung tới khối lượng không đổi thì thu được m gam chất rắn. Tính giá trị của m? Đáp án 1-C 2-B 3-B 4-B 5-C 6-D 7-A 8-D 9-C 10-D 11-A 12-B 13- 14- 15- 16- 17- 18- 19- 20- LỜI GIẢI CHI TIẾT
Câu 1: Đáp án C Phương pháp giải:
Dựa vào phương pháp điều chế N2 trong phòng thí nghiệm. Giải chi tiết:
Trong phòng thí nghiệm, người ta thường điều chế N2 bằng phương pháp đun nóng dung dịch NH4NO2 bão hòa: Trang 2
NH4NO2 N2 + 2H2O
Câu 2: Đáp án Phương pháp giải:
Nhiệt phân các muối nitrat kim loại M(NO3)n:
Muối nitrat của các kim loại hoạt động mạnh [K, …, Ca] bị nhiệt phân thu được muối nitrit và O2.
Muối nitrat của các kim loại [Mg, …, Cu] bị nhiệt phân thu được oxit bazo, NO2 và O2.
Muối nitrat của các kim loại [Hg, Ag, …] bị nhiệt phân thu được kim loại, NO2 và O2. Giải chi tiết: 4Fe(NO3)3 2Fe2O3 + 12NO2 + 3O2
Vậy nhiệt phân muối Fe(NO3)3 thu được Fe2O3, NO2 và 3O2
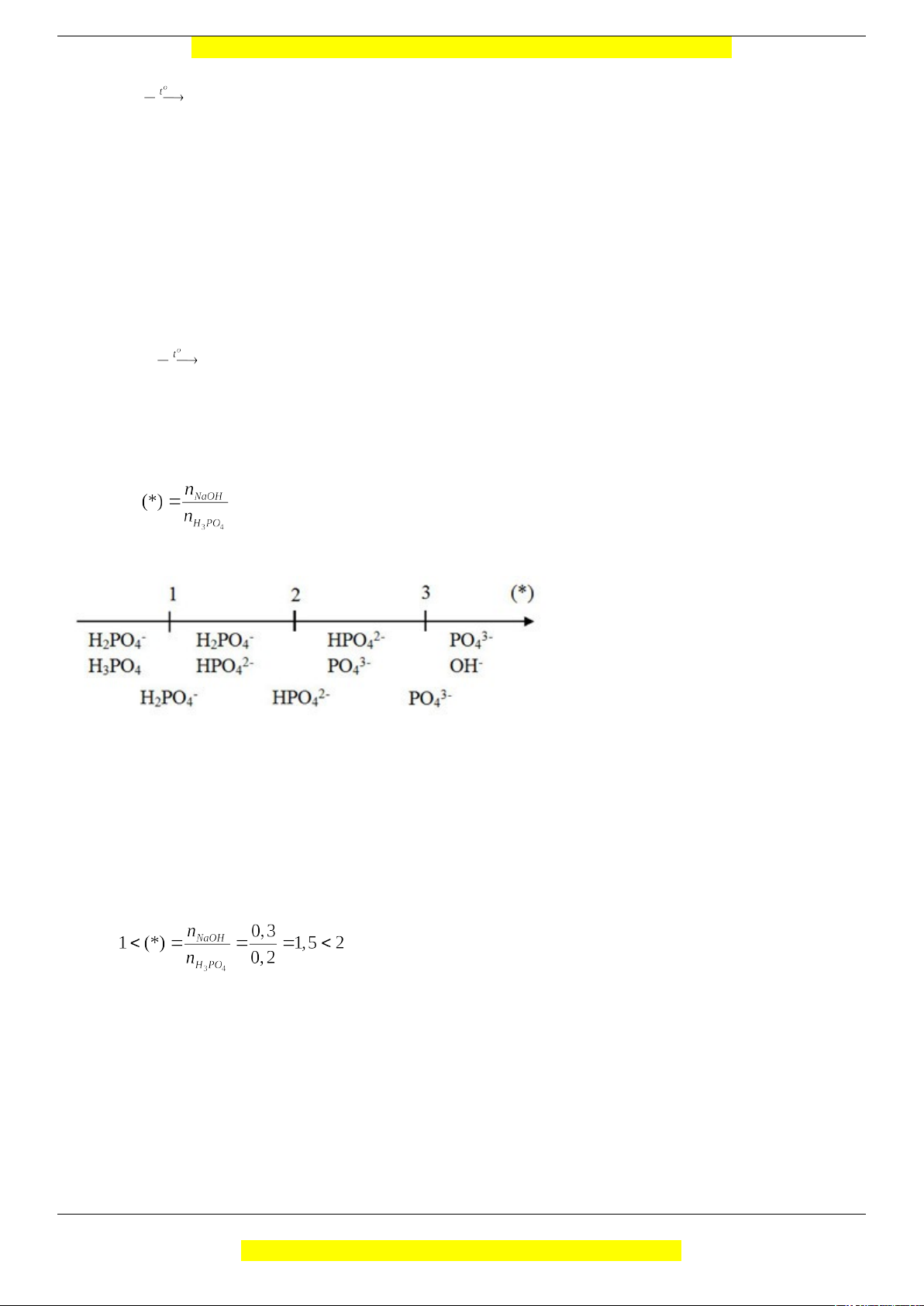
Câu 3: Đáp án Phương pháp giải: Tính tỉ lệ Qua sơ đồ ta thấy: (*) ≤ 1 => tạo muối H - 2PO4
1 < (*) < 2 => tạo muối H - 2- 2PO4 và HPO4
(*) = 2 => tạo muối HPO 2- 4
2 < (*) < (3) => tạo muối HPO 2- 3- 4 và PO4
(*) ≤ 3 => tạo muối PO 3- 4 Giải chi tiết: Ta có:
=> tạo muối NaH2PO4 và Na2HPO4
Câu 4: Đáp án Phương pháp giải:
- Những chất không phản ứng với nhau có thể tồn tại trong cùng một dung dịch.
- Các ion phản ứng với nhau khi tạo thành kết tủa/chất khí/chất điện li yếu. Giải chi tiết: A loại vì Ag+ + SO 2- 4 → Ag2SO4 ↓ B đúng Trang 3
C loại vì Fe2+ + S2- → FeS↓
D loại vì Fe3+ + 3OH- → Fe(OH)3↓
Câu 5: Đáp án Phương pháp giải:
Đánh giá độ dinh dưỡng của phân đạm người ta dựa vào % khối lượng của N, phân lân dựa vào % khối
lượng của P2O5, phân kali dựa vào 5 khối lượng của K2O. Giải chi tiết:
Phân bón hóa học: Đạm, Lân, Kali lần lượt được đánh giá theo chỉ số hàm lượng % khối lượng N, P2O5, K2O.
Câu 6: Đáp án Phương pháp giải: Giải chi tiết:
Để tạo độ xốp cho một số loại bánh, người ta thường dùng bột nở có thành phần hóa học chính là NH4HCO3. NH4HCO3 NH3 + CO2 + H2O
Câu 7: Đáp án Phương pháp giải:
HNO3 thể hiện tính oxi hóa khi phản ứng với các chất khử (chất có khả năng tăng số oxi hóa) Giải chi tiết: A đúng B loại CuO, CaCO3 C loại CaO D loại Fe2O3
Câu 8: Đáp án Phương pháp giải:
Để ngăn khí độc ta dùng hóa chất phản ứng với khí đó tạo thành chất không độc. Giải chi tiết:
Trong 4 biện pháp trên, biện pháp có hiệu quả nhất là dùng bông có tẩm nước vôi trong để nút vào ống nghiệm.
2Ca(OH)2 + 4NO2 → Ca(NO3)2 + Ca(NO2)2 + 2H2O
Câu 9: Đáp án Phương pháp giải:
HF có khả năng hòa tan SiO2 (thành phần chính của thủy tinh). Giải chi tiết: Trang 4
Đề thi học kì I Hóa lớp 11 trường THPT Yên Hòa - Hà Nội
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Bộ 29 Đề thi học kì 1 Hóa học năm 2023 - 2024 chọn lọc từ các trường bản word có lời giải chi tiết:
+ Đề thi học kì 1 Hóa học năm 2023 trường THPT Trần Hưng Đạo - Hà Nội;
+Đề thi học kì 1 Hóa học năm 2023 trường THPT Tenlơman - TP. Hồ Chí Minh;
+Đề thi học kì 1 Hóa học năm 2023 trường THPT Bình Chánh - TP. Hồ Chí Minh;
+Đề thi học kì 1 Hóa học năm 2023 trường THPT Quang Trung;
+Đề thi học kì 1 Hóa học năm 2023 Sở GD_ĐT tỉnh Quảng Nam.
…..……………………
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(830 )Trọng Bình
Giúp ích cho tôi rất nhiều
Duy Trần
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN Hóa Học
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Lớp 11
Xem thêmTài liệu bộ mới nhất