ĐỀ THI THỬ THPT QUỐC GIA NĂM 2023
Môn thi: HÓA HỌC– ĐỀ SỐ 04
Thời gian làm bài: 50 phút, không kể thời gian phát đề
Họ, tên thí sinh:.......................................................................
Số báo danh:............................................................................
Cho biết nguyên tử khối của các nguyên tố: H = 1; He = 4; C = 12; N = 14; O = 16; Na = 23; Mg = 24;
Al = 27; Si = 28; S = 32; Cl = 35,5; K = 39; Ca = 40; Fe = 56; Cu = 64; Ag = 108; Ba = 137.
Câu 1: Kim loại dẫn điện tốt nhất là A. Ag. B. Cu. C. Au. D. Fe.
Câu 2: Số nhóm –OH trong mỗi mắc xích của xenlulozơ là A. 2. B. 3. C. 4. D. 5.
Câu 3: Thành phần chính của quặng manhetit là A. Fe2O3. B. Fe3O4. C. FeS2. D. FeCO3
Câu 4: Công thức chung của este đơn chức, mạch hở, có một liên kết π trong phần tử là A. CnH2nO2 (n ≥ 3).
B. Cn H2n-2O2 (n ≥ 3). C. CnH2n-2O2 (n ≥ 4). D. CnH2nO2 (n ≥ 2).
Câu 5: Hóa chất nào sau đây được dùng để làm mềm nước có tính chất cứng vĩnh cửu? A. CaCl2. B. KNO3. C. Na3PO4 D. MgSO4.
Câu 6: Sự gia tăng nồng độ khí nào sau đây là nguyên nhân chính gây nên hiệu ứng nhà kính, làm cho
nhiệt độ của trái đất tăng lên? A. CO2. B. SO2. C. CO. D. N2.
Câu 7: Chất nào sau đây tác dụng hoàn toàn với dung dịch KOH loãng, dư, thu được kết tủa trắng? A. FeCl3. B. Zn(NO3)2. C. (NH4)2SO4. D. MgCl2.
Câu 8: Este nào sau đây có khả năng tham gia phản ứng tráng bạc? A. CH3COOC2H5. B. HCOOC6H5. C. C2H3COOC2H5. D. C6H5COOCH3.
Câu 9: Dung dịch nào sau đây hòa tan được Cu(OH)2 ở điều kiện thường? A. Propan-1,3-điol. B. Saccarozơ. C. Ancol etylic. D. Triolein.
Câu 10: Cho 4,2 gam Si tác dụng vừa đủ với dung dịch NaOH, thu được V lít H2 (đktc). Giá trị V là A. 3,36. B. 5,04. C. 6,72. D. 13,44.
Câu 11: Benzanđehit có công thức cấu tạo là A. COOH. B. CH2 CHO. Trang 1
C. CHO. D. CH2 COOH.
Câu 12: Trùng hợp monome nào sau đây thu được polime dùng để sản xuất thủy tinh hữu cơ? A. Vinyl clorua. B. Metyl metacrylat. C. Acrilonitrin. D. Buta-1,3-đien.
Câu 13: Cho 1 mol chất X phản ứng với dung dịch KOH (dư, đun nóng) thí số mol KOH phản ứng tối đa
là 2 mol. Chất X có thể là A. Gly-Ala-Val. B. lysin. C. axit glutamic. D. metylamoni clorua.
Câu 14: Ứng với ông thức phân tử C3H8O có bao nhiêu chất hữu cơ là đồng phân cấu tạo của nhau? A. 1. B. 2. C. 3. D. 4.
Câu 15: Đốt cháy hoàn toàn 11,52 gam este đơn chức X, thu được 10,752 lít CO2 (đktc) và 5,76 gam
H2O. Công thức phân tử của X là A. C3H4O2. B. C2H4O2. C. C3H6O2. D. C4H6O2.
Câu 16: Khí amoniac không có tính chất nào sau đây?
A. Có mùi khai và xốc.
B. Ít tan trong nước.
C. Nhẹ hơn không khí.
D. Làm xanh giấy quì tím ẩm.
Câu 17: Đốt cháy hoàn toàn chất X, thu được số mol H2O lớn hơn số mol CO2. Chất X không thể là A. amino axit. B. ancol. C. amin. D. anđehit.
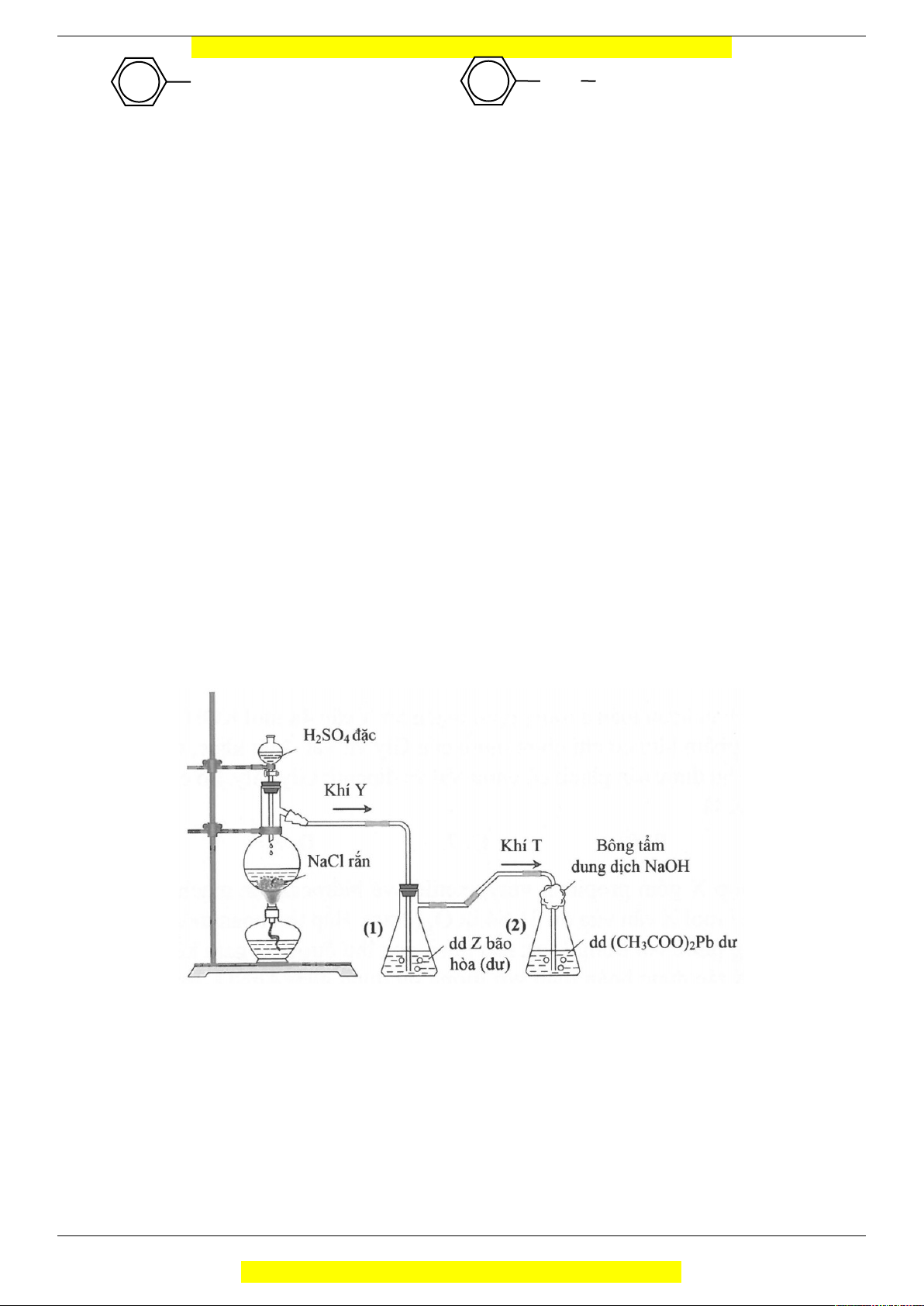
Câu 18: Tiến hành thí nghiệm như hình vẽ sau:
Sau khi các phản ứng xảy ra hoàn toàn, bình tam giác (2) xuất hiện kết tủa màu đen. Các chất Y, Z, T lần lượt là A. Cl2, KHS, H2S. B. SO2, KHS, H2S. C. HCl, KHS, H2S. D. HCl, KHSO3, SO2.
Câu 19: Cho m gam glucozơ tác dụng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3 đun nóng,
thu được 5,4 gam Ag. Giá trị của m là A. 4,5. B. 9,0. C. 13,5. D. 18,0. Trang 2
Câu 20: Cho phản ứng hóa học sau: KOH + HNO3 KNO3 + H2O.
Phản ứng hóa học nào sau đây có cùng phương trình ion thu gọn với phản ứng trên?
A. Ba(OH)2 + H2SO4 BaSO4 + 2H2O.
B. 2KHCO3 + H2SO4 K2SO4 + 2CO2 + 2H2O.
C. 3KOH + Fe(NO3)3 3KNO3 + Fe(OH)3.
D. NaOH +HCl NaCl +H2O.
Câu 21: Cho dãy các chất: toluene, etylamin, tristearin, phenol, alanine, etilen. Có bao nhiêu chất trong
dãy là chất lỏng ở điều kiện thường? A. 1. B. 2. C. 3. D. 4.
Câu 22: Tiến hành phản ứng nhiệt nhôm hỗn hợp X gồm 0,09 mol Al và 0,12 mol CuO trong khí trơ. Sau
một thời gian, thu được m gam hỗn hợp rắn Y. Giá trị của m là A. 10,44. B. 12,03. C. 11,76. D. 11,07.
Câu 23: Cho phản ứng: NaCrO2 + Br2 + NaOH Na2CrO4 + NaBr + H2O
Trong phương trình của phản ứng trên, khi hệ số của NaCrO2 là 2 thì hệ số của NaOH là A. 4. B. 6. C. 8. D. 10.
Câu 24: Cho peptit mạch hở X được tạo từ các amimo axit no, mạch hở, có không quá hai nhóm chức.
Đốt cháy hoàn toàn 10,29 gam X, thu được 1,68 lít N2 (đktc) và 24,03 gam hỗn hợp CO2 và H2O. Số liên
kết peptit trong phân tử X là A. 7. B. 8. C. 9. D. 10.
Câu 25: Thủy phân hoàn toàn a mol peptit mạch hở X cần 4a mol KOH trong dung dịch, thu được sản
phẩm hữu cơ chỉ chứa muối cua Gly và Val. Mặt khác, thủy phân không hoàn toàn X, thu được sản phẩm
có chưa Val và đipeptit Gly-Gly. Số công thức cấu tạo phù hợp của X là A. 5. B. 6. C. 7. D. 8.
Câu 26: Hỗn hợp X gồm propilen, vinylaxetilen và hiđrocacbon mạch hở Y. Đốt cháy hoàn toàn 0,27
mol X cần vừa đủ 21,84 lít O2 (đktc). Hấp thụ hoàn toàn sản phẩm cháy vào bình đựng nước vôi trong
(dư), sau phản ứng thu được 75 gam kết tủa. Mặt khác, cho 33 gam X tác dụng hoàn toàn với lượng dư
dung dịch AgNO3 trong NH3, số mol AgNO3 phản ứng là A. 0,6 mol. B. 0,8 mol. C. 1,0 mol. D. 1,2 mol.
Câu 27: Tiến hành các phản ứng theo sơ đồ sau (đúng với tỉ lệ mol các chất) X1 + CO2 +H2O 2X2
2X2 + X3 CaCO3 ↓ + X1 + 2H2O.
Hai chất X1 và X3 lần lượt là A. BaCO3 và Ca(OH)2. B. KHCO3 và Ca(OH)2. C. K2CO3 và Ca(HCO3)2. D. Na2CO3 và Ca(OH)2.
Câu 28: Thực hiện các thí nghiệm sau:
(a) Cho Cu vào dung dịch H2SO4 đặc, nóng. Trang 3
(b) Nung nóng hỗn hợp tecmit.
(c) Cho Fe2O3 vào dung dịch HNO3.
(d) Nhúng thanh kẽm vào dung dịch Fe2(SO4)3.
(e) Cho hơi nước đi qua than nóng đỏ.
Số thí nghiệm xảy ra sự oxi hóa kim loại là A. 1. B. 2. C. 3. D. 4.
Câu 29: Đốt cháy một lượng Fe dư trong V lít (đktc) hỗn hợp khí X gồm O2 và Cl2, có tỉ khối so với He
là 11,25, thu được 44,2 gam hỗn hợp rắn Y. Hòa tan hoàn toàn Y trong 550ml dung dịch HCl 2M (vừa
đủ), thu được dung dịch Z. Cho Z phản ứng hoàn toàn với dung dịch AgNO3 dư, thu được 209,57 gam kết tủa. Giá trị của V là A. 8,064. B. 10,752. C. 5,376. D. 16,128.
Câu 30: Hỗn hợp X gồm ankan Y và hai amin no, đơn chức, mạch hở, kế tiếp nhau trong dãy đồng đẳng.
Đốt cháy hoàn toàn 3,95 gam X cần vừa đủ 8,12 lít O2 (đktc), thu được 0,57 mol hỗn hợp khí và hơi gồm
N2, H2O và CO2. Công thức phân tử của Y là A. CH4. B. C2H6. C. C3H8. D. C4H10.
Câu 31: Tiến hành điện phân dung dịch X chưa a mol CuSO4 và b mol NaCl bằng dòng điện một chiều
(điện cực trơ, có màng ngăn). Sau thời gian t giây thì ngừng điện phân, thu được ba khí thoát ra ở hai cực
điện với thể tích bằng nhau (các thể tích khí đo ở điều kiện nhiệt độ và áp suất). Biết hiệu suất điện phân
là 100%, các khí sinh ra không tan trong dung dịch. Tỉ lệ a : b là A. 1: 2. B. 2 : 3. C. 1 : 1. D. 2 : 1.
Câu 32: Cho hai axit cacboxylic mạch hở X và Y (MX < MY). Đốt cháy hoàn toàn X hoặc Y bằng một
lượng oxi vừa đủ, đều thu được số mol H2O gấp đôi số mol O2 đã phản ứng. cho 31,8 gam hỗn hợp Z gồm
X và Y tác dụng với 800ml dung dịch NaOH 1M (dư). Cô cạn dung dịch sau phản ứng, thu được 51,2
gam rắn. Phần trăm khối lượng X trong Z là A. 43,40%. B. 28,93%. C. 84,91%. D. 56,60%.
Câu 33: Kết quả thí nghiệm của các dung dịch X, Y, Z, T với thuốc thử được ghi lại trong bảng sau Mẫu thử Thuốc thử Hiện tượng X Nước Br2 Kết tủa trắng Y
Dung dịch AgNO3 trong NH3 đun nóng Kết tủa Ag trắng sáng Z Quỳ tím Chuyển màu hồng T Cu(OH)2 Có màu tím
Các dung dịch X, Y, Z, T lần lượt là
A. Fructozơ, anilin, axit axetic, anbumin.
B. Anilin, fructozơ, anbumin, axit axetic. Trang 4
C. Anilin, anbumin, axit axetic, fructozơ.
D. Anilin, fructozơ, axit axetic, anbumin.
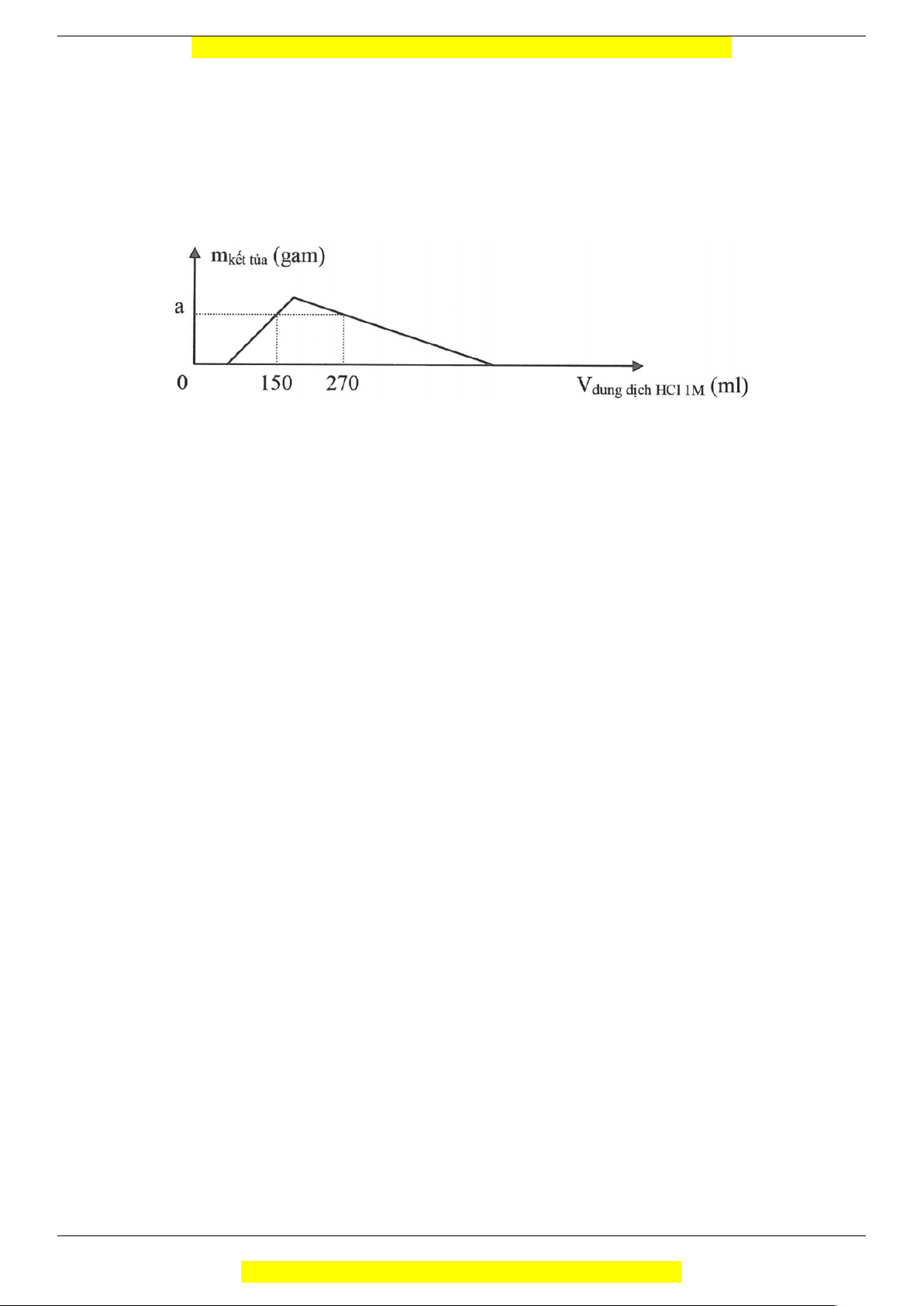
Câu 34: Nhiệt phân hoàn toàn 27,09 gam hỗn hợp BaCO3 và Al(OH)3 đến khối lượng không đổi, thu
được hỗn hợp X,. Hòa tan hoàn toàn X vào lượng nước dư, thu được dung dịch Y trong suốt. Cho từ từ
dung dịch HCl 1M vào dung dịch Y, phản ứng được biểu diễn theo đồ thị sau: Giá trị của a là A. 7,02. B. 7,80. C. 6,24. D. 9,36.
Câu 35: Hỗn hợp X gồm hai chất có công thức phân tử là C3H7NO4 và C3H7NO2. Cho 56,52 gam X tác
dụng vừa đủ với dung dịch NaOH 32% (đun nóng), cô cạn dung dịch sau phản ứng, thu được hỗn hợp Y
gồm hai muối đều có phân tử khối nhỏ hơn 100 và 89,32 gam hỗn hợp Z gồm hơi nước và chất hữu cơ T.
Biết tỉ khối củ T so với H2 là 16. Phần trăm khối lượng của muối có phân tử khối nhỏ hơn trong Y là A. 52,87%. B. 30,14%. C. 53,25%. D. 31,39%.
Câu 36: Cho các phát biểu sau:
(a) Kim loài kiềm được điều chế bằng phương pháp điện phân dung dịch muối halogenua tương ứng.
(b) Sắt có trong hemoglobin (huyết cầu tố) của máu.
(c) Độ dinh dưỡng của phân kali được đánh giá theo phần trăm khối lượng nguyên tố kali.
(d) Dung dịch axit nitric đặc, không màu để ngoài ánh sáng lâu ngày sẽ chuyển thành màu vàng.
(e) Tất cả các ion kim loại đều không có tính khử.
Số phát biểu sai là A. 1. B. 2. C. 3. D. 4.
Câu 37: Hòa tan hoàn toàn m gam hỗn hợp X gồm Fe, Fe3O4, FeS (trong đó nguyên tố oxi chiếm 12,5%
về khối lượng) trong dung dịch chứa a mol KNO3 và 0,43 mol H2SO4 (loãng), sau phản ứng thu được khi
NO (sản phẩm khử duy nhất của N+5 và dung dịch Y. Cho Y phản ứng vừa đủ với 740ml dung dịch KOH
1M, thu được 21,4 gam kết tủa và dung dịch Z chứa 101,14 gam hỗn hợp muối. Giá trị của a là A. 0,38. B. 0,40. C. 0,42. D. 0,44.
Câu 38: Cho X và Y (MX < MY) là hai axit cacboxylic đơn chức, mạch hở; T là este mạch hở tạo từ X, Y
và ancol Z. Đốt cháy hoàn toàn 32,65 gam hỗn hợp E gồm X, Y, T cần vừa đủ 31,64 lít O2 (đktc). Mặt
khác, cho 32,65 gam E tác dụng vừa đủ với 450ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng,
thu được 39,3 gam muối và m gam ancol Z. Dẫn m gam Z vào bình đựng kali dư, sau phản ứng thấy có
khí thoát ra và khối lượng bình tăng 7,5 gam. Phần trăm khối lượng của X trong E là Trang 5
Đề thi THPT Quốc Gia Hóa năm 2023 Bookgol - Đề 4
600
300 lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Đề thi được cập nhật liên tục trong gói này từ nay đến hết tháng 6/2023. Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Bộ 20 đề luyện thi TN THPT Quốc gia môn Hóa năm 2022-2023 có lời giải chi tiết được chọn lọc và biên soạn công phu bám sát đề thi minh họa của Bộ GD&ĐT.
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(600 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN Hóa Học
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Lớp 12
Xem thêmTài liệu bộ mới nhất

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
ĐỀ THI THỬ THPT QUỐC GIA NĂM 2023
Môn thi: HÓA HỌC– ĐỀ SỐ 04
Thời gian làm bài: 50 phút, không kể thời gian phát đề
Họ, tên thí sinh:.......................................................................
Số báo danh:............................................................................
Cho biết nguyên tử khối của các nguyên tố: H = 1; He = 4; C = 12; N = 14; O = 16; Na = 23; Mg = 24;
Al = 27; Si = 28; S = 32; Cl = 35,5; K = 39; Ca = 40; Fe = 56; Cu = 64; Ag = 108; Ba = 137.
Câu 1: Kim loại dẫn điện tốt nhất là
A. Ag. B. Cu. C. Au. D. Fe.
Câu 2: Số nhóm –OH trong mỗi mắc xích của xenlulozơ là
A. 2. B. 3. C. 4. D. 5.
Câu 3: Thành phần chính của quặng manhetit là
A. Fe
2
O
3
. B. Fe
3
O
4
. C. FeS
2
. D. FeCO
3
Câu 4: Công thức chung của este đơn chức, mạch hở, có một liên kết π trong phần tử là
A. C
n
H
2n
O
2
(n ≥ 3). B. C
n
H
2n-2
O
2
(n ≥ 3).
C. C
n
H
2n-2
O
2
(n ≥ 4). D. C
n
H
2n
O
2
(n ≥ 2).
Câu 5: Hóa chất nào sau đây được dùng để làm mềm nước có tính chất cứng vĩnh cửu?
A. CaCl
2
. B. KNO
3
. C. Na
3
PO
4
D. MgSO
4
.
Câu 6: Sự gia tăng nồng độ khí nào sau đây là nguyên nhân chính gây nên hiệu ứng nhà kính, làm cho
nhiệt độ của trái đất tăng lên?
A. CO
2
. B. SO
2
. C. CO. D. N
2
.
Câu 7: Chất nào sau đây tác dụng hoàn toàn với dung dịch KOH loãng, dư, thu được kết tủa trắng?
A. FeCl
3
. B. Zn(NO
3
)
2
. C. (NH
4
)
2
SO
4
. D. MgCl
2
.
Câu 8: Este nào sau đây có khả năng tham gia phản ứng tráng bạc?
A. CH
3
COOC
2
H
5
. B. HCOOC
6
H
5
.
C. C
2
H
3
COOC
2
H
5
. D. C
6
H
5
COOCH
3
.
Câu 9: Dung dịch nào sau đây hòa tan được Cu(OH)
2
ở điều kiện thường?
A. Propan-1,3-điol. B. Saccarozơ.
C. Ancol etylic. D. Triolein.
Câu 10: Cho 4,2 gam Si tác dụng vừa đủ với dung dịch NaOH, thu được V lít H
2
(đktc).
Giá trị V là
A. 3,36. B. 5,04. C. 6,72. D. 13,44.
Câu 11: Benzanđehit có công thức cấu tạo là
A. B.
Trang 1
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
COOH.
CH
2
CHO.
Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
C. D.
Câu 12: Trùng hợp monome nào sau đây thu được polime dùng để sản xuất thủy tinh hữu cơ?
A. Vinyl clorua. B. Metyl metacrylat.
C. Acrilonitrin. D. Buta-1,3-đien.
Câu 13: Cho 1 mol chất X phản ứng với dung dịch KOH (dư, đun nóng) thí số mol KOH phản ứng tối đa
là 2 mol. Chất X có thể là
A. Gly-Ala-Val. B. lysin.
C. axit glutamic. D. metylamoni clorua.
Câu 14: Ứng với ông thức phân tử C
3
H
8
O có bao nhiêu chất hữu cơ là đồng phân cấu tạo của nhau?
A. 1. B. 2. C. 3. D. 4.
Câu 15: Đốt cháy hoàn toàn 11,52 gam este đơn chức X, thu được 10,752 lít CO
2
(đktc) và 5,76 gam
H
2
O. Công thức phân tử của X là
A. C
3
H
4
O
2
. B. C
2
H
4
O
2
. C. C
3
H
6
O
2
. D. C
4
H
6
O
2
.
Câu 16: Khí amoniac không có tính chất nào sau đây?
A. Có mùi khai và xốc. B. Ít tan trong nước.
C. Nhẹ hơn không khí. D. Làm xanh giấy quì tím ẩm.
Câu 17: Đốt cháy hoàn toàn chất X, thu được số mol H
2
O lớn hơn số mol CO
2
. Chất X không thể là
A. amino axit. B. ancol. C. amin. D. anđehit.
Câu 18: Tiến hành thí nghiệm như hình vẽ sau:
Sau khi các phản ứng xảy ra hoàn toàn, bình tam giác (2) xuất hiện kết tủa màu đen. Các chất Y, Z, T lần
lượt là
A. Cl
2
, KHS, H
2
S. B. SO
2
, KHS, H
2
S.
C. HCl, KHS, H
2
S. D. HCl, KHSO
3
, SO
2
.
Câu 19: Cho m gam glucozơ tác dụng hoàn toàn với lượng dư dung dịch AgNO
3
trong NH
3
đun nóng,
thu được 5,4 gam Ag. Giá trị của m là
A. 4,5. B. 9,0. C. 13,5. D. 18,0.
Trang 2
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
CHO.
CH
2
COOH.

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Câu 20: Cho phản ứng hóa học sau: KOH + HNO
3
KNO
3
+ H
2
O.
Phản ứng hóa học nào sau đây có cùng phương trình ion thu gọn với phản ứng trên?
A. Ba(OH)
2
+ H
2
SO
4
BaSO
4
+ 2H
2
O.
B. 2KHCO
3
+ H
2
SO
4
K
2
SO
4
+ 2CO
2
+ 2H
2
O.
C. 3KOH + Fe(NO
3
)
3
3KNO
3
+ Fe(OH)
3
.
D. NaOH +HCl NaCl +H
2
O.
Câu 21: Cho dãy các chất: toluene, etylamin, tristearin, phenol, alanine, etilen. Có bao nhiêu chất trong
dãy là chất lỏng ở điều kiện thường?
A. 1. B. 2. C. 3. D. 4.
Câu 22: Tiến hành phản ứng nhiệt nhôm hỗn hợp X gồm 0,09 mol Al và 0,12 mol CuO trong khí trơ. Sau
một thời gian, thu được m gam hỗn hợp rắn Y. Giá trị của m là
A. 10,44. B. 12,03. C. 11,76. D. 11,07.
Câu 23: Cho phản ứng: NaCrO
2
+ Br
2
+ NaOH Na
2
CrO
4
+ NaBr + H
2
O
Trong phương trình của phản ứng trên, khi hệ số của NaCrO
2
là 2 thì hệ số của NaOH là
A. 4. B. 6. C. 8. D. 10.
Câu 24: Cho peptit mạch hở X được tạo từ các amimo axit no, mạch hở, có không quá hai nhóm chức.
Đốt cháy hoàn toàn 10,29 gam X, thu được 1,68 lít N
2
(đktc) và 24,03 gam hỗn hợp CO
2
và H
2
O. Số liên
kết peptit trong phân tử X là
A. 7. B. 8. C. 9. D. 10.
Câu 25: Thủy phân hoàn toàn a mol peptit mạch hở X cần 4a mol KOH trong dung dịch, thu được sản
phẩm hữu cơ chỉ chứa muối cua Gly và Val. Mặt khác, thủy phân không hoàn toàn X, thu được sản phẩm
có chưa Val và đipeptit Gly-Gly. Số công thức cấu tạo phù hợp của X là
A. 5. B. 6. C. 7. D. 8.
Câu 26: Hỗn hợp X gồm propilen, vinylaxetilen và hiđrocacbon mạch hở Y. Đốt cháy hoàn toàn 0,27
mol X cần vừa đủ 21,84 lít O
2
(đktc). Hấp thụ hoàn toàn sản phẩm cháy vào bình đựng nước vôi trong
(dư), sau phản ứng thu được 75 gam kết tủa. Mặt khác, cho 33 gam X tác dụng hoàn toàn với lượng dư
dung dịch AgNO
3
trong NH
3
, số mol AgNO
3
phản ứng là
A. 0,6 mol. B. 0,8 mol. C. 1,0 mol. D. 1,2 mol.
Câu 27: Tiến hành các phản ứng theo sơ đồ sau (đúng với tỉ lệ mol các chất)
X
1
+ CO
2
+H
2
O 2X
2
2X
2
+ X
3
CaCO
3
↓ + X
1
+ 2H
2
O.
Hai chất X
1
và X
3
lần lượt là
A. BaCO
3
và Ca(OH)
2
. B. KHCO
3
và Ca(OH)
2
.
C. K
2
CO
3
và Ca(HCO
3
)
2
. D. Na
2
CO
3
và Ca(OH)
2
.
Câu 28: Thực hiện các thí nghiệm sau:
(a) Cho Cu vào dung dịch H
2
SO
4
đặc, nóng.
Trang 3
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
(b) Nung nóng hỗn hợp tecmit.
(c) Cho Fe
2
O
3
vào dung dịch HNO
3
.
(d) Nhúng thanh kẽm vào dung dịch Fe
2
(SO
4
)
3
.
(e) Cho hơi nước đi qua than nóng đỏ.
Số thí nghiệm xảy ra sự oxi hóa kim loại là
A. 1. B. 2. C. 3. D. 4.
Câu 29: Đốt cháy một lượng Fe dư trong V lít (đktc) hỗn hợp khí X gồm O
2
và Cl
2
, có tỉ khối so với He
là 11,25, thu được 44,2 gam hỗn hợp rắn Y. Hòa tan hoàn toàn Y trong 550ml dung dịch HCl 2M (vừa
đủ), thu được dung dịch Z. Cho Z phản ứng hoàn toàn với dung dịch AgNO
3
dư, thu được 209,57 gam kết
tủa. Giá trị của V là
A. 8,064. B. 10,752. C. 5,376. D. 16,128.
Câu 30: Hỗn hợp X gồm ankan Y và hai amin no, đơn chức, mạch hở, kế tiếp nhau trong dãy đồng đẳng.
Đốt cháy hoàn toàn 3,95 gam X cần vừa đủ 8,12 lít O
2
(đktc), thu được 0,57 mol hỗn hợp khí và hơi gồm
N
2
, H
2
O và CO
2
. Công thức phân tử của Y là
A. CH
4
. B. C
2
H
6
. C. C
3
H
8
. D. C
4
H
10
.
Câu 31: Tiến hành điện phân dung dịch X chưa a mol CuSO
4
và b mol NaCl bằng dòng điện một chiều
(điện cực trơ, có màng ngăn). Sau thời gian t giây thì ngừng điện phân, thu được ba khí thoát ra ở hai cực
điện với thể tích bằng nhau (các thể tích khí đo ở điều kiện nhiệt độ và áp suất). Biết hiệu suất điện phân
là 100%, các khí sinh ra không tan trong dung dịch. Tỉ lệ a : b là
A. 1: 2. B. 2 : 3. C. 1 : 1. D. 2 : 1.
Câu 32: Cho hai axit cacboxylic mạch hở X và Y (M
X
< M
Y
). Đốt cháy hoàn toàn X hoặc Y bằng một
lượng oxi vừa đủ, đều thu được số mol H
2
O gấp đôi số mol O
2
đã phản ứng. cho 31,8 gam hỗn hợp Z gồm
X và Y tác dụng với 800ml dung dịch NaOH 1M (dư). Cô cạn dung dịch sau phản ứng, thu được 51,2
gam rắn. Phần trăm khối lượng X trong Z là
A. 43,40%. B. 28,93%. C. 84,91%. D. 56,60%.
Câu 33: Kết quả thí nghiệm của các dung dịch X, Y, Z, T với thuốc thử được ghi lại trong bảng sau
Mẫu thử Thuốc thử Hiện tượng
X Nước Br
2
Kết tủa trắng
Y Dung dịch AgNO
3
trong NH
3
đun nóng Kết tủa Ag trắng sáng
Z Quỳ tím Chuyển màu hồng
T Cu(OH)
2
Có màu tím
Các dung dịch X, Y, Z, T lần lượt là
A. Fructozơ, anilin, axit axetic, anbumin.
B. Anilin, fructozơ, anbumin, axit axetic.
Trang 4
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
C. Anilin, anbumin, axit axetic, fructozơ.
D. Anilin, fructozơ, axit axetic, anbumin.
Câu 34: Nhiệt phân hoàn toàn 27,09 gam hỗn hợp BaCO
3
và Al(OH)
3
đến khối lượng không đổi, thu
được hỗn hợp X,. Hòa tan hoàn toàn X vào lượng nước dư, thu được dung dịch Y trong suốt. Cho từ từ
dung dịch HCl 1M vào dung dịch Y, phản ứng được biểu diễn theo đồ thị sau:
Giá trị của a là
A. 7,02. B. 7,80. C. 6,24. D. 9,36.
Câu 35: Hỗn hợp X gồm hai chất có công thức phân tử là C
3
H
7
NO
4
và C
3
H
7
NO
2
. Cho 56,52 gam X tác
dụng vừa đủ với dung dịch NaOH 32% (đun nóng), cô cạn dung dịch sau phản ứng, thu được hỗn hợp Y
gồm hai muối đều có phân tử khối nhỏ hơn 100 và 89,32 gam hỗn hợp Z gồm hơi nước và chất hữu cơ T.
Biết tỉ khối củ T so với H
2
là 16. Phần trăm khối lượng của muối có phân tử khối nhỏ hơn trong Y là
A. 52,87%. B. 30,14%. C. 53,25%. D. 31,39%.
Câu 36: Cho các phát biểu sau:
(a) Kim loài kiềm được điều chế bằng phương pháp điện phân dung dịch muối halogenua tương ứng.
(b) Sắt có trong hemoglobin (huyết cầu tố) của máu.
(c) Độ dinh dưỡng của phân kali được đánh giá theo phần trăm khối lượng nguyên tố kali.
(d) Dung dịch axit nitric đặc, không màu để ngoài ánh sáng lâu ngày sẽ chuyển thành màu vàng.
(e) Tất cả các ion kim loại đều không có tính khử.
Số phát biểu sai là
A. 1. B. 2. C. 3. D. 4.
Câu 37: Hòa tan hoàn toàn m gam hỗn hợp X gồm Fe, Fe
3
O
4
, FeS (trong đó nguyên tố oxi chiếm 12,5%
về khối lượng) trong dung dịch chứa a mol KNO
3
và 0,43 mol H
2
SO
4
(loãng), sau phản ứng thu được khi
NO (sản phẩm khử duy nhất của N
+5
và dung dịch Y. Cho Y phản ứng vừa đủ với 740ml dung dịch KOH
1M, thu được 21,4 gam kết tủa và dung dịch Z chứa 101,14 gam hỗn hợp muối. Giá trị của a là
A. 0,38. B. 0,40. C. 0,42. D. 0,44.
Câu 38: Cho X và Y (M
X
< M
Y
) là hai axit cacboxylic đơn chức, mạch hở; T là este mạch hở tạo từ X, Y
và ancol Z. Đốt cháy hoàn toàn 32,65 gam hỗn hợp E gồm X, Y, T cần vừa đủ 31,64 lít O
2
(đktc). Mặt
khác, cho 32,65 gam E tác dụng vừa đủ với 450ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng,
thu được 39,3 gam muối và m gam ancol Z. Dẫn m gam Z vào bình đựng kali dư, sau phản ứng thấy có
khí thoát ra và khối lượng bình tăng 7,5 gam. Phần trăm khối lượng của X trong E là
Trang 5
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85