Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải) Trường THPT ……….. Họ và tên giáo viên Tổ: ………………. ……………… CHƯƠNG 4. HYDROCARBON
BÀI 16: HYDROCARBON KHÔNG NO ( 4 tiết) Tuần: Tiết: Ngày soạn: Thời gian thực hiện: I. MỤC TIÊU Về kiến thức
- Nêu được khái niệm về alkene và alkyne, công thức chung của alkene, alkyne; đặc điểm
liên kết, hình dạng phân tử của ethylene, acetylene.
- Gọi tên một số alkene, alkyne đơn giản (C2-C5), tên thông thường của một vài alkene, alkyne thường gặp.
- Nêu được khái niệm và xác định được đồng phân hình học (cis – trans) trong một số trường hợp đơn giản.
- Nêu được đặc điểm về tính chất vật lý (nhiệt độ nóng chảy, nhiệt độ sôi, tỉ khối, tính tan)
của một số alkene, alkyne.
- Trình bày được các tính chất hóa học của alkene, alkyne: phản ứng cộng hydrogen, cộng
halogen (bromine), cộng hydrogen halide (HBr) và cộng nước; quy tắc Markovnikov (Mac-
cop-nhi-cop); phản ứng trùng hợp của alkene; phản ứng của alk-1-yne với dung dịch
AgNO3 trong NH3, phản ứng oxi hóa hoàn toàn (phản ứng cháy), phản ứng oxi hóa không
hoàn toàn (phản ứng làm mất màu dung dịch KMnO4 của alkene, alkyne).
- Thực hiện được thí nghiệm điều chế và thử tính chất của ethylene và acetylene (phản ứng
cháy, phản ứng với nước bromine, phản ứng mất màu thuốc tím); mô tả các hiện tượng thí
nghiệm và giải thích được tính chất hóa học của alkene,alkyne.
- Trình bày được ứng dụng của các alkene và acetylene trong thực tiễn; phương pháp điều
chế alkene, acetylene trong phòng thí nghiệm (phản ứng dehydrate hóa alcohol điều chế
alkene, từ calcium carbide điều chế acetylene) và trong công nghiệp (phản ứng cracking
điều chế alkene, điều chế acetylene từ methane). Về năng lực
- Tự chủ và tự học: Chủ động, tích cực tìm hiểu về bộ môn hóa học.
- Giao tiếp và hợp tác: Sử dụng ngôn ngữ khoa học để diễn đạt về đối tượng nghiên cứu của
hóa học; phương pháp học tập và nghiên cứu hóa học; vai trò của hóa học đối với đời sống,
sản xuất,…; hoạt động nhóm cách hiệu quả theo đúng yêu cầu của giáo viên, đảm bảo các
thành viên trong nhóm đều được tham gia và trình bày báo cáo.
- Giải quyết vấn đề và sáng tạo: Thảo luận với các thành viên trong nhóm nhằm giải quyết
các vấn đề trong bài học hoàn thành nhiệm vụ học tập.
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải) Về phẩm chất
- Chăm chỉ, tham gia tích cực hoạt động nhóm phù hợp với khả năng của bản thân.
- Cẩn thận, trung thực và thực hiện an toàn trong quá trình làm thực hành.
- Có niềm say mê hứng thú với việc khám phá và học tập hóa học.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU 1. Giáo viên
- Phim thí nghiệm ethylene, acetylene tác dụng nước bromine, dung dịch KMnO4; acetylen
tác dụng dung dịch AgNO3/NH3.
- Dụng cụ: Ống nghiệm, ống hút nhỏ giọt, chén sứ, que đóm, giá đỡ ống nghiệm, bông hấp, nút cao su, đá bọt
- Hóa chất: CaC2, C2H5OH, H2SO4 đặc, nước bromine, dung dịch KMnO4, dung dịch NaOH. - Phiếu học tập. 2. Học sinh
- Sách giáo khoa, vở ghi bài, bảng nhóm. II. TIẾN TRÌNH DẠY HỌC
1. Hoạt động: Khởi động. 5’ a. Mục tiêu
- Tạo hứng thú và kích thích sự tò mò của học sinh vào chủ đề học tập. Học sinh tiếp
nhận kiến thức chủ động, tích cực, hiệu quả. b. Nội dung CÂU HỎI KHỞI ĐỘNG
Giáo viên cho học sinh xem các hình ảnh giới thiệu về khí X.
Khí X sinh ra từ trái cà chín kích thích các trái
Khí X sinh ra từ quá trình hô hấp của quả chuối
còn xanh xung quanh nhanh chín
sau thu hoạch làm cà chua xanh mau chín
1. Tham khảo SGK, cho biết tên của khí X?
2. Viết CTCT của C2H6, C2H4, C2H2? Nêu sự khác nhau về đặc đặc điểm liên kết trong ba phân tử hydrocarbon đó?
c. Sản phẩm: Các câu trả lời của HS.
TRẢ LỜI CÂU HỎI KHỞI ĐỘNG 1. Khí ethylene.
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
2. CTCT: CH3 – CH3; CH2 = CH2 ; HC ≡ CH
Điểm khác về cấu tạo giữa các chất: Trong C2H6: chỉ có liên kết đơn; C2H4: có nhiều liên kết
đơn và một liên kết đôi; C2H2: có nhiều liên kết đơn và một liên kết ba. d. Tổ chức thực hiện
Chuyển giao nhiệm vụ học tập
Yêu cầu học sinh quan sát video và hình ảnh lửa cháy ở bếp gas, trả lời câu hỏi trong phiếu khởi động. HS nhận nhiệm vụ. Thực hiện nhiệm vụ
HS Suy nghĩ và trả lời câu hỏi
GV Theo dõi và hỗ trợ cho nhóm HS
Báo cáo kết quả và thảo luận
Yêu cầu đại diện một học sinh báo cáo kết quả
Kết luận và nhận định
C2H4 (ethylene) và C2H2 (acetylen) là các hydrocarbon không no, trong đó, C2H4 là alkene,
C2H2 là alkyne. Các alkene, alkyne có cấu tạo, tính chất và ứng dụng gì, chúng ta sẽ cùng tìm hiểu trong bài này.
2. Hoạt động: Hình thành kiến thức mới
Hoạt động 1: Khái niệm, đồng phân, danh pháp Mục tiêu:
- Nêu được khái niệm về alkene và alkyne, công thức chung của alkene, alkyne; đặc điểm
liên kết và hình dạng phân tử của ethylene và acethylene.
- Gọi được tên một số alkene và alkyne đơn giản (C2 – C5), tên thông thường một vài
alkene, alkyne thường gặp.
- Nêu được khái niệm và xác định được đồng phân hình học (cis và trans) trong một số trường hợp đơn giản. Hoạt động của GV - HS Nội dung
Giao nhiệm vụ học tập:
I. Khái niệm, đồng phân, danh pháp
GV yêu cầu HS thảo luận nhóm, 1. Khái niệm và công thức chung của alkene,
hoàn thành các câu hỏi sau trong alkyne
phiếu học tập số 1: (10 phút)
Hydrocarbon không no là những hydrocarbon trong HS nhận nhiệm vụ.
phân tử có chứa liên kết đôi, liên kết ba (gọi chung là
Thực hiện nhiệm vụ học tập
- HS thảo luận hoàn thành phiếu liên kết bội) hoặc đồng thời cả liên kết đôi và liên kết học tập. ba.
- GV theo dõi, đôn đốc và hỗ trợ
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
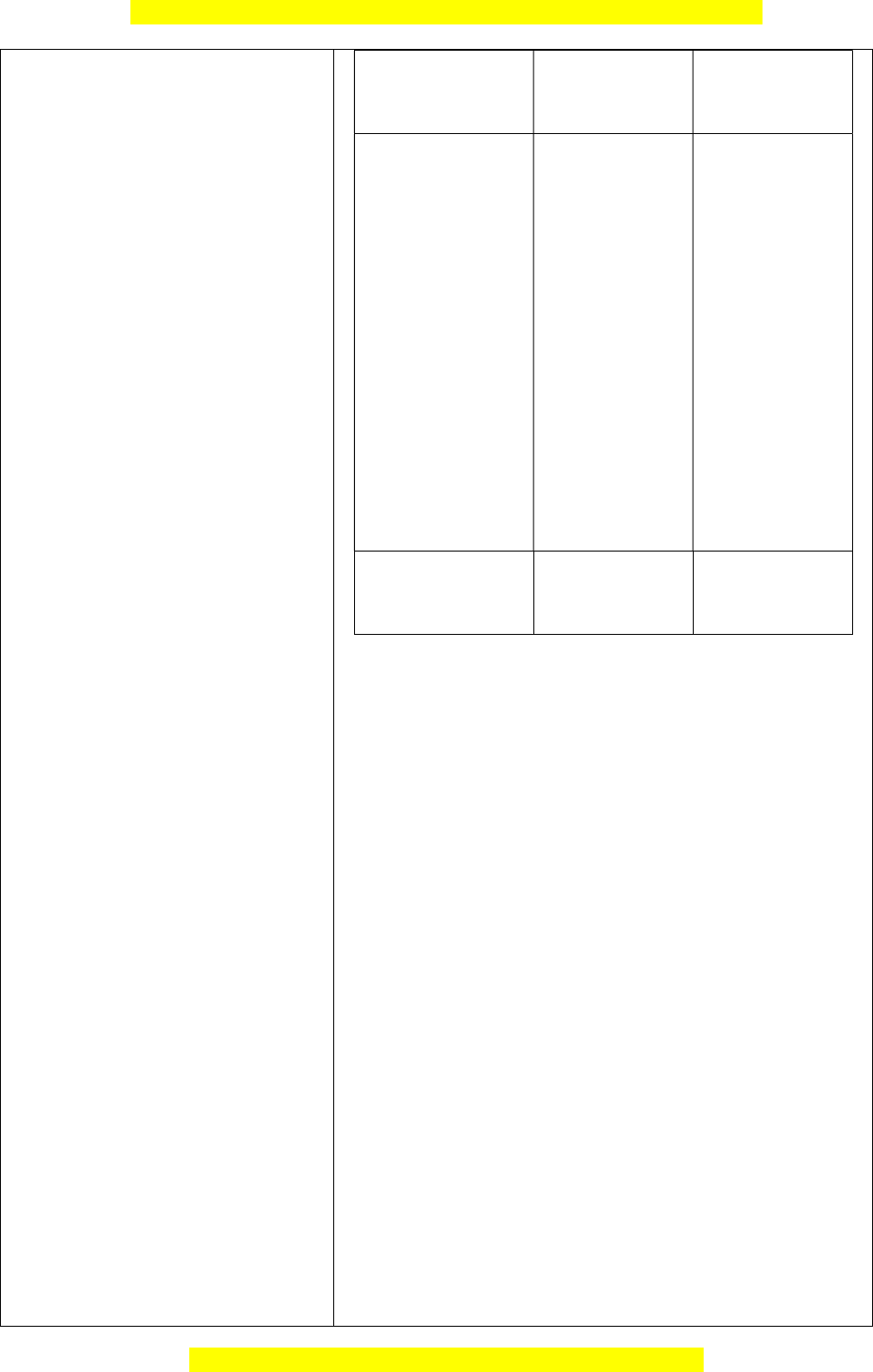
Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải) HS khi cần thiết. Hydrocarbon Alkene Alkyne Báo cáo, thảo luận không no
- HS lên trình bày kết quả Khái niệm
Alkene là các Alkyne là các
- Các HS còn lại chú ý theo dõi, hydrocarbon hydrocarbon nhận xét. Kết luận, nhận định không no, không no,
GV tổng kết, chốt kiến thức
mạch hở, có mạch hở có
chứa một liên chứa một liên
kết đôi >C = kết ba − C≡C
C< trong phân – trong phân tử tử Công thức CnH2n (n ≥ 2) CnH2n - 2 (n ≥ chung 2) 2. Đồng phân a) Đồng phân cấu tạo
Alkene và alkyne có hai loại đồng phân cấu tạo là
đồng phân vị trí liên kết bội (từ C4 trở lên) và đồng
phân mạch carbon (từ C4 trở lên với alkene và từ C5 trở lên với alkyne). b) Đồng phân hình học
Trong phân tử alkene nếu mỗi nguyên tử carbon của
liên kết đôi liên kết với hai nguyên tử hoặc hai nhóm
nguyên tử khác nhau thì sẽ có đồng phân hình học.
+ Nếu mạch chính nằm ở cùng một phía của liên kết
đôi, gọi là đồng phân hình học dạng cis −.
+ Nếu mạch chính nằm ở hai phía khác nhau của liên
kết đôi, gọi là đồng phân hình học dạng trans−. 3. Danh pháp
Tên theo danh pháp thay thế của alkene và alkyne:
Phần nền - vị trí liên kết bội - ene hoặc yne
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
Giáo án Hydrocarbon không no Hóa học 11 Kết nối tri thức
1.1 K
537 lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Bộ giáo án Hóa học 11 Kết nối tri thức được cập nhật liên tục trong gói này từ nay đến hết tháng 3/2024
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Bộ giáo án Hóa học 11 Kết nối tri thức năm 2023 mới, chuẩn nhất được thiết kế theo phong cách hiện đại, đẹp mắt, trình bày chi tiết cho từng bài học và bám sát chương trình Sách giáo khoa Hóa học 11 Kết nối tri thức.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(1073 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN Hóa Học
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Lớp 11
Xem thêmTài liệu bộ mới nhất

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
Trường THPT ………..
Tổ: ……………….
Họ và tên giáo viên
………………
CHƯƠNG 4. HYDROCARBON
BÀI 16: HYDROCARBON KHÔNG NO ( 4 tiết)
Tuần: Tiết: Ngày soạn: Thời gian thực hiện:
I. MỤC TIÊU
Về kiến thức
- Nêu được khái niệm về alkene và alkyne, công thức chung của alkene, alkyne; đặc điểm
liên kết, hình dạng phân tử của ethylene, acetylene.
- Gọi tên một số alkene, alkyne đơn giản (C2-C5), tên thông thường của một vài alkene,
alkyne thường gặp.
- Nêu được khái niệm và xác định được đồng phân hình học (cis – trans) trong một số
trường hợp đơn giản.
- Nêu được đặc điểm về tính chất vật lý (nhiệt độ nóng chảy, nhiệt độ sôi, tỉ khối, tính tan)
của một số alkene, alkyne.
- Trình bày được các tính chất hóa học của alkene, alkyne: phản ứng cộng hydrogen, cộng
halogen (bromine), cộng hydrogen halide (HBr) và cộng nước; quy tắc Markovnikov (Mac-
cop-nhi-cop); phản ứng trùng hợp của alkene; phản ứng của alk-1-yne với dung dịch
AgNO
3
trong NH
3
, phản ứng oxi hóa hoàn toàn (phản ứng cháy), phản ứng oxi hóa không
hoàn toàn (phản ứng làm mất màu dung dịch KMnO
4
của alkene, alkyne).
- Thực hiện được thí nghiệm điều chế và thử tính chất của ethylene và acetylene (phản ứng
cháy, phản ứng với nước bromine, phản ứng mất màu thuốc tím); mô tả các hiện tượng thí
nghiệm và giải thích được tính chất hóa học của alkene,alkyne.
- Trình bày được ứng dụng của các alkene và acetylene trong thực tiễn; phương pháp điều
chế alkene, acetylene trong phòng thí nghiệm (phản ứng dehydrate hóa alcohol điều chế
alkene, từ calcium carbide điều chế acetylene) và trong công nghiệp (phản ứng cracking
điều chế alkene, điều chế acetylene từ methane).
Về năng lực
- Tự chủ và tự học: Chủ động, tích cực tìm hiểu về bộ môn hóa học.
- Giao tiếp và hợp tác: Sử dụng ngôn ngữ khoa học để diễn đạt về đối tượng nghiên cứu của
hóa học; phương pháp học tập và nghiên cứu hóa học; vai trò của hóa học đối với đời sống,
sản xuất,…; hoạt động nhóm cách hiệu quả theo đúng yêu cầu của giáo viên, đảm bảo các
thành viên trong nhóm đều được tham gia và trình bày báo cáo.
- Giải quyết vấn đề và sáng tạo: Thảo luận với các thành viên trong nhóm nhằm giải quyết
các vấn đề trong bài học hoàn thành nhiệm vụ học tập.

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
Về phẩm chất
- Chăm chỉ, tham gia tích cực hoạt động nhóm phù hợp với khả năng của bản thân.
- Cẩn thận, trung thực và thực hiện an toàn trong quá trình làm thực hành.
- Có niềm say mê hứng thú với việc khám phá và học tập hóa học.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
1. Giáo viên
- Phim thí nghiệm ethylene, acetylene tác dụng nước bromine, dung dịch KMnO
4
; acetylen
tác dụng dung dịch AgNO
3
/NH
3
.
- Dụng cụ: Ống nghiệm, ống hút nhỏ giọt, chén sứ, que đóm, giá đỡ ống nghiệm, bông hấp,
nút cao su, đá bọt
- Hóa chất: CaC
2
, C
2
H
5
OH, H
2
SO
4
đặc, nước bromine, dung dịch KMnO
4
, dung dịch NaOH.
- Phiếu học tập.
2. Học sinh
- Sách giáo khoa, vở ghi bài, bảng nhóm.
II. TIẾN TRÌNH DẠY HỌC
1. Hoạt động: Khởi động. 5’
a. Mục tiêu
- Tạo hứng thú và kích thích sự tò mò của học sinh vào chủ đề học tập. Học sinh tiếp
nhận kiến thức chủ động, tích cực, hiệu quả.
b. Nội dung
CÂU HỎI KHỞI ĐỘNG
Giáo viên cho học sinh xem các hình ảnh giới thiệu về khí X.
1. Tham khảo SGK, cho biết tên của khí X?
2. Viết CTCT của C
2
H
6
, C
2
H
4
, C
2
H
2
? Nêu sự khác nhau về đặc đặc điểm liên kết trong ba
phân tử hydrocarbon đó?
c. Sản phẩm: Các câu trả lời của HS.
TRẢ LỜI CÂU HỎI KHỞI ĐỘNG
1. Khí ethylene.
Khí X sinh ra t
ừ
trái cà chín kích thích các trái
còn xanh xung quanh nhanh chín
Khí X sinh ra t
ừ
quá trình hô h
ấ
p c
ủ
a qu
ả
chu
ố
i
sau thu hoạch làm cà chua xanh mau chín

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
2. CTCT: CH
3
– CH
3
; CH
2
= CH
2
; HC ≡ CH
Điểm khác về cấu tạo giữa các chất: Trong C
2
H
6
: chỉ có liên kết đơn; C
2
H
4
: có nhiều liên kết
đơn và một liên kết đôi; C
2
H
2
: có nhiều liên kết đơn và một liên kết ba.
d. Tổ chức thực hiện
Chuyển giao nhiệm vụ học tập
Yêu cầu học sinh quan sát video và hình ảnh lửa cháy ở bếp gas, trả lời câu hỏi trong phiếu
khởi động.
HS nhận nhiệm vụ.
Thực hiện nhiệm vụ
HS Suy nghĩ và trả lời câu hỏi
GV Theo dõi và hỗ trợ cho nhóm HS
Báo cáo kết quả và thảo luận
Yêu cầu đại diện một học sinh báo cáo kết quả
Kết luận và nhận định
C
2
H
4
(ethylene) và C
2
H
2
(acetylen) là các hydrocarbon không no, trong đó, C
2
H
4
là alkene,
C
2
H
2
là alkyne. Các alkene, alkyne có cấu tạo, tính chất và ứng dụng gì, chúng ta sẽ cùng
tìm hiểu trong bài này.
2. Hoạt động: Hình thành kiến thức mới
Hoạt động 1: Khái niệm, đồng phân, danh pháp
Mục tiêu:
- Nêu được khái niệm về alkene và alkyne, công thức chung của alkene, alkyne; đặc điểm
liên kết và hình dạng phân tử của ethylene và acethylene.
- Gọi được tên một số alkene và alkyne đơn giản (C
2
– C
5
), tên thông thường một vài
alkene, alkyne thường gặp.
- Nêu được khái niệm và xác định được đồng phân hình học (cis và trans) trong một số
trường hợp đơn giản.
Hoạt động của GV - HS Nội dung
Giao nhiệm vụ học tập:
GV yêu cầu HS thảo luận nhóm,
hoàn thành các câu hỏi sau trong
phiếu học tập số 1: (10 phút)
HS nhận nhiệm vụ.
Thực hiện nhiệm vụ học tập
- HS thảo luận hoàn thành phiếu
học tập.
- GV theo dõi, đôn đốc và hỗ trợ
I. Khái niệm, đồng phân, danh pháp
1. Khái niệm và công thức chung của alkene,
alkyne
Hydrocarbon không no là những hydrocarbon trong
phân tử có chứa liên kết đôi, liên kết ba (gọi chung là
liên kết bội) hoặc đồng thời cả liên kết đôi và liên kết
ba.
Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
HS khi cần thiết.
Báo cáo, thảo luận
- HS lên trình bày kết quả
- Các HS còn lại chú ý theo dõi,
nhận xét.
Kết luận, nhận định
GV tổng kết, chốt kiến thức
Hydrocarbon
không no
Alkene Alkyne
Khái niệm
Alkene là các
hydrocarbon
không no,
mạch hở, có
chứa một liên
kết đôi >C =
C< trong phân
tử
Alkyne là các
hydrocarbon
không no,
mạch hở có
chứa một liên
kết ba − C≡C
– trong phân
tử
Công thức
chung
C
n
H
2n
(n ≥ 2) C
n
H
2n - 2
(n ≥
2)
2. Đồng phân
a) Đồng phân cấu tạo
Alkene và alkyne có hai loại đồng phân cấu tạo là
đồng phân vị trí liên kết bội (từ C4 trở lên) và đồng
phân mạch carbon (từ C4 trở lên với alkene và từ C5
trở lên với alkyne).
b) Đồng phân hình học
Trong phân tử alkene nếu mỗi nguyên tử carbon của
liên kết đôi liên kết với hai nguyên tử hoặc hai nhóm
nguyên tử khác nhau thì sẽ có đồng phân hình học.
+ Nếu mạch chính nằm ở cùng một phía của liên kết
đôi, gọi là đồng phân hình học dạng cis −.
+ Nếu mạch chính nằm ở hai phía khác nhau của liên
kết đôi, gọi là đồng phân hình học dạng trans−.
3. Danh pháp
Tên theo danh pháp thay thế của alkene và alkyne:
Phần nền - vị trí liên kết bội - ene hoặc yne

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
Lưu ý:
+ Chọn mạch carbon dài nhất, có nhiều nhánh nhất và
có chứa liên kết bội làm mạch chính.
+ Đánh số sao cho nguyên tử carbon có liên kết bội
(đôi hoặc ba) có chỉ số nhỏ nhất (đánh số mạch chính
từ đầu gần liên kết bội).
+ Dùng chữ số (1, 2, 3,...) và gạch nối (-) để chì vị trí
liên kết bội (nếu chỉ có một vị trí duy nhất của liên kết
bội thì không cần).
+ Nếu alkene hoặc alkyne có nhánh thì cần thêm vị trí
nhánh và tên nhánh trước tên của alkene và alkyne
tương ứng với mạch chính.
Phiếu học tập số 1:
Nhóm 1:
Câu 1. Hydrocarbon không no là gì? Cho VD?
Câu 2. Alkene, alkyne là gì? Viết công thức chung của alkene và alkyne.
Nhóm 2:
Câu 3. Viết CTCT alkene của phân tử C
4
H
8
và xét xem có CT nào có đồng phân hình học?
Câu 4. Viết CTCT của alkyne có công thức phân tử C
4
H
6
Nhóm 3
Câu 5. Gọi tên thay thế và tên thường gọi của các alkene sau
Nhóm 4
Câu 6. Gọi tên thay thế và tên thường gọi của các alkyne sau
Đáp án phiếu học tập số 1
Câu 1:
- Hydrocarbon không no là những hydrocarbon trong phân tử có chứa liên kết đôi (C=C)
hoặc liên kết ba (C≡C) (gọi chung là liên kết bội) hoặc cả 2 loại liên kết đó.
VD: CH
2
= CH
2
; CH ≡ CH; CH
2
= CH – C ≡CH

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
Câu 2:
- Alkene là các hydrocarbon không no, mạch hở, có chứa 1 liên kết đôi C=C trong phân tử,
có công thức chung là C
n
H
2n
(n≥2).
VD: CH
2
= CH
2
; CH
3
– CH = CH
2
- Alkyne là các hydrocarbon không no, mạch hở, có chứa 1 liên kết ba C≡C trong phân tử,
có công thức chung là C
n
H
2n – 2
(n≥2).
VD: CH ≡ CH ; CH
3
– C ≡ CH
Câu 3:
- Alkene C
4
H
8
Đồng phân hình học
Cis-but-2-ene tran-but-2-ene
Câu 4:
- Alkyne C
4
H
6
Câu 5:
Tên alkene
Câu 6:
Tên akyne
CH
2
= CH
2
ethene
(ethylene)
HC ≡ CH
Ethyne
(acetylene)
CH
2
= CH – CH
3
propene
(propylene)
CH ≡ C – CH
3
propyne
but-1-ene
but-2-ene
methylpropene
but-1-yne
but-2-yne
Hoạt động 2: Tính chất vật lí (10 phút)
a. Mục tiêu
Biết được trạng thái, tính tan, sự thay đổi nhiệt độ sôi, nhiệt độ nóng chảy của alkene và
alkyne theo chiều tăng khối lượng phân tử.
b. Nội dung

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
PHIẾU HỌC TẬP SỐ 2
Câu 1. Vì sao nhiệt độ sôi, nhiệt độ nóng chảy của các alkene và alkyne tăng dần khi số
nguyên tử carbon trong phân tử tăng?
Câu 2. Vì sao các alkene và alkyne không tan hoặc rất ít tan trong nước, tan tốt trong các
dung môi hữu cơ như acetone, chloroform,…
c. Sản phẩm
TRẢ LỜI PHIẾU HỌC TẬP SỐ 2
Câu 1. Khi số nguyên tử carbon trong phân tử tăng khối lượng phân tử tăng tường
tác van der Waals tăng nhiệt độ sôi, nhiệt độ nóng chảy của các alkene và alkyne tăng.
Câu 2. Trong phân tử alkene, alkyne là các chất kém phân cực chúng hầu như không
tan trong nước (là dung môi phân cực), tan tốt trong các dung môi hữu cơ (là dung môi
không phân cực)
d. Tổ chức thực hiện
HOẠT ĐỘNG CỦA GV - HS
NỘI DUNG
Chuyển giao nhiệm vụ học tập
GV yêu cầu HS hoạt động cá nhân hoặc cặp đôi,
hoàn thành phiếu học tập số 3.
HS nhận nhiệm vụ.
Thực hiện nhiệm vụ
HS thực hiện nhiệm vụ
GV Theo dõi và hỗ trợ cho nhóm HS
Báo cáo kết quả và thảo luận
GV Gọi HS báo cáo kết quả phiếu học tập số 3
Các HS còn lại chú ý theo dõi,nhận xét.
Kết luận và nhận định
GV Nhận xét và chốt kiến thức
II. Tính chất vật lý của alkene,
alkyne
- Ở điều kiện thường, các alkene,
alkyne từ
+ C2 C4: Chất khí (trừ but–2–
yne)
+ C5 (trừ but–2– yne) C17: Chất
lỏng
+ C18 trở đi: Chất rắn
- Khi khối lượng phân tử tăng, nhiệt
độ sôi, nhiệt độ nóng chảy của
alkene, alkyne tăng.
- Các alkene, alkyne đều nhẹ hơn
nước, không tan trong nước, tan
trong dung môi hữu cơ.
Hoạt động 3: Tính chất hóa học
Mục tiêu:
- Trình được các tính chất hóa học của alkene, alkyne: phản ứng cộng hydrogen, cộng
halogen (bromine); cộng hydrogen halide (HBr) và cộng nước; quy tắc Markovnikov;
phản ứng trùng hợp của alkene; phản ứng alk – 1 – yne với dung dịch AgNO
3
trong NH
3
;
phản ứng oxi hóa ( làm mất màu thuốc tím của alkene, phản ứng cháy của alkene,

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
alkyne).
- Thực hiện được thí nghiệm điều chế và thử tính chất của ethylene, acethylene (phản
ứng cháy, phản ứng với nước bromine, phản ứng làm mất màu thuốc tím); mô tả các hiện
tượng thí nghiệm và giải thích được các tính chất hóa học của alkene, alkyne.
Hoạt động của GV Hoạt động của HS
- Giao nhiệm vụ cho nhóm chuyên gia: Các
nhóm chuyên gia lần lược làm các phiếu bài
tập
- Cho HS di chuyển về nhóm mảnh ghép
tiếp tục thảo luận để hoàn thành phiếu học
tập ở nhóm mảnh ghép (20 phút)
- Cho các nhóm treo kết quả thảo luận lên
bảng. Giáo viên sửa và yêu cầu HS chấm
chéo. (30 phút)
- Các nhóm chuyên gia thảo luận nhóm
trong 10 phút để hoàn thành phiếu học tập.
- Di chuyển về nhóm mảnh ghép và thực
hiện nhiệm vụ. (20 phút)
- Treo kết quả thảo luận lên bảng và chấm
chéo
Phiếu học tập nhóm chuyên gia
Nhóm chuyên gia 1: Tìm hiểu về phản ứng cộng và quy tắc Markovnikov
- Đặc điểm chung của liên kết bội là gì?
- Phản ứng đặc trưng của hợp chất chứa liên kết bội. Cho VD minh họa
- Quy tắc Markovnikov áp dụng vào trường hợp nào? Cho VD
Nhóm chuyên gia 2: Tìm hiểu về phản ứng trùng hợp
- Phản ứng trùng hợp là gì? Ứng dụng của phản ứng trùng hợp
- Nêu điều kiện một chất tham gia phản ứng trùng hợp.
- Nêu VD về phản ứng trùng hợp và chỉ rõ: monomer; polimer; hệ số trùng hợp
Nhóm chuyên gia 3: Tìm hiểu phản ứng của alk-1-yne với dung dịch AgNO
3
trong NH
3
- Viết phương trình chung khi cho alk-1-yne tác dụng với dung dịch AgNO
3
trong NH
3
.
- Lấy VD acetylene và propylene tác dụng với dung dịch AgNO
3
trong NH
3
. Nêu điểm
giống và khác nhau của 2 phản ứng này.
Nhóm chuyên gia 4: Tìm hiểu và phản ứng oxi hóa
- Viết PTPU khi cho ethene tác dụng với dung dịch KMnO
4
ở nhiệt độ thường
- Viết PTPU đốt cháy alkene; ankyne và cho VD
- Nêu rõ mối quan hệ số mol CO
2
và H
2
O
Phiếu học tập của nhóm mảnh ghép
1. Đặc điểm cấu tạo phân tử ethylene và của phân tử acetylene

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
Trong phân tử ethylene có một
……………………………………………
Liên kết đôi gồm
………………………….. .
Trong phân tử acetylene có một
……………………………………………
Liên kết ba gồm
…………………………… .
2. Phản ứng cộng
Liên kết π trong các liên kết bội ………………, ………..……. ra để tạo thành các liên kết
mới.
a. Cộng H
2
b. Cộng halogen
c. Cộng hydrogene halide
d. Phản ứng cộng nước
* Quy tắc Markovnikov:
....................................................................................................................................................
....................................................................................................................................................
....................................................................................................................................................
....................................................................................................................................................
....................................................................................................................................................
3. Phản ứng trùng hợp
- Phản ứng trùng hợp là
....................................................................................................................................................
....................................................................................................................................................
Phản ứng trùng hợp được ứng dụng:
……………………………………………………………….

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
Hãy nêu ý nghĩa của chữ n; chỉ ra đâu là monomer; đâu là monomer
4. Phản ứng của alk-1-yne với AgNO
3
trong NH
3
HC ≡ CH + AgNO
3
+ NH
3
CH
3
– C ≡ CH + AgNO
3
+ NH
3
Nêu điểm giống và khác nhau của 2 phản ứng này. Giải thích?
5. Phản ứng oxi hóa
a. Oxi hóa không hoàn toàn
CH
2
= CH
2
+ KMnO
4
+ H
2
O
b. Oxi hóa hoàn toàn (phản ứng cháy)
C
n
H
2n
+ O
2
t
o
C
n
H
2n-2
+ O
2
t
o
Nêu rõ mối quan hệ số mol CO
2
và H
2
O
Đáp án phiếu học tập nhóm mảnh ghép
1. Đặc điểm cấu tạo phân tử ethylene và của phân tử acetylene
CH
2
= CH
2
HC CH
Trong phân tử ethylene có một liên kết đôi
Liên kết đôi gồm 1 liên kết π và 1 liên kết σ
Trong phân tử acetylene có một liên kết ba
Liên kết ba gồm 2 liên kết π và 1 liên kết σ
2. Phản ứng cộng
Liên kết π trong các liên kết bội rất kém bền, dễ bị đứt ra để tạo thành các liên kết
mới.
a. Cộng H
2
CH
2
= CH
2
+ H
2
HC CH + 2H
2
C
2
H
4
+ H
2
C
2
H
2
+ 2H
2
HC CH + H
2
C
2
H
2
+ H
2
Ni, t
o
, p
Ni, t
o
, p
Ni, t
o
, p
Ni, t
o
, p
pd, t
o
, p
pd, t
o
, p
CH
3
- CH
3
CH
3
- CH
3
CH
2
= CH
2
C
2
H
6
C
2
H
6
C
2
H
4
b. Cộng halogen
CH
2
= CH
2
+ Br
2
HC CH + Br
2
C
2
H
4
+ Br
2
C
2
H
2
+ Br
2
Br-CH
2
- CH
2
-Br
Br-CH = CH - Br
C
2
H
4
Br
2
C
2
H
2
Br
2

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
c. Cộng hydrogene halide
d. Phản ứng cộng nước
* Quy tắc Markovnikov:
Khi cộng một tác nhân bất đối xứng vào một alkene bất đối xứng thì phần điện tích dương
của tác nhân ưu tiên tấn công vào C mang liên kết đôi có nhiều H hơn (bậc thấp hơn), còn
nguyên tử hay nhóm nguyên tử mang điện tích âm cộng vào nguyên tử cacbon bậc cao hơn.
3. Phản ứng trùng hợp
Phản ứng trùng hợp được ứng dụng: sản xuất polimer.
Hãy nêu ý nghĩa của chữ n; chỉ ra đâu là monomer; đâu là monomer
4. Phản ứng của alk-1-yne với AgNO
3
trong NH
3
HC ≡ CH + 2AgNO
3
+ 2NH
3
AgC ≡ CAg + 2NH
4
NO
3
(1)
CH
3
– C ≡ CH + AgNO
3
+ NH
3
CH
3
– C ≡ CAg + NH
4
NO
3
(2)
Phản ứng 1 phản ứng theo tỉ lệ mol 1:2, phản ứng 2 phản ứng theo tỉ lệ mol 1:1
5. Phản ứng oxi hóa
a. Oxi hóa không hoàn toàn
3CH
2
= CH
2
+ 2KMnO
4
+ 4H
2
O 3HO-CH
2
– CH
2
– OH + 2KOH + 2MnO
2
b. Oxi hóa hoàn toàn (phản ứng cháy)
0
t
n 2n 2 2 2
2 2
3n
C H + O nCO + nH O
2
nCO = nH O
0
t
n 2n 2 2 2 2
2 2
3n 2
C H + O nCO + (n - 1)H O
2
nCO > nH O
2.5. Tìm hiểu ứng dụng và cách điều chế alkene, alkyne. 15’
a. Mục tiêu
Biết phản ứng và cách điều chế alkene, alkyne trong công nghiệp; cách điều chế alkene,
alkyne.
b. Nội dung
PHIẾU HỌC TẬP SỐ 4

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
Câu 1.
Tại sao actylene được dùng làm nhiên liện trong đèn xì oxy – acetylene mà không
dùng ethylene?
Câu 2. Vì sao không được dùng nước để dập tắt đám cháy có đất đèn (có thành phần chính
là CaC
2
)?
c. Sản phẩm
TRẢ LỜI PHIẾU HỌC TẬP SỐ 4
Câu 1. Acetylene khi cháy trong oxygen tạo ngọn lửa có nhiệt độ cao, có thể lên tới
3000
o
C.
Câu 2. CaC
2
+ 2H
2
O C
2
H
2
+ Ca(OH)
2
Khí acetylene sinh ra sẽ tham gia cháy và làm đám cháy to hơn không được dùng nước
để dập tắt đám cháy có đất đèn .
d. Tổ chức thực hiện
HOẠT ĐỘNG CỦA GV - HS NỘI DUNG
Chuyển giao nhiệm vụ học tập
GV Cho HS hoạt động cá nhân hoặc cặp
đôi hoàn thành phiếu học tập số 4.
HS Nhận nhiệm vụ
Thực hiện nhiệm vụ
HS Thảo luận và ghi câu trả lời vào phiếu
học tập
GV Theo dõi và hỗ trợ cho nhóm HS
Báo cáo kết quả và thảo luận
Gv Yêu cầu đại diện HS báo cáo kết quả
phiếu học tập số 4
HS Báo cáo sản phẩm
Kết luận và nhận định
Nhận xét và chốt kiến thức
IV. Ứng dụng của alkene, alkyne và điều
chế alkene, alkyne
a. Ứng dụng của alkene, alkyne
Alkene, alkyne được dùng làm nguyên liệu
tổng hợp hữu cơ, làm nhiên liệu.
b. Điều chế alkene, alkyne
* Trong phòng thí nghiệm
C
2
H
5
OH
o
2 4dac
H SO ,170 C
C
2
H
4
+ H
2
O
CaC
2
+ 2H
2
O C
2
H
2
+ Ca(OH)
2
* Trong công nghiệp
- Cracking alkane alkene
C
15
H
32
o
zeolite,500 C
2C
2
H
4
+ C
3
H
6
+ C
8
H
18
- Chủ yếu từ CH
4
Acetylene
2CH
4
o
1500 C,lamlanhnhanh
C
2
H
2
+ 3H
2
3. Hoạt động: Thực hành – thí nghiệm (30 phút)
a. Mục tiêu
Cho HS thực hành kiểm chứng điều chế và thử tính chất của ethylene và acetylene.
b. Nội dung
Thực hành điều chế và thử tính chất của ethylene và acetylene.
c. Sản phẩm
Kết quả thực hành của học sinh

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
d. Các bước tiến hành
Thí nghiệm 1: Điều chế và thử tính chất của ethylene
GV yêu cầu HS lắp ráp thí nghiệm như hình 16.5 SGK
Bước 1: Cho vài viên đá bọt, 20ml cồn 96
0
vào bình cầu. Rót 40 ml dung dịch H
2
SO
4
đặc
vào ống đong sau đó rót từ từ H
2
SO
4
đặc từ ống đong qua phễu vào bình cầu để tránh sự tỏa
nhiệt quá mạnh.
Bước 2: Đun nóng đến khi ethylene sinh ra và sục ngay vào ống nghiệm (1) và (2).
Bước 3: Thay ống dẫn khí thủy tinh hình chữ L bằng ống dẫn thủy tinh có đầu vuốt nhọn.
Dùng que đóm đang cháy để đốt ethylene ở đầu ống dẫn khí.
Thí nghiệm 2: Điều chế và thử tính chất của acetylene
GV yêu cầu HS lắp ráp thí nghiệm như hình 16.6 SGK
Bước 1: Cho khoảng 5 g đất đèn vào bình cầu có nhánh và cho nước cất vào phễu nhỏ giọt.
Bước 2: Mở khóa phễu nhỏ giọt để nước chảy từ từ xuống, khí acetylene sinh ra được sục
ngay vào các ống nghiệm chứa dung dịch KMnO
4
và nước Br
2
đã chuẩn bị ở trên đến khi
dung dịch mất màu.
Bước 3: Thay ống dẫn khí thủy tinh hình chữ L bằng ống dẫn thủy tinh có đầu vuốt nhọn.
Dùng que đớm đang cháy để đốt acetylene sinh ra ở đầu ống dẫn khí.
4. Hoạt động: Luyện tập. 5’ (cho HS về nhà làm)
a. Mục tiêu
- Tái hiện và vận dụng những kiến thức đã học trong bài alkene, alkyne để giải bài tập.
b. Nội dung
PHIẾU HỌC TẬP 5
Câu 1. Viết CTCT của các chất có tên gọi sau:
a. 2-methylbut-2-ene
b. cis-pent-2-ene
c. pent-2-yne
d. cis-pent-2-ene
Câu 2. Viết phương trình hóa học của các phản ứng
a. Propene tác dụng hydrogen, xúc tác nickel
b. Propene tác dụng nước, xúc tác H
3
PO
4
c. 2-methylpropene tác dụng nước, xúc tác H
3
PO
4
d. But-2-ene tác dụng nước bromine
Câu 3. Trình bày các nhận biết 3 chất khí: ethane, ethylen, acetylene?
Câu 4. Đốt cháy hoàn toàn 3,7185 lít (đkc) một hydrocarbon mạch hở Y thu được 11,1555
lít CO
2
(đkc) và 8,1 gam nước. Tìm CTPT của Y?
c. Sản phẩm

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
TRẢ LỜI PHIẾU HỌC TẬP 5
Câu 1.
a. 2-methylbut-2-ene : CH
3
-C(CH
3
)=CH-CH
3
b. pent-2-ene : CH
3
– CH=CH – CH
2
– CH
3
c. pent-2-yne :
d. cis-pent-2-ene :
Câu 2.
a. CH
2
=CH-CH
3
+ H
2
o
Ni,t
CH
3
-CH
2
-CH
3
b. CH
3
-CH=CH
2
2 3 4
H O,xt:H PO
CH
3
-CH(OH)-CH
3
+ CH
3
-CH
2
-CH
2
OH
c. CH
3
-C(CH
3
)=CH
2
2 3 4
H O,xt:H PO
CH
3
-C(CH
3
)(OH)-CH
3
+ CH
3
-CH(CH
3
)-CH
2
OH
d. CH
3
-CH=CH-CH
3
+ Br
2
CH
3
-CHBr-CHBr-CH
3
Câu 3.
- Dùng dung dịch AgNO
3
/NH
3
nhận được acetylene do tạo kết tủa vàng
- Dùng nước bromine nhận được ethylene do làm mất màu nước bromine
- Còn lại ethane
Câu 4.
Vì nH
2
O = nCO
2
= 0,45 hydrocarbon mạch hở Y là alkene. Đặt CT của Y: C
n
H
2n
C
n
H
2n
+
3n
2
O
2
nCO
2
+ nH
2
O
Gt có: n
alkene
= 0,15 mol
số nguyên tử carbon/alkene =
0,45
n 3
0,15
CTPT của Y C
3
H
6
.
5. Hoạt động. Vận dụng. 5’
a. Mục tiêu
Vận dụng được kiến thức đã học để giải thích các hiện tượng xảy ra trong thực tiễn có liên
quan đến bài học.
b. Nội dung
PHIẾU HỌC TẬP SỐ 6
Câu 1. Thực vật có xu hướng sinh ra nhiều ethylene hơn khi bị tổn thương hay gặp điều
kiện bất lợi (hạn hán, ngập úng,…) Vì sao khi bày bán trong siêu thị, rau thường được chứa
trong các túi nilon có lỗ?
Câu 2. Trong một phương pháp tổng hợp polyethylene (PE), các phân tử ethylene được
hoà tan trong dung môi phản ứng với nhau để tạo thành polymer. Có thể sử dụng methyl
alcohol, nước, cyclohexane hay hex-1-ene làm dung môi cho phản ứng trùng hợp PE được

Đây là bản xem thử, vui lòng mua tài liệu để xem chi tiết (có lời giải)
Mọi thắc mắc vui lòng xin liên hệ hotline: 084 283 45 85
không? Giải thích.
c. Sản phẩm: Bài trình bày của HS được ghi vào vở.
d. Tổ chức thực hiện
- GV giao nhiệm vụ cho HS như mục Nội dung và yêu cầu thực hiện nhiệm vụ. HS nộp bài
làm vào buổi học tiếp theo.
- GV chấm bài, nhận xét và có thể cho điểm.
Gợi ý
Câu 1. Các loại rau tươi được chứa trong túi nilon đục lỗ để hơi nước, khí ethylene thoát
ra, tránh làm thối nhũn rau.
Câu 2. Có thể sử dụng methyl alcohol, nước, cyclohexane hay hex-1-ene làm dung môi
cho phản ứng trùng hợp PE. Vì dù ở nhiệt độ cao, PE cũng không thể hòa tan trong nước,
alcolhol, cyclohexane hay hex-1-ene.