ĐỀ KIỂM TRA GIỮA HỌC KÌ I Môn: Hóa học 10
Bộ sách: Cánh diều I. Phần khung đề
1. Hình thức: Gồm:
- Trắc nghiệm khách quan: Trắc nghiệm một lựa chọn đúng; Trắc nghiệm đúng sai;
Trắc nghiệm trả lời ngắn. - Tự luận.
2. Thời gian: 50 phút.
3. Phạm vi kiến thức: Sau khi kết thúc Bài 6: Cấu tạo của bảng tuần hoàn các nguyên tố hoá học.
4. Số lượng câu hỏi:
- Trắc nghiệm khách quan:
+ Trắc nghiệm một lựa chọn đúng: Gồm 12 câu.
+ Trắc nghiệm đúng - sai: Gồm 2 câu. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh
chọn đúng hoặc sai. (Đ – S).
+ Trắc nghiệm yêu cầu trả lời ngắn: Gồm 4 câu. Thí sinh trả lời từ câu 1 đến câu 4.
- Tự luận: Gồm 2 -3 câu. II. Ma trận Tỉ lệ
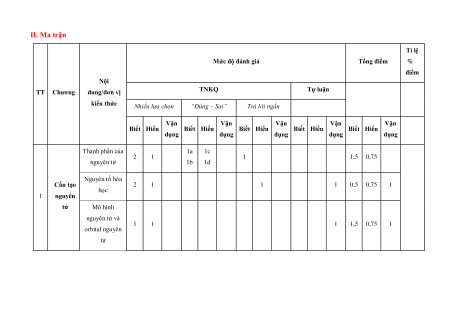
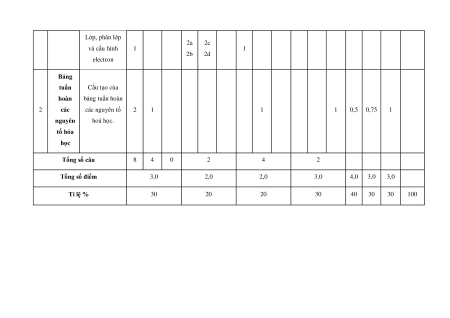
Mức độ đánh giá Tổng điểm % điểm Nội TNKQ Tự luận TT Chương dung/đơn vi ̣ kiến thức Nhiều lựa chọn “Đúng – Sai” Trả lời ngắn Vận Vận Vận Vận Vận Biết Hiểu Biết Hiểu Biết Hiểu Biết Hiểu Biết Hiểu dụng dụng dụng dụng dụng Thành phần của 1a 1c 2 1 1 1,5 0,75 nguyên tử 1b 1d Nguyên tố hóa Cấu tạo 2 1 1 1 0,5 0,75 1 học 1 nguyên tử Mô hình nguyên tử và 1 1 1 1,5 0,75 1 orbital nguyên tử Lớp, phân lớp 2a 2c và cấu hình 1 1 2b 2d electron Bảng tuần Cấu tạo của hoàn bảng tuần hoàn 2 các các nguyên tố 2 1 1 1 0,5 0,75 1 nguyên hoá học. tố hóa học Tổng số câu 8 4 0 2 4 2 Tổng số điểm 3,0 2,0 2,0 3,0 4,0 3,0 3,0 Tỉ lệ % 30 20 20 30 40 30 30 100 III. Đề kiểm tra Sở GD- ĐT …
ĐỀ KIỂM TRA GIỮA HỌC KÌ I TRƯỜNG THPT … Năm học:….. Môn: Hóa học 10 Mã đề thi: 001 Bộ: Cánh diều
Thời gian làm bài: 50 phút;
(Học sinh không được sử dụng tài liệu)
Họ, tên học sinh:..................................................................... Lớp: .............................
A. Phần trắc nghiệm (7 điểm)
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến
câu 12. Mỗi câu hỏi thí sinh chỉ chọn một phương án. (3 điểm)
Câu 1: Hạt nào sau đây nằm ở lớp vỏ nguyên tử? A. Hạt neutron.
B. Hạt proton và neutron. C. Hạt proton. D. Hạt electron.
Câu 2: Trong nguyên tử, hạt nào mang điện?
A. Neutron và electron.
B. Proton và electron. C. Proton và neutron. D. Electron.
Câu 3: X là nguyên tố phổ biến nhất trong Mặt Trời, chiếm khoảng 74% khối lượng
Mặt Trời. Biết một loại nguyên tử của nguyên tố X chỉ tạo nên bởi proton và electron
(không có neutron). Nguyên tố X là A. Lithium. B. Carbon. C. Helium. D. Hydrogen.
Câu 4: Đồng vị là các nguyên tử có cùng số proton nhưng khác nhau về
A. số đơn vị điện tích hạt nhân.
Bộ 11 đề thi giữa kì 1 Hóa học 10 Cánh diều cấu trúc mới có tự luận
3.7 K
1.8 K lượt tải
150.000 ₫
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Bộ tài liệu bao gồm: 8 tài liệu lẻ (mua theo bộ tiết kiệm đến 50%)
- Tailieugiaovien.com.vn giới thiệu bộ 11 đề thi giữa kì 1 gồm 3 đề cấu trúc mới có tự luận form 2025; 8 đề có đầy đủ ma trận và lời giải chi tiết Hóa học 10 Cánh diều mới nhất năm 2023 - 2024 nhằm giúp Giáo viên có thêm tài liệu tham khảo ra đề thi Hóa học lớp 10.
=> Tham khảo thêm: Bộ 11 đề thi giữa kì 1 Hóa học 10 Cánh diều cấu trúc mới
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(3698 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)