SỞ GDĐT BẮC NINH
ĐỀ THI THỬ TN TRUNG HỌC PHỔ THÔNG LẦN 1 THPT HÀM LONG NĂM HỌC 2022-2023
(Đề thi có 04 trang) Môn: HOÁ HỌC
(40 câu trắc nghiệm)
Thời gian: 50 phút (không tính thời gian phát đề) Mã đề 001
Cho nguyên tử khối: H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; P = 31; S = 32; Cl =
35,5; Br = 80; K = 39; Ca = 40; Fe = 56; Cu = 64; Zn = 65; Ag = 108; I = 127; Ba = 137.
Câu 1: Cho khí CO (dư) đi vào ống sứ nung nóng đựng hỗn hợp X gồm Al2O3, MgO, Fe3O4, CuO thu
được chất rắn Y. Cho Y vào dung dịch NaOH (dư), khuấy kĩ, thấy còn lại phần không tan Z. Giả sử các
phản ứng xảy ra hoàn toàn. Phần không tan Z gồm
A. MgO, Fe3O4, Cu. B. Mg, Fe, Cu.
C. Mg, Al, Fe, Cu. D. MgO, Fe, Cu.
Câu 2: Cho tất cả các đồng phân mạch hở, có cùng công thức phân tử C2H4O2 lần lượt tác dụng với: Na,
NaOH, NaHCO3. Số phản ứng xảy ra là A. 4. B. 2. C. 5. D. 3.
Câu 3: Nguyên tố X có cấu hình electron lớp ngoài cùng là … 3s23p5. Cấu hình electron của ion được tạo thành từ X là:
A. 1s22s22p63s23p6. B. 1s22s22p63s2. C. 1s22s22p6.
D. 1s22s22p63s23p4.
Câu 4: Chất nào sau đây là chất điện li yếu? A. CH3COOH. B. NaCl. C. KOH. D. KNO3.
Câu 5: Đốt một este hữu cơ X thu được 13,2 gam CO2 và 5,4 gam H2O. X thuộc loại:
A. Không no, không rõ số chức.
B. Vòng, đơn chức.
C. No, hai chức.
D. No, đơn chức.
Câu 6: Thủy phân triolein trong môi trường axit sản phẩm là ?
A. axit oleic và etilenglicol.
B. axit oleic và glixerol.
C. axit linolec và glixerol.
D. axit stearic và glixerol.
Câu 7: Cho 498,4 gam chất béo trung tính xà phòng hóa đủ với 840 ml dung dịch NaOH 2M. Tính khối
lượng xà phòng thu được? A. 529,46 gam. B. 562,14 gam. C. 514,08 gam. D. 524,68 gam.
Câu 8: Sản phẩm của phản ứng thủy phân dầu chuối trong môi trường axit là?
A. CH3COOH và (CH3)2CHCH2OH.
B. HCOOH và (CH3)2CH(CH2)2OH.
C. C2H5COOH và (CH3)2CH(CH2)2OH.
D. CH3COOH và (CH3)2CH(CH2)2OH.
Câu 9: Công thức tổng quát của ankin là
A. CnH2n (n ≥ 2).
B. CnH2n+2 (n ≥ 1).
C. CnH2n-2 (n ≥ 3).
D. CnH2n-2 (n ≥ 2).
Câu 10: Cho phản ứng: (X) + H2O ⇌ C2H5COOH + CH3OH. Tên gọi của (X) là ?
A. etyl propionat. B. metyl fomat. C. etyl axetat.
D. metyl propionat.
Câu 11: Tìm dung dịch B có pH > 7, tác dụng được với dung dịch K2SO4 tạo kết tủa: A. BaCl2. B. NaOH. C. H2SO4. D. Ba(OH)2.
Câu 12: Có thể phân biệt 3 lọ mất nhãn chứa: HCOOH; CH3COOH; C2H5OH với hóa chất nào dưới đây
A. NaOH. B. Cu(OH)2/OH-. C. Na. D. dd AgNO3/NH3.
Câu 13: Tên quốc tế của hợp chất có công thức CH3CH(C2H5)CH(OH)CH3 là
A. 2-etyl butan-3-ol.
B. 4-etyl pentan-2-ol.
C. 3-etyl hexan-5-ol.
D. 3-metyl pentan-2-ol.
Câu 14: Dãy gồm các chất đều tác dụng với ancol etylic là
A. HBr (t°), Na, CuO (t°), CH3COOH (xúc tác).
B. Ca, CuO (t°), C6H5OH (phenol), HOCH2CH2OH.
C. NaOH, K, MgO, HCOOH (xúc tác).
D. Na2CO3, CuO (t°), CH3COOH (xúc tác), (CH3CO)2O.
Câu 15: X là một anđehit no, mạch hở có công thức (C2H3O)n. Công thức cấu tạo của X là: A. CH2(CHO)2. B. C2H4(CHO)2. C. C3H6(CHO)3. D. C4H8(CHO)2.
Câu 16: Hấp thụ hoàn toàn 0,336 lít khí CO2 (đktc) vào 200 ml dung dịch gồm NaOH 0,1M và KOH
0,1M thu được dung dịch X. Cô cạn toàn bộ dung dịch X thu được bao nhiêu gam chất rắn khan. A. 2,31 gam. B. 2,58 gam. C. 2,44 gam. D. 2,22 gam.
Câu 17: Hòa tan hoàn toàn 20 gam hỗn hợp Mg và Fe bằng dung dịch HCl dư. Sau phản ứng thu được
11,2 lít khí (đktc) và dung dịch X. Cô cạn dung dịch X thì thu được bao nhiêu gam muối khan? A. 71,0g. B. 90,0g. C. 55,5g. D. 91,0g.
Câu 18: Hấp thụ hết 4,48 lít khí CO2 (đktc) vào dung dịch chứa x mol KOH và y mol K2CO3, thu được
200 ml dung dịch X. Cho từ từ đến hết 100 ml dung dịch X vào 300 ml dung dịch HCl 0,5M, thu được
2,688 lít khí (đktc). Mặt khác, cho 100 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư, thu được 39,4
gam kết tủa. Giá trị của x là A. 0,10. B. 0,05. C. 0,20. D. 0,30.
Câu 19: Hòa tan 16,8 gam Fe bằng dung dịch HNO3 loãng dư, sinh ra V lít khí NO (sản phẩm khử duy
nhất, ở đktc). Giá trị của V là A. 4,48. B. 3,36. C. 2,24. D. 6,72.
Câu 20: Có bao nhiêu đồng phân cấu tạo có công thức phân tử C5H12?
A. 3 đồng phân.
B. 5 đồng phân.
C. 4 đồng phân.
D. 6 đồng phân.
Câu 21: Hòa tan hoàn toàn hỗn hợp gồm 0,12 mol FeS2 và a mol Cu2S vào axit HNO3 (vừa đủ) thu được
dung dịch X (chỉ chứa 2 muối sunfat) và khí duy nhất NO (không còn sản phẩm khử khác). Cho dung
dịch X tác dụng với dung dịch BaCl2 dư thu được m gam kết tủa. Giá tri m là A. 46,6. B. 65,24. C. 69,9. D. 23,3.
Câu 22: Cho các hợp chất hữu cơ: C2H2; C2H4; CH2O; CH2O2 (mạch hở); C3H4O2 (mạch hở, đơn chức).
Biết C3H4O2 không làm chuyển màu quỳ tím ẩm. Số chất tác dụng được với dung dịch AgNO3 trong NH3 tạo ra kết tủa là A. 3. B. 4. C. 2. D. 5.
Câu 23: Trộn 250 ml dung dịch hỗn hợp gồm HCl 0,08 mol/lít và H2SO4 0,01 mol/lít với 250 ml dung
dịch NaOH nồng độ x mol/ lít, được 500 ml dung dịch có pH = 12. Giá trị của x là A. 0,1. B. 0,09. C. 0,11. D. 0,12.
Câu 24: Đun nóng 10,56 gam este có công thức C4H8O2 với H2SO4 loãng cho đến khi phản ứng thủy phân
hoàn toàn, trung hòa hỗn hợp thu được bằng dung dịch NaOH dư, tiếp tục cho AgNO3/NH3 dư vào hỗn
hợp dung dịch, đun nóng thì thu m gam kết tủa. Tính m ? A. 38,88 gam. B. 25,92 gam. C. 12,96 gam. D. 51,84 gam.
Câu 25: Cho phản ứng hoá học: H2S + 4Cl2 + 4H2O → H2SO4 + 8HCl. Vai trò của H2S trong phản ứng là
A. Môi trường.
B. Vừa oxi hóa, vừa khử.
C. Chất oxi hóa. D. Chất khử.
Câu 26: Dãy gồm các chất trong phân tử có liên kết ion là
A. Na2SO4, K2S, KHS, NH4Cl.
B. KHS, Na2S, NaCl, HNO3.
C. Na2SO4, KHS, H2S, SO2.
D. H2O, K2S, Na2SO3, NaHS.
Câu 27: C3H6O2 có hai đồng phân đều tác dụng được với NaOH, không tác dụng với Na. Công thức cấu
tạo của hai đồng phân đó là :
A. CH3-CH(OH)-CHO và CH3-CO-CH2OH.
B. CH3-CH2-COOH và HCOO-CH2-CH3.
C. CH3-CH2-COOH và CH3-COO-CH3.
D. CH3-COO-CH3 và HCOO-CH2-CH3.
Câu 28: Đun nóng 2,9 gam hỗn hợp A gồm C2H2 và H2 trong bình kín với xúc tác thích hợp, sau phản
ứng được hỗn hợp khí X. Dẫn hỗn hợp X qua bình đựng dung dịch Br2 dư thấy bình tăng lên 0,7 gam và
còn lại hỗn hợp khí Y. Đốt cháy hỗn hợp khí Y thu được 4,4 gam CO2. Thể tích của hỗn hợp khí Y ở đktc là: A. 17,68 lít. B. 8,96 lít. C. 11,2 lít. D. 6,72 lít.
Câu 29: Cho một este no, đơn chức có %C = 54,55%. Công thức phân tử của este là? A. C4H6O2. B. C3H6O2. C. C2H4O2. D. C4H8O2.
Câu 30: Ảnh hưởng của nhóm -OH đến gốc C6H5- trong phân tử phenol thể hiện qua phản ứng giữa phenol với
A. Na kim loại.
B. dung dịch NaOH.
C. H2 (Ni, nung nóng). D. nước Br2.
Câu 31: Hiđrocacbon C4H8 có bao nhiêu đồng phân anken? A. 4. B. 1. C. 2. D. 3.
Câu 32: Hiện tượng quan sát được khi cho Cu vào dung dịch HNO3 đặc là
A. dung dịch không đổi màu và có khí màu nâu đỏ thoát ra.
B. dung dịch chuyển sang màu nâu đỏ,có khí màu xanh thoát ra.
C. dung dịch chuyển sang màu xanh và có khí không màu thoát ra.
D. dung dịch chuyển sang màu xanh và có khí màu nâu đỏ thoát ra.
Câu 33: Nhệt độ sôi được sắp xếp theo chiều tăng dần là?
A. CH3COOH < HCOOCH3 < C2H5OH < C2H6.
B. C2H5OH < C2H6 < HCOOCH3 < CH3COOH.
C. C2H6 < HCOOCH3 < C2H5OH < CH3COOH.
D. C2H6 < C2H5OH < HCOOCH3 < CH3COOH.
Câu 34: Chất có thể dùng để làm khô khí NH3 là A. CaO. B. FeSO4 khan. C. P2O5. D. H2SO4 đặc.
Câu 35: Cho hỗn hợp tất cả các đồng phân mạch hở của C4H8 tác dụng với H2O (H+, t°) thu được tối đa
bao nhiêu sản phẩm cộng? A. 4. B. 3. C. 1. D. 2.
Câu 36: Nhiệt phân hoàn toàn 34,65 gam hỗn hợp gồm KNO3 và Cu(NO3)2, thu được hỗn hợp khí X (tỉ
khối của X so với khí hiđro bằng 18,8). Khối lượng Cu(NO3)2 trong hỗn hợp ban đầu là A. 8,60 gam. B. 9,40 gam. C. 20,50 gam. D. 11,28 gam.
Câu 37: Thành phần các nguyên tố trong hợp chất hữu cơ
A. thường có C, H hay gặp O, N, sau đó đến halogen, S, P.
B. bao gồm tất cả các nguyên tố trong bảng tuần hoàn.
C. gồm có C, H và các nguyên tố khác.
D. nhất thiết phải có cacbon, thường có H, hay gặp O, N sau đó đến halogen, S, P.
Câu 38: Đốt cháy hết 1 mol hiđrocacbon X tạo ra 5 mol CO2. Khi cho X phản ứng với Cl2 (as) tạo ra một
dẫn xuất monoclo. Tên gọi của X là A. iso butan. B. iso pentan. C. pentan. D. neo pentan.
Câu 39: Cho phản ứng: C4H8O2 + NaOH → muối + ancol bậc 2. Công thức cấu tạo của C4H8O2 là ? A. CH3COOC2H5. B. C2H5COOCH3.
C. HCOO(CH2)2CH3. D. HCOOCH(CH3)2.
Câu 40: Dãy gồm các chất đều tác dụng được với NaOH là?
A. C2H5Cl, CH3COOH, CH3COOC2H5, C6H5OH.
B. C2H4, CH3COOH, CH3COOC2H5, C6H5OH.
C. C2H5Cl, CH3COOH, CH3COOC2H5, C2H5OH.
D. C2H5Cl, CH3CHO, CH3COOC2H5, C6H5OH.
Đề thi thử THPTQG Sở Giáo Dục Và Đào Tạo Hà Nội
Câu 1: Kim loại nào sau đây có thể tan trong dung dịch HNO3 đặc nguội ? A. Cr. B. Cu. C. Fe. D. Al.
Câu 2: Cho các chất sau: CH3COOH,C2H5OH, C2H6, C2H5Cl. Chất có nhiệt độ sôi thấp nhất là A. CH3COOH. B. C2H5OH C. C2H6 D. C2H5Cl
Câu 3: Chất nào sau đây vừa tác dụng với dung dịch HCl, vừa tác dụng với dung dịch NaOH? A. Al(OH)3. B. Al2(SO4)3. C. KNO3. D. CuCl2.
Câu 4: Phenol không có khả năng phản ứng với chất nào sau đây? A. Dung dịch NaCl. B. Nước Br2.
C. Dung dịch NaOH. D. Kim loại Na.
Câu 5: Tính chất nào sau đây không phải tính chất vật lí chung của kim loại? A. Dẫn nhiệt. B. Cứng. C. Dẫn điện. D. Ánh kim.
Câu 6: “Nước đá khô” không nóng chảy mà dễ thăng hoa nên được dùng để tạo môi trường
lạnh và khô, rất tiện cho việc bảo quản thực phẩm. “ Nước đá khô” là A. CO rắn. B. SO2 rắn. C. CO2 rắn. D. H2O rắn
Câu 7: Phương trình hóa học nào sau đây không đúng? A. B. C. D.
Câu 8: Cho các chất sau: but – 2- en; propen; etan; propin. Chất có đồng phân hình học là A. but – 2- en. B. etan. C. propin. D. propen.
Câu 9: Nhỏ vài giọt dung dịch chứa chất X vào ống nghiệm đựng dung dịch hồ tinh bột thấy
xuất hiện kết tủa màu xanh.Chất X là A. Cl2. B. I2. C. Br2. D. HI.
Câu 10: Chất nào sau đây không phải là hợp chất hữu cơ? A. CH4 B. CH3COOH. C. HCN. D. HCOONa.
Câu 11: Cho m gam hỗn hợp X gồm Mg và Al vào dung dịch HCl dư thu được 8,96 lít khí.
Mặt khác, cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể
tích khí đo ở đktc. Giá trị của m là A. 7,80. B. 14,55. C. 6,45. D. 10,2.
Câu 12: Thêm từ từ V ml dung dịch Ba(OH)2 0,1M vào 120 ml dung dịch HNO3 1M, cô cạn
dung dịch sau phản ứng, làm khô thu được 17,37 gam chất rắn khan. Giá trị của V là A. 700. B. 500. C. 600. D. 300.
Câu 13: Phát biểu nào sau đây không đúng? 1
A. Tính dẫn điện của kim loại bạc tốt hơn kim loại đồng.
B. Các kim loại kiềm ( nhóm IA) đều có trúc mạng tinh thể lập phương tâm khối.
C. Từ P và HNO3 đặc, nóng có thể điều chế được H3PO4.
D. Có thể dùng CO để làm khô khí HCl có lẫn hơi nước.
Câu 14: Cho m gam hỗn hợp X gồm CuO, Fe2O3, FeO tác dụng vừa đủ với 100ml dung dịch
chứa H2SO4 1M và HCl 1M. Thể tích (ở đktc) hỗn hợp khí CO và H2 tối thiểu cần dùng để
khử hoàn toàn m gam hỗn hợp X là A. 3,36 lít. B. 6,72 lít. C. 1,12 lít. D. 4,48 lít.
Câu 15: Dung dịch nào sau đây có khả năng làm nhạt màu dung dịch KMnO4 trong môi trường H2SO4 ? A. Fe2(SO4)2. B. CuSO4. C. FeSO4. D. Fe(NO3)3
Câu 16: Cho các phát biểu sau:
(1) Để một miếng gang ( hợp kim sắt – cacbon) ngoài không khí ẩm, sẽ xảy ra ăn mòn điện hóa.
(2) Kim loại cứng nhất là W (vonfam).
(3) Hòa tan Fe3O4 bằng dung dịch HCl vừa đủ, thu được dung dịch chứa hai muối.
(4) Khi điện phân NaCl nóng chảy (điện cực trơ), tại catot xảy ra sự oxi hóa ion Na+.
(5) Không thể dùng khí CO2 để dập tắt đám cháy magie hoặc nhôm. Số phát biểu đúng là A. 4. B. 3. C. 1. D. 2.
Câu 17: Cho các phát biểu sau:
(1) Glucozơ không tham gia phản ứng công hiđro ( xúc tác Ni, đun nóng).
(2) Metyl amin làm quỳ tím ẩm đổi sang màu xanh.
(3) Đa số các polime không tan trong các dung môi thông thường.
(4) Muối natri hoặc kali của axit béo được dùng để sản xuất xà phòng. Các phát biểu đúng là A. (1), (2), (3). B. (1), (2), (4). C. (1), (3), (4). D. (2), (3), (4).
Câu 18: Trong công nghiệp, nhôm được sản xuất bằng phương pháp
A. điện phân nóng chảy AlCl3.
B. điện phân nóng chảy Al2O3.
C. dùng CO khử Al2O3 ở nhiệt độ cao.
D. dùng Mg khử Al3+ trong dung dịch.
Câu 19: Tơ nitrin dai, bền với nhiệt, giữ nhiệt tốt, thường được dùng để dệt vải và may quần
áo ẩm. Trùng hợp chất nào sau đây tạo thành polime dùng để sản xuất tơ nitron? A. CH2=CH-CN. B. CH2=CH-CH3. C. H2N- [CH2]5-COOH. D. H2N- [CH2]6-NH2. 2
Câu 20: Tiến hành thí nghiệm với các chất hữu cơ X, Y, Z, T đều trong dung dịch. Kết quả được ghi ở bảng sau: Mẫu thử Thuốc thử Hiện tượng X Nước brom Có kết tủa trắng Y,Z Cu(OH)2
Tạo thành dung dịch màu xanh lam Y,T
Dung dịch AgNO3 trong NH3 , đun nóng
Tạo thành kết tủa màu trắng bạc
Các chất X, Y, Z, T có thể lần lượt là
A. Phenol, glucozo, glixerol, etyl axetat.
B. Anilin, glucozo, glixerol, etyl fomat.
C. Phenol, saccarozo, lòng trắng trứng, etyl fomat
D. Glixerol, glucozo, etyl fomat, metanol.
Câu 21: Phát biểu nào sau đây là đúng?
A. Trong phân tử peptit mạch hở chứa n gốc α – amino axit (chứa 1 nhóm NH2, 1 nhóm
COOH) có (n-1) liên kết peptit.
B. Trong phân tử các α – amino axit chỉ có 1 nhóm amino.
C. Tất cả các peptit đều ít tan trong nước.
D. Tất cả các dung dịch amino axit đều không làm đổi màu quỳ tím.
Câu 22: Cho các chất: NaHCO3, CO, Al(OH)3, Fe(OH)3, CO2, NH4Cl. Số chất tác dụng được
với dung dịch NaOH ở nhiệt độ thường là A. 5 B. 2 C. 3 D. 4
Câu 23: Khi cho kim loại sắt vào lượng dư dung dịch chứa chất X, sau khi kết thúc phản ứng
thu được sản phẩm là muối sắt (II). Chất X có công thức hóa học là A. H2SO4 đặc, nóng. B. HNO3. C. FeCl3. D. MgSO4.
Câu 24: Isoamyl axetat là một este có mùi chuối chín, công thức cấu tạo thu gọn của este này là
A. CH3COOCH2CH2CH(CH3)2. B. C2H5COOCH2CH2CH(CH3)2. C. CH3COOCH(CH3)2. D. CH3COOCH3.
Câu 25: Dung dịch chất nào sau đây không làm đổi màu quỳ tím thành đỏ? A. CH3COOH. B. HOCH2COOH. C. HOOCC3H5(NH2)COOH. D. H2NCH2COOH.
Câu 26: Cho dãy các chất sau: etilen, hexan, hex-1-in, anilin, cumen, but-1-in, benzen, stiren,
metyl metacrylat. Số chất trong dãy trên tác dụng được với nước brom ở điều kiện thường là A. 5. B. 7. C. 8. D. 6. 3
Câu 27: Chất hữu cơ X có công thức phân tử C8H15O4N. Khi cho chất X tác dụng với dung
dịch NaOH, đun nóng, thu được sản phẩm gồm chất Y, C2H6O và CH4O. Chất Y là muối natri
của α – amino axit Z (chất Z có cấu tạo mạch hở và có mạch cacbon không phân nhánh). Số
công thức cấu tạo của phù hợp của X là A. 1. B. 2. C. 3. D. 4.
Câu 28: Cracking khí butan một thời gian thì thu được hỗn hợp khí X gồm CH4, C3H6, C2H6,
C2H4 và C4H10 dư. Cho toàn bộ hỗn hợp X đi qua dung dịch nước Br2 dư thì khối lượng bình
brom tăng lên 0,91 gam và có 4 gam Br2 phản ứng, đồng thời có hỗn hợp khí Y thoát ra khỏi
bình Br2 (thể tích của Y bằng 54,545% thể tích của X). Để đốt cháy hoàn toàn hỗn hợp Y cần
vừa đủ V lít O2 (ở đktc). Giá trị của V là A. 2,184. B. 4,368. C. 2,128. D. 1,736.
Câu 29: Cho từ từ dung dịch HCl vào dung dịch chứa a mol Ba(AlO2)2 và b mol Ba(OH)2. Số
mol Al(OH)3 tạo thành phụ thuộc vào số mol HCl được biểu diễn bằng đồ thị hình bên. Tỉ lệ a:b tương ứng là A. 9:4. B. 4:9. C. 7:4. D. 4:7.
Câu 30: Cho hơi nước đi qua than nóng đỏ, sau phản ứng thu được V lít (ở đktc) hỗn hợp khí
X gồm CO, CO2 và H2. Dẫn toàn bộ hỗn hợp X qua dung dịch Ca(OH)2 thu được 2 gam kết
tủa và khối lượng dung dịch sau phản ứng giảm 0,68 gam so với khối lượng dung dịch
Ca(OH)2 ban đầu; khí còn lại thoát ra gồm CO và H2 có tỉ khối hơi so với H2 là 3,6. Giá trị của V là A. 2,688. B. 3,136. C. 2,912. D. 3,360.
Câu 31: Cho m gam bột Fe vào 200 ml dung dịch chứa HCl 0,4M và Cu(NO3)2 0,2M. Lắc
đều cho các phản ứng xảy ra hoàn toàn, sau phản ứng thu được hỗn hợp chất rắn có khối
lượng bằng 0,75m gam và V lít (ở đktc) khí NO (sản phẩm khử duy nhất của N+5). Giá trị của m và V lần lượt là: A. 3,84 và 0,448. B. 5,44 và 0,896. C. 5,44 và 0,448. D. 9,13 và 2,24.
Câu 32: Đốt cháy hoàn toàn m gam photpho trong oxi dư. Cho toàn bộ sản phẩm tạo thành
vào 500 ml dung dịch chứa hỗn hợp NaOH 0,1M và KOH 0,2M đến khi các phản ứng xảy ra 4
SỞ GD & ĐT TỈNH BẮC NINH
THI THỬ THPT QUỐC GIA LẦN 1 THPT CHUYÊN BẮC NINH NĂM HỌC: 2018 - 2019 (Đề gồm 08 trang) Môn: Hóa Học
(Thời gian làm bài: 50 phút)
Họ, tên thí sinh:.......................................................................
Số báo danh:............................................................................
Câu 1: Thủy phân hoàn toàn 4,34 gam tripeptit mạch hở X (được tạo nên từ hai α-
amino axit có công thức dạng H2NCxHyCOOH) bằng dung dịch NaOH dư, thu được
6,38 gam muối. Mặt khác thủy phân hoàn toàn 4,34 gam X bằng dung dịch HCl dư,
thu được m gam muối. Giá trị của m là A. 6,53. B. 8,25 C. 7,25. D. 7,52.
Câu 2: Este Z đơn chức, mạch hở được tạo ra thành từ axit X v{ ancol Y. Đốt chạy
hoàn toán 2,15 gam Z, thu được 0,1 mol CO2 và 0,075 mol H2O. Mặt khác, cho 2,15
gam Z tác dụng vừa đủ với dung dịch KOH, thu được 2,75 gam muối. Công thức của X và Y lần lượt là A. CH3COOH và C3H5OH. B. C2H3COOH và CH3OH. C. HCOOH và C3H7OH. D. HCOOH và C3H5OH
Câu 3: Tiến hành thí nghiệm với các dung dịch X, Y, Z và T. Kết quả được ghi ở bảng sau: Mẫu thử Thuốc thử Hiện tượng Y Quỳ tím Quỳ chuyển sang màu xanh X, Z Dung dịch AgNO3 trong Tạo kết tủa Ag NH3, đun nóng T Dung dịch Br2 Kết tủa trắng Z Cu(OH)2 Tạo dung dịch màu xanh lam X, Y, Z, T lần lượt là:
A. Etyl fomat, lysin, glucozơ, axit acrylic.
B. Etyl fomat, lysin, glucozơ, phenol.
C. Glucozơ, lysin, etyl fomat, anilin.
D. Lysin, etyl fomat, glucozơ, anilin.
Câu 4: Nung nóng hỗn hợp chứa các chất có cùng số mol gồm Al(NO3)3, NaHCO3,
Fe(NO3)3, CaCO3 đến khi khối lượng không đổi, thu được chất rắn X. Hòa tan X vào
nước dư, thu được dung dịch Y và chất rắn Z. Thổi luồng khí CO (dùng dư) qua chất
rắn Z, nung nóng thu được chất rắn T.
Các phản ứng xảy ra hoàn toàn. Nhận định nào sau đây là đúng?
A. Nhỏ dung dịch HCl vào dung dịch Y, thấy khí không màu thoát ra.
B. Nhỏ dung dịch HCl vào dung dịch Y, thấy xuất hiện ngay kết tủa.
C. Chất rắn T chứa một đơn chất v{à hai hợp chất.
D. Chất rắn T chứa một đơn chất và một hợp chất.
Câu 5: PVC là chất rắn vô định hình, c|ch điện tốt, bền với axit, được dùng làm vật
liệu cách điện, ống dẫn nước, vải che mưa,... PVC được tổng hợp trực tiếp từ monome nào sau đây? A. Acrilonitrin. B. Vinyl axetat. C. Propilen. D. Vinyl clorua.
Câu 6: Hòa tan hoàn toàn hỗn hợp X gồm Fe(NO3)2, Fe3O4, MgO và Mg trong dung
dịch chứa 9,22 mol HCl loãng. Sau khi các phản ứng xảy ra hoàn toàn thu được dung
dịch Y chỉ chứa 463,15 gam muối clorua và 29,12 lít (đktc) khí Z gồm NO và H2 có tỉ
khối so với H2 là 69/13. Thêm NaOH dư vào dung dịch Y, sau phản ứng thấy xuất
hiện kết tủa T. Nung T trong không khí đến khối lượng không đổi được 204,4 gam
chất rắn M. Biết trong X, oxi chiếm 29,68% theo khối lượng. Phần trăm khối lượng
MgO trong X gần nhất với giá trị nào dưới đây? A. 13,33%. B. 33,33%. C. 20,00%. D. 6,80%.
Câu 7: Hỗn hợp khí E gồm một amin bậc III no, đơn chức, mạch hở và hai ankin X, Y (MX2 (đktc), thu
được hỗn hợp F gồm CO2, H2O và N2. Dẫn toàn bộ F qua bình đựng dung dịch KOH
đặc, dư đến phản ứng hoàn toàn thấy khối lượng bình bazơ nặng thêm 20,8 gam. Số
cặp công thức cấu tạo ankin X, Y thỏa mãn là A. 1. B. 2. C. 3. D. 4.
Câu 8: Cho các cặp chất sau: (1). Khí Br2 và khí O2.
(5) Si và dung dịch NaOH loãng
(2). Khí H2S và dung dịch FeCl3.
(6). Dung dịch KMnO4 và khí SO2.
(3). Khí H2S và dung dịch Pb(NO3)2. (7). Hg và S. (4). CuS và dung dịch HCl.
(8). Khí Cl2 và dung dịch NaOH.
Số cặp chất xảy ra phản ứng hóa học ở nhiệt độ thường l{ A. 8. B. 5. C. 7. D. 6.
Câu 9: Thực hiện các thí nghiệm sau:
(1) Cho hỗn hợp gồm 2a mol Na và a mol Al vào lượng nước dư.
(2) Cho a mol bột Cu vào dung dịch chứa a mol Fe2(SO4)3.
(3) Cho dung dịch chứa a mol KHSO3 vào dung dịch chứa a mol KHCO3.
(4) Cho dung dịch chứa a mol BaCl2 vào dung dịch chứa a mol CuSO4.
(5) Cho dung dịch chứa a mol Fe(NO3)2 vào dung dịch chứa a mol AgNO3.
(6) Cho a mol Na2O vào dung dịch chứa a mol CuSO4.
(7) Cho hỗn hợp Fe2O3 và Cu (tỉ lệ mol tương ứng 2:1) vào dung dịch HCl dư.
Sau khi kết thúc thí nghiệm, số trường hợp thu được dung dịch chứa hai muối là A. 4. B. 1. C. 3. D. 2.
Câu 10: Trước những năm 50 của thế kỷ XX, công nghiệp tổng hợp hữu cơ dựa trên
nguyên liệu chính là axetilen. Ngày nay, nhờ sự phát triển vượt bậc của công nghệ
khai thác và chế biến dầu mỏ, etilen trở thành nguyên liệu rẻ tiền, tiện lợi hơn nhiều so
với axetilen. Công thức phần tử của etilen là A. CH4. B. C2H6. C. C2H4. D. C2H2.
Câu 11: Thủy phân hoàn toàn m gam hỗn hợp hai este đơn chức, mạch hở E, F (ME <
MF) trong 700 ml dung dịch KOH 1M thu được dung dịch X và hỗn hợp Y gồm 2
ancol là đồng đẳng liên tiếp. Thực hiện t|ch nước Y trong H2SO4 đặc ở 140°C thu
được hỗn hợp Z. Trong Z tổng khối lượng của các ete là 8,04 gam (hiệu suất ete hóa
của các ancol đều là 60%). Cô cạn dung dịch X được 53,0 gam chất rắn. Nung chất
rắn này với CaO cho đến khi phản ứng xảy ra hoàn toàn, thu được 6,72 lít hỗn hợp khí
T (đktc). Cho các phát biểu sau:
(1) Chất F tham gia phản ứng tráng bạc (2) Khối lượng của E trong hỗn hợp là 8,6 gam
(3) Khối lượng khí T là 2,55 gam (4) Tổng số nguyên tử trong F là 12
(5) Trong Z có chứa ancol propylic Số phát biểu đúng là: A. 4. B. 2. C. 3. D. 5.
Câu 12: Thủy phân m gam saccarozơ trong môi trường axit với hiệu suất 90%, thu
được sản phẩm chứa 10,8 gam glucozơ. Giá trị của m là A. 22,8. B. 17,1. C. 18,5. D. 20,5.
Câu 13: Etanol là chất có tác động đến thần kinh trung ương. Khi hàm lượng etanol
trong màu tăng cao sẽ có hiện tượng nôn, mất tỉnh táo và có thể dẫn đến tử vong. Tên gọi kh|c của etanol là A. ancol etylic. B. axit fomic. C. etanal. D. phenol.
Câu 14: Chất X (có M = 60 và chứa C, H, O). Chất X phản ứng được với Na, NaOH
và NaHCO3. Tên gọi của X là
A. ancol propylic. B. metyl fomat C. axit fomic. D. axit axetic.
Câu 15: Xà phòng hóa chất nào sau đây thu được glixerol? A. Tristearin.
B. Benzyl axetat. C. Metyl axetat. D. Metyl fomat.
Câu 16: Cho hỗn hợp gồm 1,68 gam Fe và 2,88 gam Cu vào 400 mL dung dịch chứa
hỗn hợp gồm H2SO4 0,75M và NaNO3 0,3M. Sau khi các phản ứng xảy ra hoàn toàn,
thu được dung dịch X và khí NO (sản phẩm khử duy nhất). Cho V (mL) dung dịch
NaOH 1,0M vào dung dịch X thì lượng kết tủa thu được là lớn nhất. Gi| trị tối thiểu của V là A. 540. B. 360. C. 240. D. 420.
Câu 17: X là axit no, đơn chức, Y là axit không no, có một liên kết đôi C=C, có đồng
phân hình học và Z là este hai chức tạo X, Y và một ancol no (tất cả các chất đều
thuần chức, mạch hở). Đốt cháy hoàn toàn 9,52 gam E chứa X, Y và Z thu được 5,76
gam H2O. Mặt khác, 9,52 gam E có thể phản ứng tối đa với dung dịch chứa 0,12 mol
NaOH sản phẩm sau phản ứng có chứa 12,52 hỗn hợp các chất hữu cơ. Cho các phát
biểu liên quan tới bài toán gồm:
Document Outline
- Chương 1: Este - Lipit
- Chương 2: Cacbohiđrat
- Chương 3: Amin, Amino Axit Và Protein
- Chương 4: Polime Và Vật Liệu Polime
- Chương 5: Đại Cương Về Kim Loại
- Chương 6: Kim Loại Kiềm, Kim Loại Kiềm Thổ, Nhôm
- Chương 7: Sắt Và Một Số Kim Loại Quan Trọng
- Chương 8: Phân Biệt Một Số Chất Vô Cơ
- Chương 9: Hóa Học Và Vấn Đề Phát Triển Kinh Tế, Xã Hội, Môi Trường
- Tổng hợp lý thuyết vô cơ
- Tổng hợp lý thuyết hữu cơ
- Chương 1: Sự Điện Li
- Chương 2: Nitơ - Photpho
- Chương 3: Cacbon - Silic
- Chương 4: Đại Cương Về Hóa Học Hữu Cơ
- Chương 5: Hiđrocacbon No
- Chương 6: Hiđrocacbon Không No
- Chương 8: Dẫn Xuất Halogen - Ancol - Phenol
- Chương 9: Anđehit - Xeton - Axit cacboxylic
- Chương 1: Nguyên Tử
- Chương 2: Bảng Tuần Hoàn Các Nguyên Tố Hóa Học Và Định Luật Tuần Hoàn
- Chương 3: Liên Kết Hóa Học
- Chương 4: Phản Ứng Oxi Hóa Khử
- Chương 5: Nhóm Halogen
- Chương 6: Oxi - Lưu Huỳnh
- Chương 7: Tốc Độ Phản Ứng Và Cân Bằng Hóa Học
SỞ GD&ĐT AN GIANG
ĐỀ THI THỬ THPTQG LẦN 1 TRƯỜNG THPT CHUYÊN
NĂM HỌC 2020 – 2021 THOẠI NGỌC HẦU MÔN: HÓA HỌC
Thời gian làm bài: 50 phút; không kể thời gian phát đề
Câu 1 (NB): Natri clorua là muối chủ yếu tạo ra độ mặn trong các đại dương. Công thức của natri clorua là A. NaClO. B. NaHCO3. C. NaNO3. D. NaCl.
Câu 2 (NB): Kim loại không tan được trong lượng dung dịch H2SO4 loãng là A. Mg. B. Cu. C. Fe. D. Na.
Câu 3 (TH): Đốt cháy hoàn toàn 1,08 gam Al bằng lượng dư khí O2, thu được m gam chất rắn. Giá trị của m là A. 8,16. B. 1,72. C. 4,08. D. 2,04.
Câu 4 (NB): Thí nghiệm nào dưới đây không xảy ra phản ứng?
A. Thêm AgNO3 vào dung dịch Fe(NO3)2.
B. Cho kim loại Fe vào dung dịch HCl đặc, nguội.
C. Cho kim loại Al vào dung dịch NaOH.
D. Cho Fe tác dụng với dung dịch ZnCl2.
Câu 5 (TH): Để khử mùi tanh của cá (gây ra do một số amin) ta có thể rửa cá với A. nước. B. giấm. C. nước muối. D. nước vôi trong.
Câu 6 (NB): Kim loại nào sau đây có nhiệt độ nóng chảy cao nhất, được sử dụng làm dây tóc bóng đèn? A. Hg. B. Cr. C. W. D. Li.
Câu 7 (NB): Glucozơ không tham gia phản ứng A. lên men. B. tráng gương. C. thủy phân. D. hiđro hóa.
Câu 8 (NB): Một số cơ sở sản xuất thực phẩm thiếu lương tâm đã dùng fomon (dung dịch nước của
fomanđehit) để bảo quản bún, phở. Công thức hóa học của fomanđehit là A. HCHO. B. CH3COOH. C. CH3OH. D. CH3CHO.
Câu 9 (NB): Polime thiên nhiên X màu trắng, dạng sợi, không tan trong nước, có nhiều trong thân cây
đay, gai, tre, nứa... Polime X là A. xenlulozơ. B. saccarozơ. C. cao su isopren. D. tinh bột.
Câu 10 (VD): Phải dùng bao nhiêu lít khí nitơ và bao nhiêu lít khí hiđro để điều chế 17 gam NH3? Biết
rằng hiệu suất chuyển hóa thành amoniac là 25%. Các thể tích khí đo được ở đktc.
A. 44,8 lít N2 và 134,4 lít H2.
B. 22,4 lít N2 và 67,2 lít H2.
C. 22,4 lít N2 và 134,4 lít H2.
D. 44,8 lít N2 và 67,2 lít H2.
Câu 11 (TH): Ở nhiệt độ thường, khí nitơ khá trơ về mặt hóa học. Nguyên nhân là do
A. trong phân tử N2, mỗi nguyên tử nitơ còn 1 cặp electron chưa tham gia liên kết.
B. nguyên tử nitơ có bán kính nhỏ.
C. nguyên tử nitơ có độ âm điện kém hơn oxi. 1
D. nguyên tử nitơ có độ âm điện kém hơn oxi.
Câu 12 (NB): Chất X có công thức cấu tạo CH3COOCH3. Tên gọi của X là A. metyl acrylat. B. metyl axetat. C. propyl fomat. D. etyl axetat.
Câu 13 (TH): Cho dung dịch chứa 3,6 gam hỗn hợp glucozơ và fructozơ phản ứng hoàn toàn với lượng
dư dung dịch AgNO3 trong NH3 thu được m gam bạc. Khối lượng bạc sinh ra là A. 1,08 gam. B. 4,32 gam. C. 2,16 gam. D. 1,62 gam.
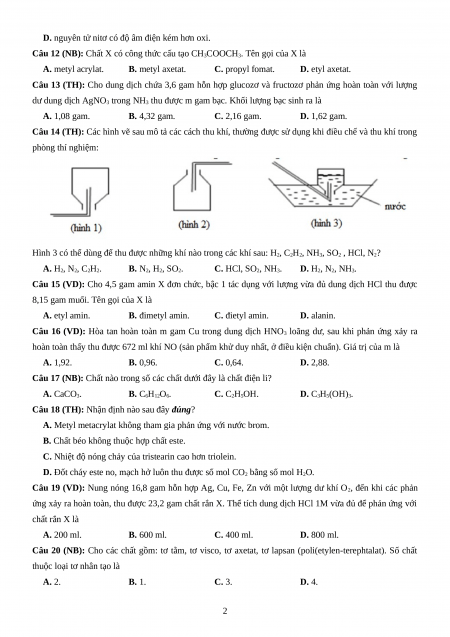
Câu 14 (TH): Các hình vẽ sau mô tả các cách thu khí, thường được sử dụng khi điều chế và thu khí trong phòng thí nghiệm:
Hình 3 có thể dùng để thu được những khí nào trong các khí sau: H2, C2H2, NH3, SO2 , HCl, N2? A. H2, N2, C2H2. B. N2, H2, SO2. C. HCl, SO2, NH3. D. H2, N2, NH3.
Câu 15 (VD): Cho 4,5 gam amin X đơn chức, bậc 1 tác dụng với lượng vừa đủ dung dịch HCl thu được
8,15 gam muối. Tên gọi của X là A. etyl amin. B. đimetyl amin. C. đietyl amin. D. alanin.
Câu 16 (VD): Hòa tan hoàn toàn m gam Cu trong dung dịch HNO3 loãng dư, sau khi phản ứng xảy ra
hoàn toàn thấy thu được 672 ml khí NO (sản phẩm khử duy nhất, ở điều kiện chuẩn). Giá trị của m là A. 1,92. B. 0,96. C. 0,64. D. 2,88.
Câu 17 (NB): Chất nào trong số các chất dưới đây là chất điện li? A. CaCO3. B. C6H12O6. C. C2H5OH. D. C3H5(OH)3.
Câu 18 (TH): Nhận định nào sau đây đúng?
A. Metyl metacrylat không tham gia phản ứng với nước brom.
B. Chất béo không thuộc hợp chất este.
C. Nhiệt độ nóng chảy của tristearin cao hơn triolein.
D. Đốt cháy este no, mạch hở luôn thu được số mol CO2 bằng số mol H2O.
Câu 19 (VD): Nung nóng 16,8 gam hỗn hợp Ag, Cu, Fe, Zn với một lượng dư khí O2, đến khi các phản
ứng xảy ra hoàn toàn, thu được 23,2 gam chất rắn X. Thể tích dung dịch HCl 1M vừa đủ để phản ứng với chất rắn X là A. 200 ml. B. 600 ml. C. 400 ml. D. 800 ml.
Câu 20 (NB): Cho các chất gồm: tơ tằm, tơ visco, tơ axetat, tơ lapsan (poli(etylen-terephtalat). Số chất
thuộc loại tơ nhân tạo là A. 2. B. 1. C. 3. D. 4. 2
Câu 21 (NB): Chất nào sau đây không hòa tan Cu(OH)2 ở nhiệt độ thường? A. Glucozơ. B. Tinh bột. C. Saccarozơ. D. Fructozơ.
Câu 22 (TH): Chất nào sau đây vừa tác dụng được với H2NCH2COOH vừa tác dụng với CH3NH2? A. NaOH. B. CH3OH. C. HCl. D. NaCl.
Câu 23 (NB): Chất nào sau đây có đồng phân hình học?
A. CH2 = CH – CH2 – CH3.
B. CH3 – CH = CH – CH2 – CH3.
C. CH3 – CH = C(CH3)2.
D. (CH3)2 – CH – CH = CH2.
Câu 24 (NB): Cho phản ứng hoá học: Fe + CuSO4 → FeSO4 + Cu. Trong phản ứng xảy ra
A. sự khử Fe2+ và sự oxi hoá Cu.
B. sự khử Fe2+ và sự khử Cu2+.
C. sự oxi hoá Fe và sự khử Cu2+.
D. sự oxi hoá Fe và sự oxi hoá Cu.
Câu 25 (VD): Đốt cháy hoàn toàn một hiđrocacbon X thu được 0,11 mol CO2 và 0,132 mol H2O. Khi X
tác dụng với khí clo (theo tỉ lệ số mol 1 : 1) thu được một sản phẩm hữu cơ duy nhất. Tên gọi của X là
A. 2,2-đimetylpropan. B. 2-metylpropan. C. etan. D. 2-metylbutan.
Câu 26 (TH): Cho các phát biểu sau:
(a) Độ dinh dưỡng của phân đạm được đánh giá theo phần trăm khối lượng nguyên tố nitơ.
(b) Fe2O3 phản ứng với axit HCl sẽ tạo ra 2 muối.
(c) Kim cương được dùng làm đồ trang sức, chế tạo mũi khoan, dao cắt thủy tinh.
(d) Amoniac được sử dụng để sản xuất axit nitric, phân đạm.
(e) Tính chất hóa học chung của kim loại là tính oxi hóa.
Số phát biểu đúng là A. 1. B. 2. C. 3. D. 4.
Câu 27 (VD): Hòa tan hết m gam P2O5 vào 400 gam dung dịch KOH 10% dư, sau phản ứng hoàn toàn cô
cạn dung dịch thu được 3,5m gam chất rắn. Giá trị nào sau đây gần nhất với giá trị của m? A. 13. B. 15. C. 14. D. 16.
Câu 28 (NB): “Hiệu ứng nhà kính” là hiện tượng làm cho trái đất nóng dần lên, do các bức xạ bị giữ lại
mà không thoát ra ngoài. Nguyên nhân chính gây ra hiệu ứng nhà kính là do sự gia tăng nồng độ của khí
X trong không khí. Khí X là A. CF4. B. O3. C. O2. D. CO2.
Câu 29 (VD): Đốt cháy hoàn toàn 2 amin no, đơn chức đồng đẳng liên tiếp, thu được hỗn hợp gồm khí và
hơi, trong đó tỉ lệ VCO2 : VH2O = 8 : 17. Công thức của 2 amin là
A. C4H9NH2 và C5H11NH2.
B. C2H5NH2 và C3H7NH2. C. CH3NH2 và C2H5NH2.
D. C3H7NH2 và C4H9NH2.
Câu 30 (VD): Cho hỗn hợp kim loại Mg, Zn, Fe vào dung dịch chứa AgNO3 và Cu(NO3)2. Sau khi phản
ứng xảy ra hoàn toàn thu được dung dịch X gồm 3 muối và chất rắn Y gồm 3 kim loại. Ba muối trong X là
A. Mg(NO3)2, Fe(NO3)3, AgNO3.
B. Mg(NO3)2, Zn(NO3)2, Fe(NO3)2. 3
C. Mg(NO3)2, Zn(NO3)2, Cu(NO3)2.
D. Mg(NO3)2, Zn(NO3)2, Fe(NO3)3.
Câu 31 (VD): Trong phòng thí nghiệm, etyl axetat được điều chế theo các bước:
Bước 1: Cho 1 ml ancol etylic, 1 ml axit axetic nguyên chất và 1 giọt axit sunfuric đặc vào ống nghiệm.
Bước 2: Lắc đều, đồng thời đun cách thủy 5 - 6 phút trong nồi nước nóng 65 - 70°C.
Bước 3: Làm lạnh rồi rót thêm vào ống nghiệm 2 ml dung dịch NaCl bão hòa. Cho các phát biểu sau:
(a) Có thể thay dung dịch axit sunfuric đặc bằng dung dịch axit sunfuric loãng.
(b) Để kiểm soát nhiệt độ trong quá trình đun nóng có thể dùng nhiệt kế.
(c) Dung dịch NaCl bão hòa được thêm vào ống nghiệm để phản ứng đạt hiệu suất cao hơn.
(d) Có thể thay dung dịch NaCl bão hòa bằng dung dịch HCl bão hòa.
(e) Để hiệu suất phản ứng cao hơn nên dùng dung dịch axit axetic 15%.
Số phát biểu đúng là A. 2. B. 3. C. 0. D. 1.
Câu 32 (VD): Cho 4,825 gam hỗn hợp bột Al và Fe (có tỉ lệ mol nAl : nFe = 3 : 2) vào 350 ml dung dịch
AgNO3 1M. Khuấy kĩ cho phản ứng xảy ra hoàn toàn, thu được m gam chất rắn. Giá trị của m là A. 37,8. B. 13,5. C. 35,1. D. 27,0.
Câu 33 (VDC): Hòa tan hoàn toàn 216,55 gam hỗn hợp KHSO4, và Fe(NO3)3 vào nước được dung dịch
X. Cho m gam hỗn hợp Y gồm Mg, Al, MgO, Al2O3 (trong đó mO = 64/205.mY) tan hết vào X. Sau khi
các phản ứng kết thúc, thu được dung dịch Z chỉ chứa muối trung hòa và 2,016 lít (đktc) hỗn hợp khí T có
tổng khối lượng 1,84 gam (trong đó H2 chiếm 4/9 về thể tích và nguyên tố oxi chiếm 8/23 khối lượng hỗn
hợp). Cho BaCl2 dư vào Z thu được 356,49 gam kết tủa. Giá trị của m là A. 20,5. B. 22,5. C. 20,0. D. 22,0.
Câu 34 (VD): Hỗn hợp chất rắn X gồm Ba(HCO3)2, KOH và Ba(OH)2 có tỉ lệ số mol lần lượt là 1 : 2 : 1.
Cho hỗn hợp X vào bình đựng nước dư, sau khi các phản ứng xảy ra hoàn toàn, chất còn lại trong bình (không kể H2O) là A. KHCO3. B. KOH. C. BaCO3, KHCO3. D. BaCO3, KOH.
Câu 35 (TH): Cho các nhận định sau:
(1) Kim loại mềm nhất là K, Rb, Cs (có thể dùng dao cắt được).
(2) Độ dẫn điện của nhôm (Al) tốt hơn của đồng (Cu).
(3) Những kim loại có độ dẫn điện tốt thì cũng dẫn nhiệt tốt.
(4) Crom (Cr) là kim loại cứng nhất trong các kim loại.
(5) Kim loại Na khử được ion Cu2+ trong dung dịch thành Cu.
Số nhận định đúng là A. 2. B. 3. C. 4. D. 5.
Câu 36 (TH): Cho các phát biểu sau:
(a) Chất béo là trieste của glixerol với axit béo. 4
SỞ GDĐT BẮC NINH
ĐỀ THI THỬ TN TRUNG HỌC PHỔ THÔNG LẦN 1 THPT HÀM LONG NĂM HỌC 2022-2023
(Đề thi có 04 trang) Môn: HOÁ HỌC
(40 câu trắc nghiệm)
Thời gian: 50 phút (không tính thời gian phát đề) Mã đề 001
Cho nguyên tử khối: H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; P = 31; S = 32; Cl =
35,5; Br = 80; K = 39; Ca = 40; Fe = 56; Cu = 64; Zn = 65; Ag = 108; I = 127; Ba = 137.
Câu 1: Cho khí CO (dư) đi vào ống sứ nung nóng đựng hỗn hợp X gồm Al2O3, MgO, Fe3O4, CuO thu
được chất rắn Y. Cho Y vào dung dịch NaOH (dư), khuấy kĩ, thấy còn lại phần không tan Z. Giả sử các
phản ứng xảy ra hoàn toàn. Phần không tan Z gồm
A. MgO, Fe3O4, Cu. B. Mg, Fe, Cu.
C. Mg, Al, Fe, Cu. D. MgO, Fe, Cu.
Câu 2: Cho tất cả các đồng phân mạch hở, có cùng công thức phân tử C2H4O2 lần lượt tác dụng với: Na,
NaOH, NaHCO3. Số phản ứng xảy ra là A. 4. B. 2. C. 5. D. 3.
Câu 3: Nguyên tố X có cấu hình electron lớp ngoài cùng là … 3s23p5. Cấu hình electron của ion được tạo thành từ X là:
A. 1s22s22p63s23p6. B. 1s22s22p63s2. C. 1s22s22p6.
D. 1s22s22p63s23p4.
Câu 4: Chất nào sau đây là chất điện li yếu? A. CH3COOH. B. NaCl. C. KOH. D. KNO3.
Câu 5: Đốt một este hữu cơ X thu được 13,2 gam CO2 và 5,4 gam H2O. X thuộc loại:
A. Không no, không rõ số chức.
B. Vòng, đơn chức.
C. No, hai chức.
D. No, đơn chức.
Câu 6: Thủy phân triolein trong môi trường axit sản phẩm là ?
A. axit oleic và etilenglicol.
B. axit oleic và glixerol.
C. axit linolec và glixerol.
D. axit stearic và glixerol.
Câu 7: Cho 498,4 gam chất béo trung tính xà phòng hóa đủ với 840 ml dung dịch NaOH 2M. Tính khối
lượng xà phòng thu được? A. 529,46 gam. B. 562,14 gam. C. 514,08 gam. D. 524,68 gam.
Câu 8: Sản phẩm của phản ứng thủy phân dầu chuối trong môi trường axit là?
A. CH3COOH và (CH3)2CHCH2OH.
B. HCOOH và (CH3)2CH(CH2)2OH.
C. C2H5COOH và (CH3)2CH(CH2)2OH.
D. CH3COOH và (CH3)2CH(CH2)2OH.
Câu 9: Công thức tổng quát của ankin là
A. CnH2n (n ≥ 2).
B. CnH2n+2 (n ≥ 1).
C. CnH2n-2 (n ≥ 3).
D. CnH2n-2 (n ≥ 2).
Câu 10: Cho phản ứng: (X) + H2O ⇌ C2H5COOH + CH3OH. Tên gọi của (X) là ?
A. etyl propionat. B. metyl fomat. C. etyl axetat.
D. metyl propionat.
Câu 11: Tìm dung dịch B có pH > 7, tác dụng được với dung dịch K2SO4 tạo kết tủa: A. BaCl2. B. NaOH. C. H2SO4. D. Ba(OH)2.
Câu 12: Có thể phân biệt 3 lọ mất nhãn chứa: HCOOH; CH3COOH; C2H5OH với hóa chất nào dưới đây
A. NaOH. B. Cu(OH)2/OH-. C. Na. D. dd AgNO3/NH3.
Câu 13: Tên quốc tế của hợp chất có công thức CH3CH(C2H5)CH(OH)CH3 là
A. 2-etyl butan-3-ol.
B. 4-etyl pentan-2-ol.
C. 3-etyl hexan-5-ol.
D. 3-metyl pentan-2-ol.
Câu 14: Dãy gồm các chất đều tác dụng với ancol etylic là
A. HBr (t°), Na, CuO (t°), CH3COOH (xúc tác).
B. Ca, CuO (t°), C6H5OH (phenol), HOCH2CH2OH.
C. NaOH, K, MgO, HCOOH (xúc tác).
D. Na2CO3, CuO (t°), CH3COOH (xúc tác), (CH3CO)2O.
Câu 15: X là một anđehit no, mạch hở có công thức (C2H3O)n. Công thức cấu tạo của X là: A. CH2(CHO)2. B. C2H4(CHO)2. C. C3H6(CHO)3. D. C4H8(CHO)2.
Câu 16: Hấp thụ hoàn toàn 0,336 lít khí CO2 (đktc) vào 200 ml dung dịch gồm NaOH 0,1M và KOH
0,1M thu được dung dịch X. Cô cạn toàn bộ dung dịch X thu được bao nhiêu gam chất rắn khan. A. 2,31 gam. B. 2,58 gam. C. 2,44 gam. D. 2,22 gam.
Câu 17: Hòa tan hoàn toàn 20 gam hỗn hợp Mg và Fe bằng dung dịch HCl dư. Sau phản ứng thu được
11,2 lít khí (đktc) và dung dịch X. Cô cạn dung dịch X thì thu được bao nhiêu gam muối khan? A. 71,0g. B. 90,0g. C. 55,5g. D. 91,0g.
Câu 18: Hấp thụ hết 4,48 lít khí CO2 (đktc) vào dung dịch chứa x mol KOH và y mol K2CO3, thu được
200 ml dung dịch X. Cho từ từ đến hết 100 ml dung dịch X vào 300 ml dung dịch HCl 0,5M, thu được
2,688 lít khí (đktc). Mặt khác, cho 100 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư, thu được 39,4
gam kết tủa. Giá trị của x là A. 0,10. B. 0,05. C. 0,20. D. 0,30.
Câu 19: Hòa tan 16,8 gam Fe bằng dung dịch HNO3 loãng dư, sinh ra V lít khí NO (sản phẩm khử duy
nhất, ở đktc). Giá trị của V là A. 4,48. B. 3,36. C. 2,24. D. 6,72.
Câu 20: Có bao nhiêu đồng phân cấu tạo có công thức phân tử C5H12?
A. 3 đồng phân.
B. 5 đồng phân.
C. 4 đồng phân.
D. 6 đồng phân.
Câu 21: Hòa tan hoàn toàn hỗn hợp gồm 0,12 mol FeS2 và a mol Cu2S vào axit HNO3 (vừa đủ) thu được
dung dịch X (chỉ chứa 2 muối sunfat) và khí duy nhất NO (không còn sản phẩm khử khác). Cho dung
dịch X tác dụng với dung dịch BaCl2 dư thu được m gam kết tủa. Giá tri m là A. 46,6. B. 65,24. C. 69,9. D. 23,3.
Câu 22: Cho các hợp chất hữu cơ: C2H2; C2H4; CH2O; CH2O2 (mạch hở); C3H4O2 (mạch hở, đơn chức).
Biết C3H4O2 không làm chuyển màu quỳ tím ẩm. Số chất tác dụng được với dung dịch AgNO3 trong NH3 tạo ra kết tủa là A. 3. B. 4. C. 2. D. 5.
Câu 23: Trộn 250 ml dung dịch hỗn hợp gồm HCl 0,08 mol/lít và H2SO4 0,01 mol/lít với 250 ml dung
dịch NaOH nồng độ x mol/ lít, được 500 ml dung dịch có pH = 12. Giá trị của x là A. 0,1. B. 0,09. C. 0,11. D. 0,12.
Câu 24: Đun nóng 10,56 gam este có công thức C4H8O2 với H2SO4 loãng cho đến khi phản ứng thủy phân
hoàn toàn, trung hòa hỗn hợp thu được bằng dung dịch NaOH dư, tiếp tục cho AgNO3/NH3 dư vào hỗn
hợp dung dịch, đun nóng thì thu m gam kết tủa. Tính m ? A. 38,88 gam. B. 25,92 gam. C. 12,96 gam. D. 51,84 gam.
Câu 25: Cho phản ứng hoá học: H2S + 4Cl2 + 4H2O → H2SO4 + 8HCl. Vai trò của H2S trong phản ứng là
A. Môi trường.
B. Vừa oxi hóa, vừa khử.
C. Chất oxi hóa. D. Chất khử.
Câu 26: Dãy gồm các chất trong phân tử có liên kết ion là
A. Na2SO4, K2S, KHS, NH4Cl.
B. KHS, Na2S, NaCl, HNO3.
C. Na2SO4, KHS, H2S, SO2.
D. H2O, K2S, Na2SO3, NaHS.
Câu 27: C3H6O2 có hai đồng phân đều tác dụng được với NaOH, không tác dụng với Na. Công thức cấu
tạo của hai đồng phân đó là :
A. CH3-CH(OH)-CHO và CH3-CO-CH2OH.
B. CH3-CH2-COOH và HCOO-CH2-CH3.
C. CH3-CH2-COOH và CH3-COO-CH3.
D. CH3-COO-CH3 và HCOO-CH2-CH3.
Câu 28: Đun nóng 2,9 gam hỗn hợp A gồm C2H2 và H2 trong bình kín với xúc tác thích hợp, sau phản
ứng được hỗn hợp khí X. Dẫn hỗn hợp X qua bình đựng dung dịch Br2 dư thấy bình tăng lên 0,7 gam và
còn lại hỗn hợp khí Y. Đốt cháy hỗn hợp khí Y thu được 4,4 gam CO2. Thể tích của hỗn hợp khí Y ở đktc là: A. 17,68 lít. B. 8,96 lít. C. 11,2 lít. D. 6,72 lít.
Câu 29: Cho một este no, đơn chức có %C = 54,55%. Công thức phân tử của este là? A. C4H6O2. B. C3H6O2. C. C2H4O2. D. C4H8O2.
Câu 30: Ảnh hưởng của nhóm -OH đến gốc C6H5- trong phân tử phenol thể hiện qua phản ứng giữa phenol với
A. Na kim loại.
B. dung dịch NaOH.
C. H2 (Ni, nung nóng). D. nước Br2.
Câu 31: Hiđrocacbon C4H8 có bao nhiêu đồng phân anken? A. 4. B. 1. C. 2. D. 3.
Câu 32: Hiện tượng quan sát được khi cho Cu vào dung dịch HNO3 đặc là
A. dung dịch không đổi màu và có khí màu nâu đỏ thoát ra.
B. dung dịch chuyển sang màu nâu đỏ,có khí màu xanh thoát ra.
C. dung dịch chuyển sang màu xanh và có khí không màu thoát ra.
D. dung dịch chuyển sang màu xanh và có khí màu nâu đỏ thoát ra.
Câu 33: Nhệt độ sôi được sắp xếp theo chiều tăng dần là?
A. CH3COOH < HCOOCH3 < C2H5OH < C2H6.
B. C2H5OH < C2H6 < HCOOCH3 < CH3COOH.
C. C2H6 < HCOOCH3 < C2H5OH < CH3COOH.
D. C2H6 < C2H5OH < HCOOCH3 < CH3COOH.
Câu 34: Chất có thể dùng để làm khô khí NH3 là A. CaO. B. FeSO4 khan. C. P2O5. D. H2SO4 đặc.
Câu 35: Cho hỗn hợp tất cả các đồng phân mạch hở của C4H8 tác dụng với H2O (H+, t°) thu được tối đa
bao nhiêu sản phẩm cộng? A. 4. B. 3. C. 1. D. 2.
Câu 36: Nhiệt phân hoàn toàn 34,65 gam hỗn hợp gồm KNO3 và Cu(NO3)2, thu được hỗn hợp khí X (tỉ
khối của X so với khí hiđro bằng 18,8). Khối lượng Cu(NO3)2 trong hỗn hợp ban đầu là A. 8,60 gam. B. 9,40 gam. C. 20,50 gam. D. 11,28 gam.
Câu 37: Thành phần các nguyên tố trong hợp chất hữu cơ
A. thường có C, H hay gặp O, N, sau đó đến halogen, S, P.
B. bao gồm tất cả các nguyên tố trong bảng tuần hoàn.
C. gồm có C, H và các nguyên tố khác.
D. nhất thiết phải có cacbon, thường có H, hay gặp O, N sau đó đến halogen, S, P.
Câu 38: Đốt cháy hết 1 mol hiđrocacbon X tạo ra 5 mol CO2. Khi cho X phản ứng với Cl2 (as) tạo ra một
dẫn xuất monoclo. Tên gọi của X là A. iso butan. B. iso pentan. C. pentan. D. neo pentan.
Câu 39: Cho phản ứng: C4H8O2 + NaOH → muối + ancol bậc 2. Công thức cấu tạo của C4H8O2 là ? A. CH3COOC2H5. B. C2H5COOCH3.
C. HCOO(CH2)2CH3. D. HCOOCH(CH3)2.
Câu 40: Dãy gồm các chất đều tác dụng được với NaOH là?
A. C2H5Cl, CH3COOH, CH3COOC2H5, C6H5OH.
B. C2H4, CH3COOH, CH3COOC2H5, C6H5OH.
C. C2H5Cl, CH3COOH, CH3COOC2H5, C2H5OH.
D. C2H5Cl, CH3CHO, CH3COOC2H5, C6H5OH.