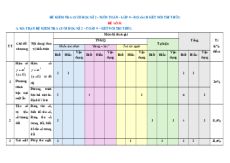
UBND TP BIÊN HÒA
ĐỀ KIỂM TRA HỌC KÌ I
TRƯỜNG THCS TRƯỜNG SA MÔN: Hóa – Lớp 9
Thời gian làm bài: 45 phút; không kể thời gian phát đề
Câu 1 (TH): Viết phương trình hóa học thực hiện chuỗi phản ứng sau:
Al → Al2O3 → Al2(SO4)3 → Al(OH)3 → Al2O3
Câu 2 (TH): a. Nêu phương pháp hóa học làm sạch dung dịch muối AlCl3 có lẫn muối CuCl2. Viết phương trình hóa học.
b. Để bảo quản cửa sắt được bền người ta thường làm gì? Giải thích cơ sở của việc làm đó?
c. Nêu phương pháp hóa học nhận biết các kim loại: Mg, Na, Cu.Viết phương trình hóa học.
Câu 3 (VD): Cho 1,2g kim loại A (hóa trị II) tác dụng hết với dung dịch HCl thu được 1,12 lít khí H2 ở đktc. Xác định A.
Câu 4 (VD): Cho 5,84g hỗn hợp Fe và FeO tác dụng vừa đủ với dung dịch HCl 1M. Sau phản ứng thu
được 0,896 lít (đktc) khí A và dung dịch B.
a. Tính thành phần phần trăm theo khối lượng của FeO trong hỗn hợp ban đầu.
b. Tính thể tích dung dịch axit đã dùng. Biết HCl có khối lượng riêng là 1,15g/ml.
c. Tính nồng độ phần trăm dung dịch B.
Cho Mg: 24; Fe: 56; 0:16; Zn: 65; CI: 35,5; H:1; Ca:40 LỜI GIẢI CHI TIẾT
Câu 1: Đáp án Phương pháp giải:
Dựa vào kiến thức được học về tính chất hóa học của Al - sgk hóa trang 55 Giải chi tiết:
Câu 2: Đáp án Phương pháp giải:
a) Chọn chất làm sạch có phản ứng với dd CuCl2 và không sinh dd mới
b) Dựa vào kiến thức bài 21 sự ăn mòn kim loại và bảo vệ kim loại không bị ăn mòn - sgk hóa 9 - trang 64
c) Dựa vào tính chất hóa học khác nhau của Na, Mg, Cu. Trang 1
Giải chi tiết:
a. Cho kim loại Al vào hỗn hợp, sau đó lọc bỏ chất rắn ta sẽ thu được dd AlCl3 tinh khiết
PTHH: 2Al + 3CuCl2 → 2AlCl3 + 3Cu↓
b. Để cửa sắt được bền người ta thường sơn lên cửa sắt 1 lớp sơn. Việc sơn này để tránh sự tiếp xúc của
sắt với oxi không khí, hơi nước bên ngoài từ đó tránh được sắt bị gỉ (ăn mòn sắt)
c. Hòa tan các kim loại vào nước dư
+ Kim loại nào tan có khí thoát ra là Na
PTHH: 2Na + 2H2O → 2NaOH + H2↑
+ Hai kim loại không tan là Mg và Cu
- Cho dd HCl dư lần lượt vào 2 kim loại không tan trên
+ Kim loại nào tan dần và có khí không màu thoát ra là Mg
PTHH: Mg + 2HCl → MgCl2 + H2↑
+ Còn lại không có hiện tượng gì là Cu.
Câu 3: Đáp án Phương pháp giải: Đổi số mol H2
Viết PTHH xảy ra, tính số mol A theo số mol H2 → MA = mA : nA = ? Giải chi tiết:
PTHH: A + 2HCl → ACl2 + H2↑
Theo PTHH: nA = nH2 = 0,05 (mol)
=> A là kim loại Magie (KH: Mg)
Câu 4: Đáp án Phương pháp giải:
a. Viết PTHH xảy ra, tính số mol Fe theo mol H2
Từ đó tính được mFe và phần trăm khối lượng mỗi chất
b. Tính số mol HCl theo số mol Fe và FeO
c. mdd B = mhh + mdd HCl - mH2 = ? dd B chứa FeCl2 Giải chi tiết: a) PTHH: Trang 2
Đề thi cuối kì 1 Hóa học 9 trường THCS Trường Sa
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Đề thi được cập nhật liên tục trong gói này từ nay đến hết tháng 6/2023. Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Bộ 29 Đề thi học kì 1 Hóa học năm 2023 chọn lọc từ các trường bản word có lời giải chi tiết gồm:
+ Đề thi học kì 1 Hóa học năm 2023 trường THCS Trần Quốc Toản – Quận Bình Tân;
+Đề thi học kì 1 Hóa học năm 2023 trường THCS Nguyễn Trãi - Thành phố Châu Đốc;
+Đề thi học kì 1 Hóa học năm 2023 trường THCS Trường Sa - Thành phố Biên Hòa;
+Đề thi học kì 1 Hóa học năm 2023 Sở GD_ĐT Lạng Sơn.
…..……………………
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(648 )Trọng Bình
Giúp ích cho tôi rất nhiều
Duy Trần
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN Hóa Học
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Lớp 9
Xem thêmTài liệu bộ mới nhất