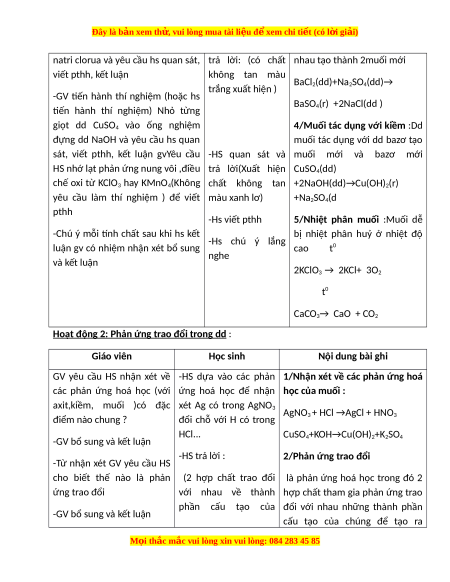
Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t (c ế ó l i ờ gi i ả ) Ngày soạn : Tuần 7 , tiết 14 ,15
TÍNH CHẤT HOÁ HỌC CỦA MUỐI I. M ục tiêu 1) K
iến thức : Học sinh biết
-Những tính chất hoá học của muối (kiến thức trọng tâm): tác dụng với kim
loại, dd axit, dd bazơ, dd muối khác, nhiều muối bị nhiệt phân huỷ ở nhiệt độ cao.
-Khái niệm phản ứng trao đổi và những điều kiện để xảy ra phản ứng trao đổi (kiến thức trọng tâm) 2) K ĩ năng :
-Tiến hành một số thí nghiệm, quan sát giải thích hiện tượng rút ra được kết
luận về tính chất hoá học của muối.
-viết đựơc các PTHH minh hoạ cho mỗi tính chất hoá học của muối.
-Tính thể tích hoặc khối lượng dd muối trong phản ứng. 3) T hái độ:
- Ham mê hóa học và khoa học, tích cực học tập và giải quyết vấn đề
4) Phát triển năng lực
- Năng lực tự học và giải quyết vấn đề
- Năng lực sử dụng ngôn ngữ hóa học
- Năng lực quan sát và giải thích thí nghiệm
- Năng lực giao tiếp và làm việc cá nhân, làm việc nhóm II. Chuẩn bị :
Dụng cụ :giá ống nghiệm ,ống nghiệm ,kẹp gỗ ,ống hút và nhỏ giọt hoá chất ,đèn cồn . M i ọ thắc m c
ắ vui lòng xin vui lòng: 084 283 45 85
Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t (c ế ó l i ờ gi i ả )
Hoá chất :Dd AgNO3, dd NaCl, dd CuSO4, KMnO4 tinh thể , dd HCl ,dd BaCl2, dd
Na2SO4, dd NaOH , đinh sắt mới . III. T
iến trình lên lớp : 1) Ổ n định : 2) K
iểm tra bài cũ :Nêu tính chất hoá học của Ca(OH)2 . 3) C
ác hoạt động dạy và học :
-Giới thiệu bài :GV yêu cầu HS viết CTHH của 1 số hợp chất có tên sau :Natri clorua ,
kali cacbonat ,sắt(II) sunfat, canxi hiđrô cacbonat
Các em có nhận xét gì về thành phần phân tử của hợp chất trên .HS trả lời →GV
giới thiệu tên bài học và ghi đề mục lên bảng H
oạt động 1:Nghiên cứu tính chất hoá học của muối : Giáo viên Học sinh Nội dung bài ghi
-GV tiến hành thí nghiệm( hoặc hs - HS tiến hành thí 1/Muối tác dụng với kim loại
làm thí nghiệm).Thả 1 đinh sắt nghiệm (nếu có)
Dd muối có thể tác dụng với
sạch vào ống nghiệm đựng dd
kim loại tạo thành muối mới CuSO4 và kim loại mới
-GV yêu cầu hs quan sát hiện Fe(r)+CuSO4(dd)→FeSO4(dd)
tượng, viết pthh và kết luận
-Hs qsát và trả lời +Cu(r) Cây đinh sắt có
-Gv tiến hành thí nghiệm (hoặc hs
2/Muối tác dụng với axit: màu đỏ ,dd CuSO
tiến hành thí nghiệm).Thả 1 mẫu 4 nhạt dần
Muối có thể tác dụng được với
nhỏ CaCO3 vào ống nghiệm chứa
axit sản phẩm là muối mới và
dd HCl và yêu cầu hs quan sát và -Hs quan sát và axit mới viết pthh và kết luận trả lời Có sũi bọt khí CaCO
-GV tiến hành thí nghiệm(hoặc hs 3(r)+H2SO4(dd)→
tiến hành thí nghiệm) nhỏ vài giọt CaSO4(r)+H2O(l)+CO2(k) dd AgNO3
3/Muối tác dụng với muối:
Vào ống nghiệm có sẵn 1ml dd -Hs quan sát và 2 dd muối có thể tác dụng với M i ọ thắc m c
ắ vui lòng xin vui lòng: 084 283 45 85
Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t (c ế ó l i ờ gi i ả )
natri clorua và yêu cầu hs quan sát, trả lời: (có chất nhau tạo thành 2muối mới viết pthh, kết luận không tan màu BaCl trắng xuất hiện ) 2(dd)+Na2SO4(dd)→
-GV tiến hành thí nghiệm (hoặc hs BaSO
tiến hành thí nghiệm) Nhỏ từng 4(r) +2NaCl(dd )
giọt dd CuSO4 vào ống nghiệm
4/Muối tác dụng với kiềm :Dd
đựng dd NaOH và yêu cầu hs quan
muối tác dụng với dd bazơ tạo
sát, viết pthh, kết luận gvYêu cầu -HS quan sát và muối mới và bazơ mới
HS nhớ lạt phản ứng nung vôi ,điều trả lời(Xuất hiện CuSO4(dd)
chế oxi từ KClO3 hay KMnO4(Không chất không tan +2NaOH(dd)→Cu(OH)2(r)
yêu cầu làm thí nghiệm ) để viết màu xanh lơ) +Na2SO4(d pthh -Hs viết pthh
5/Nhiệt phân muối :Muối dễ
-Chú ý mỗi tính chất sau khi hs kết
bị nhiệt phân huỷ ở nhiệt độ -Hs chú ý lắng
luận gv có nhiệm nhận xét bổ sung cao t0 nghe và kết luận 2KClO3 → 2KCl+ 3O2 t0 CaCO3→ CaO + CO2
Hoạt động 2: Phản ứng trao đổi trong dd : Giáo viên Học sinh Nội dung bài ghi
GV yêu cầu HS nhận xét về -HS dựa vào các phản 1/Nhận xét về các phản ứng hoá
các phản ứng hoá học (với ứng hoá học để nhận học của muối :
axit,kiềm, muối )có đặc xét Ag có trong AgNO3 AgNO điểm nào chung ? đổi chỗ với H có trong 3 + HCl →AgCl + HNO3 HCl... CuSO
-GV bổ sung và kết luận 4+KOH→Cu(OH)2+K2SO4 -HS trả lời :
2/Phản ứng trao đổi
-Từ nhận xét GV yêu cầu HS
cho biết thế nào là phản (2 hợp chất trao đổi là phản ứng hoá học trong đó 2 ứng trao đổi
với nhau về thành hợp chất tham gia phản ứng trao
phần cấu tạo của đổi với nhau những thành phần
-GV bổ sung và kết luận
cấu tạo của chúng để tạo ra M i ọ thắc m c
ắ vui lòng xin vui lòng: 084 283 45 85
Giáo án Tính chất hóa học của muối Hóa học 9
721
361 lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Bộ giáo án Hóa 9 được cập nhật liên tục trong gói này từ nay đến hết tháng 3/2024.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Bộ giáo án Hóa học 9 năm 2023 mới, chuẩn nhất (tặng kèm đề kiểm tra 1 tiết, đề thi học kì) được thiết kế theo phong cách hiện đại, đẹp mắt, trình bày chi tiết cho từng bài học và bám sát chương trình Sách giáo khoa Hóa 9.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(721 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN Hóa Học
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Lớp 9
Xem thêmTài liệu bộ mới nhất

Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có l i gi i)ả ử ệ ể ế ờ ả
TÍNH CHẤT HOÁ HỌC CỦA MUỐI
I. Mục êu
1)
!"#$%&'()*%+",-./(%
0,,$1,,$23,,%&("4%&567*896:;$<
"6%7=)$:>.:4(6:?1=)$7=)$:>
'()*%+
2) @A
%;&B6%C$"=B6DE)F)$:DE(
0G.4 !"#$%&<
.:H3"I%%J !"#$%&<
B? K(&0DE,,%&)7=<
3) ":;
$%%LM$.($ HG7.=C.!:4
4)I")?A0H
A0HH.=C.!:4
A0HN,-OM$
A0HC$".=BB6%
A0H$7.0%.6"*0%.6M%
II. Chuẩn bị :
P--"&6%&6%(Q7J&F.R"!:S
T<
M i th c m c vui lòng xin vui lòng: 084 283 45 85ọ ắ ắ

Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có l i gi i)ả ử ệ ể ế ờ ả
"!P,UV
W
,,$X0,,XYV
ZV
?,,X0,,[$X0
\
,,
$
\
YV
,,$V:]%/<
III. Tiến trình lên lớp
1) ^:5
2) ?%)$_ L !"#$X$'V+
\
<
3) X":;,.
`/6`aLY.X#$&E7!ML$$)0)$
($0$$]'bb+c$$1:)O$$
X"d%MG1ef.477*N#$E7!)L<Y)=0gh`a
/6L.:4%-0L=
Hoạt động 1:Nghiên cứu 0nh chất hoá học của muối
Giáo viên Học sinh Nội dung bài ghi
`aB6%'K
0% B 6%+<= : ]
. & 6% :H ,,
XYV
`a L C$ " 6
DE.7.(0G
`.B6%'K
B6%+<=%i
RX$XV
W
.&6%$
,,X0.LC$".
.7.(0G
`aB6%'K
B6%+R.
,,UV
W
a & 6% M j %0 ,,
YB
6%'M+
C".)=0g
Cây đinh sắt có
màu đỏ ,dd CuSO
4
nhạt dần
C$ " .
)=0g Có sũi bọt
khí
C$ " .
1/Muối tác dụng với kim loại
P,%&M?",-./
(%0%&%/
.(%0%/
kd')+lXYV
',,+hkdYV
',,+
lX')+
2/Muối tác dụng với axit
Z&M?",-:DE./
$1=7m%0%&%/.
$1%/
X$XV
W
')+l
\
YV
',,+h
X$YV
')+l
\
V'0+lXV
\
'(+
3/Muối tác dụng với muối:
\,,%&M?",-./
M i th c m c vui lòng xin vui lòng: 084 283 45 85ọ ắ ắ

Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có l i gi i)ả ử ệ ể ế ờ ả
$)0)$.LC$"
.7(0G
`aB6%'K
B 6%+ R n
,, XYV
. & 6%
:H,,$V.LC$
".7(0G.oL
Y/07=.O:4
1nX0V
W
$ZV
'O
L0%B6%+:?.
7
XFp%J !$((
0G.M6%G1e>
.(0G
)= 0g 'M !
(O $ %
)]1!6+
Y C$ " .
)= 0g'q! 6
! (O $
%1$03+
.7
F p 0]
d
$\%&%/
[$X0
\
',,+l$
\
YV
',,+h
[$YV
')+l\$X0',,+
4/Muối tác dụng với kiềmP,
%&",-./,,$23
%& %/ . $23 %/
XYV
',,+
l\$V',,+hX'V+
\
')+
l$
\
YV
',
5/Nhiệt phân muối Z&,r
567*896:;
$
s
\X0V
W
h\X0lWV
\
s
X$XV
W
hX$VlXV
\
Hoạt động 2: Phản ứng trao đổi trong dd
Giáo viên Học sinh Nội dung bài ghi
`aLYG1e.4
"7="'./
$1(4% %& +M :K
:?%t
`a>.(0G
nG1e`aLY
0 7=
)$:>
`a>.(0G
Y,H$."7=
":?G
1eUM)UV
W
:>J./M)
X0<<<
Y)=0g
'\E7!)$:>
./ $ .4
7 ! #$
1/Nhận xét về các phản ứng hoá
học của muối :
UV
W
lX0hUX0lV
W
XYV
lVhX'V+
\
l
\
YV
2/Phản ứng trao đổi
07="):M\
E7!$%$7=)$
:>./$7
! #$ F :? )$
M i th c m c vui lòng xin vui lòng: 084 283 45 85ọ ắ ắ