Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t (c ế ó l i ờ gi i ả ) SỞ GIÁO D C Ụ VÀ ĐÀO T O Ạ Đ Ề THI CH N Ọ H C Ọ SINH GI I Ỏ L P Ớ 9 H U Ậ GIANG
NĂM HỌC: 2022 – 2023 Đ C Ề HÍNH TH C Ứ
Môn thi: Hóa học – Ngày thi: 01/03/2023 Th i ờ gian: 150 phút (không k ể th i ờ gian giao đ ) ề
Câu 1 (5,0 điểm).
1. Hãy cho biết các chất X, Y, Z, T, M và hoàn thành s đ ơ ồ chuyển hóa sau: 0 t (1): X + H 2SO4 đặc Y + SO2 + H2O 0 t
(2): T + CO X + CO2 (3): Y + KOH Z + K2SO4
(4): X + Y M 0 t
(5): Z T + H2O 1.2. M t ộ b n ạ h c
ọ sinh đã làm 5 thí nghi m ệ v i ớ 5 ch t ấ khác nhau c a ủ X và đ u ề cho k t ế t a ủ sau ph n ả ng. ứ Phư ng t ơ rình hóa h c ọ chung có dạng nh s
ư au: X+ Ba(NO3)2 Y↓ + NaNO3 Tìm 5 chất th a ỏ mãn và vi t ế các phư ng t ơ rình c a ủ ph n ả ng ứ hóa h c ọ đã x y ra ả ?
Câu 2 (5,0 điểm). 2.1. Có 4 ng nghi ố m ệ , m i ỗ ng c ố hứa một dung d c ị h mu i ố (không trùng kim lo i ạ cũng nh g ư c ố axit) t ừ nh ng ki ữ
m loại: Pb, Mg, K, Ba và nh ng g ữ c
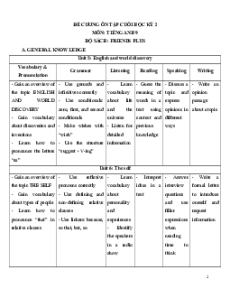
ố axit: nitrat, cacbonat, sunfat, clorua. a) Hãy cho biết dung d c ị h mu i ố chứa trong 4 ng nghi ố m ệ trên. b) Trình bày phư ng ơ pháp hóa h c ọ nhận bi t ế t ng dung d ừ ịch trong ng ố nghi m ệ . 2.2. Hình v d ẽ ư i
ớ đây mô tả các đi u c ề
hế oxi trong phòng thí nghiệm
a) Hãy cho biết tại sao oxi đư c ợ đi u c ề h t ế heo phư ng phá ơ p đ y n ẩ ư c ớ ? b) Tại sao ng nghi ố m ệ đ ng K ự
MnO4 lại lắp hơi chúc xu ng và ố khi k t ế thúc thí nghi m ệ ph i ả tháo ng ố d n ẫ
khí trước khi tắt đèn c n? ồ c) Để thu đư c ợ 112 ml oxi đkt ở c c n ph ầ i
ả dùng bao nhiêu gam KMnO4 biết hi u s ệ uất phản ng l ứ à 80%?
Câu 3 (5,0 điểm). 3.1. Đ i ờ s ng ố c a ủ th c ự v t ậ và đ ng ộ v t ậ ph ụ thu c ộ vào pH c a ủ môi trư ng. ờ M t ộ s ố cây tr ng ồ thích h p ợ v i ớ
đất chua (đất axit) có pH t 4 đ ừ n 6. M ế t
ộ số khác lại thích h p v ợ ới đất ki m ề có pH từ 8 đ n 9. Cá ế thích h p ợ M i
ọ thắc mắc vui lòng xin liên h h
ệ otline: 084 283 45 85
Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t (c ế ó l i ờ gi i ả ) v i ớ nước có pH b ng ằ 7. Em hãy tính xem c n ầ thêm vào các dung d c ị h dư i
ớ đây bao nhiêu ml dung d c ị h NaOH 0,01M ho c ặ HCl 0,01M đ dung d ể c
ị h sau khi thêm có pH b ng 7. ằ a. 100 ml dung d c ị h Ca(OH)2 0,01M. b. 100 ml dung dịch g m
ồ HNO3 0,015M và H2SO4 0,005M. 3.2. H p c ợ
hất A và B là hai chất chỉ ch a ứ các nguyên t
ố X, Y. Thành phần phần trăm c a ủ nguyên t ố X trong
A và B lần lư t ợ là 30,49% và 25,9%. Bi t ế rằng A, B có kh i ố lư ng ợ phân t l ử n l ầ ư t ợ là 46 đvC và 108 đvC.
a) Biết rằng công thức phân t c ử a
ủ A là XY2. Tìm công thức c a ủ A, B. b) Hoàn thành phản ng s ứ au: A + O2 + H2O Z B + H2O Z
Câu 4 (5,0 điểm). 4.1. Trong “viên s i ủ ” có nh ng ữ ch t ấ hóa h c ọ có tác d ng ụ ch a ữ b nh, ệ ngoài ra còn còn m t ộ ít b t ộ natri hidrocacbonat và b t ộ axit h u
ữ cơ như axit xitric (axit có trong quả chanh). Khi “viên s i ủ ” g p ặ nư c ớ t o ạ ra dung d c ị h axit. Dung d c ị h này tác d ng v ụ i
ớ NaHCO3 sinh ra khí cacbonic theo phư ng ơ trình sau:
HOC3H4(COOH)3 + 3NaHCO3 → HOC3H4(COONa)3 + 3CO2↑ + 3H2O Khí này thoát ra kh i ỏ c c ố nư c ớ dưới d ng b ạ t ọ khí. a. Tính th t ể ích CO2 thu đư c ợ ở đktc n u t ế rong “viên s i ủ ” có ch a
ứ 0,42 gam NaHCO3 biết lư ng a ợ xit xitric tạo ra đ đ ủ ể hòa tan hết lư ng ợ NaHCO3. b. Dẫn toàn b khí ộ CO2 thu đư c ợ t ở rên qua 100 ml dung d c
ị h Ca(OH)2 0,03M thì thu được bao nhiêu gam kết t a ủ . 4.2.a. Nhà máy nư c ớ thư ng
ờ khai thác và xử lý nư c ớ ng m ầ để cung c p ấ nư c ớ s c ạ h cho thành ph , ố nông thôn. Trong nư c ớ ngầm thư ng ờ có ch a ứ s t ắ , mangan dư i ớ d ng ạ mu i ố s t
ắ (II), mangan (II) tan trong nư c ớ có nh ả hư ng ở không t t ố t i ớ s c ứ kh e ỏ con ngư i ờ . Để lo i ạ bỏ h p ợ ch t ấ s t
ắ (II), mangan (II) trong nư c ớ ng m ầ , các nhà máy nước s d ử ng m ụ
ột trong các cách sau đây: (i): B m ơ nư c ớ ngầm cho ch y qua ả các giàn m a ư . (ii): S c ụ khí oxi vào b c ể h a ứ nước ngầm. Em hãy cho bi t ế m c ụ đích c a ủ hai cách làm trên.
b. Oxi hóa hoàn toàn 10,52 gam h n ỗ h p ợ ba kim lo i ạ d ng ạ b t ộ Fe, Al, Cu b ng ằ oxi thu đư c ợ 17,4 gam h n ỗ h p ợ oxit. Vi t ế các ph n ả ng ứ x y
ả ra và tìm thể tích nhỏ nh t ấ c a ủ dung d c ị h HCl 2,0M đ ể hòa tan v a ừ h t ế lư ng ợ h n h ỗ p oxi ợ t trên. ----------------H t ế ---------------- M i
ọ thắc mắc vui lòng xin liên h h
ệ otline: 084 283 45 85
Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t (c ế ó l i ờ gi i ả ) SỞ GIÁO D C Ụ VÀ ĐÀO T O Ạ
HDC ĐỀ THI CHỌN HỌC SINH GIỎI LỚP 9 H U Ậ GIANG
NĂM HỌC: 2022 – 2023 ĐÁP ÁN
Môn thi: Hóa học – Ngày thi: 01/03/2023
Thời gian: 150 phút (không kể thời gian giao đề)
Câu 1 (5,0 điểm).
1. Hãy cho biết các chất X, Y, Z, T, M và hoàn thành s đ ơ ồ chuyển hóa sau: 0 t (1): X + H 2SO4 đặc Y + SO2 + H2O 0 t
(2): T + CO X + CO2 (3): Y + KOH Z + K2SO4
(4): X + Y M 0 t
(5): Z T + H2O Giải 0 t (1): 2Fe + 6H 2SO4 đặc Fe2(SO4)3 + 3SO2 + 6H2O 0 t (2): Fe 2O3 + 3CO 2Fe + 3CO2 (3): Fe2(SO4)3 + 6KOH 2Fe(OH)3↓ + 3K2SO4 (4): Fe + Fe2(SO4)3 3FeSO4 0 t (5): 2Fe(OH) 3 Fe2O3 + 3H2O 1.2. M t ộ b n ạ h c
ọ sinh đã làm 5 thí nghi m ệ v i ớ 5 ch t ấ khác nhau c a ủ X và đ u ề cho k t ế t a ủ sau ph n ả ng. ứ Phư ng t ơ rình hóa h c ọ chung có dạng nh s
ư au: X+ Ba(NO3)2 Y↓ + NaNO3 Tìm 5 chất th a ỏ mãn và vi t ế các phư ng t ơ rình c a ủ ph n ả ng ứ hóa h c ọ đã x y ra ả ? Giải (1): Na2SO4 + Ba(NO3)2 BaSO4↓ + 2NaNO3 (2): Na2CO3 + Ba(NO3)2 BaCO3↓ + 2NaNO3 (3): Na2SO3 + Ba(NO3)2 BaSO3↓ + 2NaNO3
(4): 2Na3PO4 + 3Ba(NO3)2 Ba3(PO4)2↓ + 6NaNO3 M i
ọ thắc mắc vui lòng xin liên h h
ệ otline: 084 283 45 85
Đây là bản xem th , vu ử i lòng mua tài li u ệ đ xe ể m chi ti t (c ế ó l i ờ gi i ả )
(5): Na2SiO3 + Ba(NO3)2 BaSiO3↓ + 2NaNO3
Câu 2 (5,0 điểm). 2.1. Có 4 ng nghi ố m ệ , m i ỗ ng c ố hứa một dung d c ị h mu i ố (không trùng kim lo i ạ cũng nh g ư c ố axit) t ừ nh ng ki ữ
m loại: Pb, Mg, K, Ba và nh ng g ữ c
ố axit: nitrat, cacbonat, sunfat, clorua. a) Hãy cho biết dung d c ị h mu i ố chứa trong 4 ng nghi ố m ệ trên. b) Trình bày phư ng ơ pháp hóa h c ọ nhận bi t ế t ng dung d ừ ịch trong ng ố nghi m ệ . Giải a) 4 dung d c
ị h cần tìm là: Pb(NO3)2, MgSO4, K2CO3, BaCl2. b) Dùng HCl đặc phân bi t ệ đư c ợ Pb(NO3)2 vì tạo k t ế t a ủ tr ng: ắ
Pb(NO3)2 + 2HCl → PbCl2↓ + 2HNO3
K2CO3 vì có khí bay ra: K2CO3 + 2HCl → 2KCl + CO2↑ + H2O
Dùng H2SO4 để nhận ra BaCl2 vì tạo kết tủa trắng, còn lại là MgSO4:
BaCl2 + H2SO4 → BaSO4↓ + 2HCl 2.2. Hình v d ẽ ư i
ớ đây mô tả các đi u c ề
hế oxi trong phòng thí nghiệm
a) Hãy cho biết tại sao oxi đư c ợ đi u c ề h t ế heo phư ng phá ơ p đ y n ẩ ư c ớ ? b) Tại sao ng nghi ố m ệ đ ng K ự
MnO4 lại lắp hơi chúc xu ng và ố khi k t ế thúc thí nghi m ệ ph i ả tháo ng ố d n ẫ
khí trước khi tắt đèn c n? ồ c) Để thu đư c ợ 112 ml oxi đkt ở c c n ph ầ i
ả dùng bao nhiêu gam KMnO4 biết hi u s ệ uất phản ng l ứ à 80%? Giải a) Vì oxi ít tan trong nư c ớ và không ph n ả ng ứ v i ớ nư c ớ . b) ng nghi Ố m ệ lắp KMnO4 phải h i ơ chúc xu ng đ ố nh ể ng gi ữ ọt nư c ớ b ng ị ng ư t không c ụ hảy ngư c ợ l i ạ làm n t ứ , vỡ ng do s ố c ự hênh l c ệ h nhi t ệ đ . ộ Nếu tắt đèn c n t ồ rư c ớ thì giữa ng nghi ố ệm n m
ằ ngang và bên ngoài có s c ự hênh l c ệ h áp su t ấ và nhi t ệ đ ộ do đó nư c ớ t bê ừ n ngoài b hút ị vào ng nghi ố
ệm nằm ngang do đó có thể làm v ỡ ng nghi ố m ệ . 0 t c) 2KMnO 4 K2MnO4 + MnO2 + O2 s m
ố ol KMnO4 = 2.số mol O2 = 0,01 mol m = 158 : 80% = 1,975 gam.
Câu 3 (5,0 điểm). 3.1. Đ i ờ s ng ố c a ủ th c ự v t ậ và đ ng ộ v t ậ ph ụ thu c ộ vào pH c a ủ môi trư ng. ờ M t ộ s ố cây tr ng ồ thích h p ợ v i ớ
đất chua (đất axit) có pH t 4 đ ừ n 6. M ế t
ộ số khác lại thích h p v ợ ới đất ki m ề có pH từ 8 đ n 9. Cá ế thích h p ợ v i ớ nước có pH b ng ằ 7. Em hãy tính xem c n ầ thêm vào các dung d c ị h dư i
ớ đây bao nhiêu ml dung d c ị h NaOH 0,01M ho c ặ HCl 0,01M đ dung d ể c
ị h sau khi thêm có pH b ng 7. ằ a. 100 ml dung d c ị h Ca(OH)2 0,01M. M i
ọ thắc mắc vui lòng xin liên h h
ệ otline: 084 283 45 85
Đề HSG Hóa 9 Sở Hậu Giang năm 2023 có đáp án
2.3 K
1.2 K lượt tải
MUA NGAY ĐỂ XEM TOÀN BỘ TÀI LIỆU
CÁCH MUA:
- B1: Gửi phí vào TK:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official ( nhấn vào đây ) để xác nhận thanh toán và tải tài liệu - giáo án
Liên hệ ngay Hotline hỗ trợ: 084 283 45 85
Tài liệu được cập nhật liên tục trong gói này từ nay đến hết tháng 3/2024. Chúng tôi đảm bảo đủ số lượng đề đã cam kết hoặc có thể nhiều hơn, tất cả có BẢN WORD, LỜI GIẢI CHI TIẾT và tải về dễ dàng.
Để tải tài liệu gốc về máy bạn click vào nút Tải Xuống ở trên!
Thuộc bộ (mua theo bộ để tiết kiệm hơn):
- Tailieugiaovien.com.vn giới thiệu Đề HSG Hóa 9 Sở Hậu Giang năm 2023 có đáp án.
- File word có lời giải chi tiết 100%.
- Mua trọn bộ sẽ tiết kiệm hơn tải lẻ 50%.
Đánh giá
4.6 / 5(2328 )5
4
3
2
1
Trọng Bình
Tài liệu hay
Giúp ích cho tôi rất nhiều
Duy Trần
Tài liệu chuẩn
Rất thích tài liệu bên VJ soạn (bám sát chương trình dạy)
TÀI LIỆU BỘ BÁN CHẠY MÔN Hóa Học
Xem thêmTÀI LIỆU BỘ BÁN CHẠY Lớp 9
Xem thêmTài liệu bộ mới nhất
Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có l i gi i)ả ử ệ ể ế ờ ả
S GIÁO D C VÀ ĐÀO T OỞ Ụ Ạ
H U GIANGẬ
Đ CHÍNH TH CỀ Ứ
Đ THI CH N H C SINH GI I L P 9Ề Ọ Ọ Ỏ Ớ
NĂM H C: 2022 – 2023Ọ
Môn thi: Hóa h c – Ngày thi: 01/03/2023ọ
Th i gian: 150 phút (không k th i gian giao đ )ờ ể ờ ề
Câu 1 (5,0 đi m)ể .
1. Hãy cho bi t các ch t ế ấ X, Y, Z, T, M và hoàn thành s đ chuy n hóa sau:ơ ồ ể
(1): X + H
2
SO
4
đ cặ
0
t
Y + SO
2
+ H
2
O
(2): T + CO
0
t
X + CO
2
(3): Y + KOH
Z + K
2
SO
4
(4): X + Y
M
(5): Z
0
t
T + H
2
O
1.2. M t b n h c sinh đã làm 5 thí nghi m v i 5 ch t khác nhau c a ộ ạ ọ ệ ớ ấ ủ X và đ u cho k t t a sau ph n ng.ề ế ủ ả ứ
Ph ng trình hóa h c chung có d ng nh sau:ươ ọ ạ ư X+ Ba(NO
3
)
2
Y↓ + NaNO
3
Tìm 5 ch t th a mãn và vi t các ph ng trình c a ph n ng hóa h c đã x y ra?ấ ỏ ế ươ ủ ả ứ ọ ả
Câu 2 (5,0 đi m)ể .
2.1. Có 4 ng nghi m, m i ng ch a m t dung d ch mu i (không trùng kim lo i cũng nh g c axit) t ố ệ ỗ ố ứ ộ ị ố ạ ư ố ừ
nh ng kim lo i: Pb, Mg, K, Ba và nh ng g c axit: nitrat, cacbonat, sunfat, clorua.ữ ạ ữ ố
a) Hãy cho bi t dung d ch mu i ch a trong 4 ng nghi m trên.ế ị ố ứ ố ệ
b) Trình bày ph ng pháp hóa h c nh n bi t t ng dung d ch trong ng nghi m.ươ ọ ậ ế ừ ị ố ệ
2.2. Hình v d i đây mô t các đi u ch oxi trong phòng thí nghi mẽ ướ ả ề ế ệ
a) Hãy cho bi t t i sao oxi đ c đi u ch theo ph ng pháp đ y n c?ế ạ ượ ề ế ươ ẩ ướ
b) T i sao ng nghi m đ ng KMnOạ ố ệ ự
4
l i l p h i chúc xu ng và khi k t thúc thí nghi m ph i tháo ng d n ạ ắ ơ ố ế ệ ả ố ẫ
khí tr c khi t t đèn c n?ướ ắ ồ
c) Đ thu đ c 112 ml oxi đktc c n ph i dùng bao nhiêu gam KMnOể ượ ở ầ ả
4
bi t hi u su t ph n ng là 80%?ế ệ ấ ả ứ
Câu 3 (5,0 đi m)ể .
3.1. Đ i s ng c a th c v t và đ ng v t ph thu c vào pH c a môi tr ng. M t s cây tr ng thích h p v iờ ố ủ ự ậ ộ ậ ụ ộ ủ ườ ộ ố ồ ợ ớ
đ t chua (đ t axit) có pH t 4 đ n 6. M t s khác l i thích h p v i đ t ki m có pH t 8 đ n 9. Cá thích h pấ ấ ừ ế ộ ố ạ ợ ớ ấ ề ừ ế ợ
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ

Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có l i gi i)ả ử ệ ể ế ờ ả
v i n c có pH b ng 7. Em hãy tính xem c n thêm vào các dung d ch d i đây bao nhiêu ml dung d chớ ướ ằ ầ ị ướ ị
NaOH 0,01M ho c HCl 0,01M đ dung d ch sau khi thêm có pH b ng 7. ặ ể ị ằ
a. 100 ml dung d ch Ca(OH)ị
2
0,01M.
b. 100 ml dung d ch g m HNOị ồ
3
0,015M và H
2
SO
4
0,005M.
3.2. H p ch t ợ ấ A và B là hai ch t ch ch a các nguyên t ấ ỉ ứ ố X, Y. Thành ph n ph n trăm c a nguyên t ầ ầ ủ ố X trong
A và B l n l t là 30,49% và 25,9%. Bi t r ng A, B có kh i l ng phân t l n l t là 46 đvC và 108 đvC.ầ ượ ế ằ ố ượ ử ầ ượ
a) Bi t r ng công th c phân t c a ế ằ ứ ử ủ A là XY
2
. Tìm công th c c a ứ ủ A, B.
b) Hoàn thành ph n ng sau:ả ứ
A + O
2
+ H
2
O
Z
B + H
2
O
Z
Câu 4 (5,0 đi m)ể .
4.1. Trong “viên s i” có nh ng ch t hóa h c có tác d ng ch a b nh, ngoài ra còn còn m t ít b t natriủ ữ ấ ọ ụ ữ ệ ộ ộ
hidrocacbonat và b t axit h u c nh axit xitric (axit có trong qu chanh). Khi “viên s i” g p n c t o raộ ữ ơ ư ả ủ ặ ướ ạ
dung d ch axit. Dung d ch này tác d ng v i NaHCOị ị ụ ớ
3
sinh ra khí cacbonic theo ph ng trình sau:ươ
HOC
3
H
4
(COOH)
3
+ 3NaHCO
3
→ HOC
3
H
4
(COONa)
3
+ 3CO
2
↑ + 3H
2
O
Khí này thoát ra kh i c c n c d i d ng b t khí.ỏ ố ướ ướ ạ ọ
a. Tính th tích COể
2
thu đ c đktc n u trong “viên s i” có ch a 0,42 gam NaHCOượ ở ế ủ ứ
3
bi t l ng axit xitric ế ượ
t o ra đ đ hòa tan h t l ng NaHCOạ ủ ể ế ượ
3
.
b. D n toàn b khí COẫ ộ
2
thu đ c trên qua 100 ml dung d ch Ca(OH)ượ ở ị
2
0,03M thì thu đ c bao nhiêu gam ượ
k t t a.ế ủ
4.2.a. Nhà máy n c th ng khai thác và x lý n c ng m đ cung c p n c s ch cho thành ph , nôngướ ườ ử ướ ầ ể ấ ướ ạ ố
thôn. Trong n c ng m th ng có ch a s t, mangan d i d ng mu i s t (II), mangan (II) tan trong n c cóướ ầ ườ ứ ắ ướ ạ ố ắ ướ
nh h ng không t t t i s c kh e con ng i. Đ lo i b h p ch t s t (II), mangan (II) trong n c ng m,ả ưở ố ớ ứ ỏ ườ ể ạ ỏ ợ ấ ắ ướ ầ
các nhà máy n c s d ng m t trong các cách sau đây:ướ ử ụ ộ
(i): B m n c ng m cho ch y qua các giàn m a.ơ ướ ầ ả ư
(ii): S c khí oxi vào b ch a n c ng m.ụ ể ứ ướ ầ
Em hãy cho bi t m c đích c a hai cách làm trên.ế ụ ủ
b. Oxi hóa hoàn toàn 10,52 gam h n h p ba kim lo i d ng b t Fe, Al, Cu b ng oxi thu đ c 17,4 gam h nỗ ợ ạ ạ ộ ằ ượ ỗ
h p oxit. Vi t các ph n ng x y ra và tìm th tích nh nh t c a dung d ch HCl 2,0M đ hòa tan v a h tợ ế ả ứ ả ể ỏ ấ ủ ị ể ừ ế
l ng h n h p oxit trên.ượ ỗ ợ
----------------H t----------------ế
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ

Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có l i gi i)ả ử ệ ể ế ờ ả
S GIÁO D C VÀ ĐÀO T OỞ Ụ Ạ
H U GIANGẬ
ĐÁP ÁN
HDC ĐỀ THI CHỌN HỌC SINH GIỎI LỚP 9
NĂM HỌC: 2022 – 2023
Môn thi: Hóa học – Ngày thi:
01/03/2023
Thời gian: 150 phút (không kể thời gian
giao đề)
Câu 1 (5,0 đi m)ể .
1. Hãy cho bi t các ch t ế ấ X, Y, Z, T, M và hoàn thành s đ chuy n hóa sau:ơ ồ ể
(1): X + H
2
SO
4
đ cặ
0
t
Y + SO
2
+ H
2
O
(2): T + CO
0
t
X + CO
2
(3): Y + KOH
Z + K
2
SO
4
(4): X + Y
M
(5): Z
0
t
T + H
2
O
Gi iả
(1): 2Fe + 6H
2
SO
4
đ cặ
0
t
Fe
2
(SO
4
)
3
+ 3SO
2
+ 6H
2
O
(2): Fe
2
O
3
+ 3CO
0
t
2Fe + 3CO
2
(3): Fe
2
(SO
4
)
3
+ 6KOH
2Fe(OH)
3
↓ + 3K
2
SO
4
(4): Fe + Fe
2
(SO
4
)
3
3FeSO
4
(5): 2Fe(OH)
3
0
t
Fe
2
O
3
+ 3H
2
O
1.2. M t b n h c sinh đã làm 5 thí nghi m v i 5 ch t khác nhau c a ộ ạ ọ ệ ớ ấ ủ X và đ u cho k t t a sau ph n ng.ề ế ủ ả ứ
Ph ng trình hóa h c chung có d ng nh sau:ươ ọ ạ ư X+ Ba(NO
3
)
2
Y↓ + NaNO
3
Tìm 5 ch t th a mãn và vi t các ph ng trình c a ph n ng hóa h c đã x y ra?ấ ỏ ế ươ ủ ả ứ ọ ả
Gi iả
(1): Na
2
SO
4
+ Ba(NO
3
)
2
BaSO
4
↓ + 2NaNO
3
(2): Na
2
CO
3
+ Ba(NO
3
)
2
BaCO
3
↓ + 2NaNO
3
(3): Na
2
SO
3
+ Ba(NO
3
)
2
BaSO
3
↓ + 2NaNO
3
(4): 2Na
3
PO
4
+ 3Ba(NO
3
)
2
Ba
3
(PO
4
)
2
↓ + 6NaNO
3
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ
Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có l i gi i)ả ử ệ ể ế ờ ả
(5): Na
2
SiO
3
+ Ba(NO
3
)
2
BaSiO
3
↓ + 2NaNO
3
Câu 2 (5,0 đi m)ể .
2.1. Có 4 ng nghi m, m i ng ch a m t dung d ch mu i (không trùng kim lo i cũng nh g c axit) t ố ệ ỗ ố ứ ộ ị ố ạ ư ố ừ
nh ng kim lo i: Pb, Mg, K, Ba và nh ng g c axit: nitrat, cacbonat, sunfat, clorua.ữ ạ ữ ố
a) Hãy cho bi t dung d ch mu i ch a trong 4 ng nghi m trên.ế ị ố ứ ố ệ
b) Trình bày ph ng pháp hóa h c nh n bi t t ng dung d ch trong ng nghi m.ươ ọ ậ ế ừ ị ố ệ
Gi iả
a) 4 dung d ch c n tìm là: Pb(NOị ầ
3
)
2
, MgSO
4
, K
2
CO
3
, BaCl
2
.
b) Dùng HCl đ c phân bi t đ cặ ệ ượ
Pb(NO
3
)
2
vì t o k t t a tr ng: Pb(NOạ ế ủ ắ
3
)
2
+ 2HCl → PbCl
2
↓ + 2HNO
3
K
2
CO
3
vì có khí bay ra: K
2
CO
3
+ 2HCl → 2KCl + CO
2
↑ + H
2
O
Dùng H
2
SO
4
đ nh n ra BaClể ậ
2
vì t o k t t a tr ng, còn l i là MgSOạ ế ủ ắ ạ
4
:
BaCl
2
+ H
2
SO
4
→ BaSO
4
↓ + 2HCl
2.2. Hình v d i đây mô t các đi u ch oxi trong phòng thí nghi mẽ ướ ả ề ế ệ
a) Hãy cho bi t t i sao oxi đ c đi u ch theo ph ng pháp đ y n c?ế ạ ượ ề ế ươ ẩ ướ
b) T i sao ng nghi m đ ng KMnOạ ố ệ ự
4
l i l p h i chúc xu ng và khi k t thúc thí nghi m ph i tháo ng d n ạ ắ ơ ố ế ệ ả ố ẫ
khí tr c khi t t đèn c n?ướ ắ ồ
c) Đ thu đ c 112 ml oxi đktc c n ph i dùng bao nhiêu gam KMnOể ượ ở ầ ả
4
bi t hi u su t ph n ng là 80%?ế ệ ấ ả ứ
Gi iả
a) Vì oxi ít tan trong n c và không ph n ng v i n c.ướ ả ứ ớ ướ
b) ng nghi m l p KMnOỐ ệ ắ
4
ph i h i chúc xu ng đ nh ng gi t n c b ng ng t không ch y ng c l i ả ơ ố ể ữ ọ ướ ị ư ụ ả ượ ạ
làm n t, v ng do s chênh l ch nhi t đ .ứ ỡ ố ự ệ ệ ộ
N u t t đèn c n tr c thì gi a ng nghi m n m ngang và bên ngoài có s chênh l ch áp su t và nhi t đ ế ắ ồ ướ ữ ố ệ ằ ự ệ ấ ệ ộ
do đó n c t bên ngoài b hút vào ng nghi m n m ngang do đó có th làm v ng nghi m.ướ ừ ị ố ệ ằ ể ỡ ố ệ
c) 2KMnO
4
0
t
K
2
MnO
4
+ MnO
2
+ O
2
s mol KMnOố
4
= 2.s mol Oố
2
= 0,01 mol m = 158 : 80% = 1,975 gam.
Câu 3 (5,0 đi m)ể .
3.1. Đ i s ng c a th c v t và đ ng v t ph thu c vào pH c a môi tr ng. M t s cây tr ng thích h p v iờ ố ủ ự ậ ộ ậ ụ ộ ủ ườ ộ ố ồ ợ ớ
đ t chua (đ t axit) có pH t 4 đ n 6. M t s khác l i thích h p v i đ t ki m có pH t 8 đ n 9. Cá thích h pấ ấ ừ ế ộ ố ạ ợ ớ ấ ề ừ ế ợ
v i n c có pH b ng 7. Em hãy tính xem c n thêm vào các dung d ch d i đây bao nhiêu ml dung d chớ ướ ằ ầ ị ướ ị
NaOH 0,01M ho c HCl 0,01M đ dung d ch sau khi thêm có pH b ng 7. ặ ể ị ằ
a. 100 ml dung d ch Ca(OH)ị
2
0,01M.
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ

Đây là b n xem th , vui lòng mua tài li u đ xem chi ti t (có l i gi i)ả ử ệ ể ế ờ ả
b. 100 ml dung d ch g m HNOị ồ
3
0,015M và H
2
SO
4
0,005M.
Gi iả
Môi tr ng trung tính có pH = 7 do đó axit ph i ph n ng v a đ v i bazườ ả ả ứ ừ ủ ớ ơ
a. Ca(OH)
2
+ 2HCl
CaCl
2
+ 2H
2
O
mol: 0,001 → 0,002
V
HCl
= 0,002 : 0,01 = 0,2 lít = 200 ml.
a. NaOH + HNO
3
NaNO
3
+ H
2
O
mol: 0,0015 ← 0,0015
2NaOH + H
2
SO
4
Na
2
SO
4
+ 2H
2
O
mol: 0,001 ← 0,0005
s mol NaOH = 0,0025 mol ố V
NaOH
= 0,0025 : 0,01 = 0,25 lít = 250 ml.
3.2. H p ch t ợ ấ A và B là hai ch t ch ch a các nguyên t ấ ỉ ứ ố X, Y. Thành ph n ph n trăm c a nguyên t ầ ầ ủ ố X trong
A và B l n l t là 30,49% và 25,9%. Bi t r ng A, B có kh i l ng phân t l n l t là 46 đvC và 108 đvC.ầ ượ ế ằ ố ượ ử ầ ượ
a) Bi t r ng công th c phân t c a ế ằ ứ ử ủ A là XY
2
. Tìm công th c c a ứ ủ A, B.
b) Hoàn thành ph n ng sau:ả ứ
A + O
2
+ H
2
O
Z
B + H
2
O
Z
Gi iả
a) A có d ng XYạ
2
trong đó: X + 2Y = 46 và X = 46.30,49% X = 14 (N) và Y = 16 (O) A là NO
2
+ B có d ng: Nạ
x
O
y
14x + 16y = 108 và 14x = 108.25,9% x = 2; y = 5 B là N
2
O
5
.
b) Các ph n ng x y ra:ả ứ ả
4NO
2
+ O
2
+ 2H
2
O → 4HNO
3
N
2
O
5
+ H
2
O → 2HNO
3
Câu 4 (5,0 đi m)ể .
4.1. Trong “viên s i” có nh ng ch t hóa h c có tác d ng ch a b nh, ngoài ra còn còn m t ít b t natriủ ữ ấ ọ ụ ữ ệ ộ ộ
hidrocacbonat và b t axit h u c nh axit xitric (axit có trong qu chanh). Khi “viên s i” g p n c t o raộ ữ ơ ư ả ủ ặ ướ ạ
dung d ch axit. Dung d ch này tác d ng v i NaHCOị ị ụ ớ
3
sinh ra khí cacbonic theo ph ng trình sau:ươ
HOC
3
H
4
(COOH)
3
+ 3NaHCO
3
→ HOC
3
H
4
(COONa)
3
+ 3CO
2
↑ + 3H
2
O
Khí này thoát ra kh i c c n c d i d ng b t khí.ỏ ố ướ ướ ạ ọ
a. Tính th tích COể
2
thu đ c đktc n u trong “viên s i” có ch a 0,42 gam NaHCOượ ở ế ủ ứ
3
bi t l ng axit xitric ế ượ
t o ra đ đ hòa tan h t l ng NaHCOạ ủ ể ế ượ
3
.
b. D n toàn b khí COẫ ộ
2
thu đ c trên qua 100 ml dung d ch Ca(OH)ượ ở ị
2
0,03M thì thu đ c bao nhiêu gam ượ
k t t a.ế ủ
Gi iả
a. Ph n ng x y ra: HOCả ứ ả
3
H
4
(COOH)
3
+ 3NaHCO
3
→ HOC
3
H
4
(COONa)
3
+ 3CO
2
↑ + 3H
2
O
s mol COố
2
= s mol NaHCOố
3
= 0,005 mol V
CO2
= 0,112 lít.
b. Ph n ng x y ra:ả ứ ả
M i th c m c vui lòng xin liên h hotline: 084 283 45 85ọ ắ ắ ệ